Hämerythrin
| Hämerythrin ( Dendrostomum dyscritum ) | ||
|---|---|---|
| ||
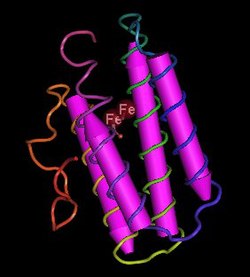
| Modell av hemerytrinmonomeren fra peanøttorm ( Dendrostomum dyscritum ) ifølge PDB 1HMO | ||
| Masse / lengde primærstruktur | 113 aminosyrer | |
| Sekundær til kvartær struktur | Homooktamer | |
| Kofaktor | jern | |
| Identifikator | ||
| Eksterne ID-er | ||
| Hendelse | ||
| Parent taxon | Hvirvelløse dyr | |
Hämerythrine er respiratoriske blodproteiner , som i en rekke marine virvelløse dyr (for eksempel B. leddormer , sipunkulider , brachiopoder ) som oksygentransportfunksjonen. Så de utfører de samme oppgavene som hemoglobin og myoglobin hos høyere dyr. Det er ingen kjente stammer av dyr som lever på land som har hemerytrin.
Til tross for navnet deres tilhører ikke hemerytrinene heme- enzymene. Det aktive sentrum av den reduserte tilstanden er representert av to jern (II) -ioner broet av en hydroksydligand og to karboksylater.Koordinasjonssfærene til jernsentrene kompletteres av to eller tre histidinligander . I løpet av binding av dioksygenmolekylet oksiderer det ganske enkelt begge jernsentre og reduseres i seg selv til peroksidionet. Samtidig tar det over en proton fra hydroksidobroen. Det dannede hydroperoksidionet blir deretter bundet til det femkoordinatiske jernsenteret og til den brodannende oksofunksjonen med en hydrogenbinding. Fargen på det oksyderte molekylet er lilla, når det er avoksidert er det fargeløst; molekylmassen er 108 kDa .
Se også
- Jernmetabolisme
- Hemocyanin , et lignende kobberholdig protein med en tilsvarende funksjon.
hovne opp
Individuelle bevis
- ↑ InterPro-oppføring
- ↑ R. Sauermost (red.): Dictionary of Biology på CD-Rom . Spektrum Akademischer Verlag, München 2004, ISBN 3-8274-0356-1 .
- ^ R. Wehner , W. Gehring : Zoologie . 24. utgave. Georg Thieme Verlag, Stuttgart, New York 2007, ISBN 978-3-13-367424-9 , pp. 339 (tabell 4.4).
