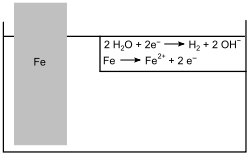Korrosjonsbeskyttelse
Ettersom korrosjonsbeskyttende tiltak kalles for å unngå skader forårsaket av korrosjon, kan det være forårsaket av metalliske komponenter. Siden absolutt korrosjonsbestandighet ikke kan oppnås, er beskyttelsestiltakene som er tatt generelt rettet mot å redusere hastigheten på etsende angrep i en slik grad at skade på komponenten kan unngås i løpet av dens levetid.
Generell
Begrepet korrosjon brukes ikke lenger bare for metalliske materialer , men også for glass, plast , bygningsmaterialer, etc. Det angripende mediet kalles et etsende middel. Hvis funksjonen til en komponent svekkes av et korrosjonsangrep, blir dette referert til som korrosjonsskader.
I henhold til DIN EN ISO 8044 skilles det mellom følgende typer korrosjon:
- Overflate korrosjon , hvor overflaten er skadet jevnt
- Velkorrosjon , der overflaten blir skadet ujevnt og alvorlig
- Pitting korrosjon som bare ødelegger små områder av overflaten
- Sprekkkorrosjon , der materialoverflaten i smale sprekker, z. B. i sveiser blir angrepet

For å forhindre kjemiske korrosjonsprosesser, er det forskjellige metoder og prosedyrer som vanligvis kalles korrosjonsbeskyttelse. Metallisk korrosjonsbeskyttelse er diskutert mer detaljert nedenfor.
Det skilles mellom aktiv og passiv korrosjonsbeskyttelse. Basert på begrepet "konstruktiv trebeskyttelse ", kan et visst nivå av korrosjonsbeskyttelse også oppnås med metalliske materialer gjennom en passende konstruksjon.
Passiv korrosjonsbeskyttelse
Passiv korrosjonsbeskyttelse inkluderer alle tiltak som oppnår en skjermende effekt mot etsende medier.
Konstruktiv korrosjonsbeskyttelse
Tiltak som taktekking, sprutbeskyttelse og en gradient for drenering av væsker reduserer kontakt med etsende medier som vann.
Korrosjonsbeskyttelse gjennom belegg
Et materiale kan nesten fullstendig isoleres fra etsende gasser og væsker ved hjelp av passende belegg som belegg . Bindemidler som syntetiske harpikser er ofte tilsatt tilsetningsstoffer som jernholdig jernoksid - pigmenter beriket for å forbedre skjermingseffekten og øke motstanden. Pigmenter som sinkstøv , sinkfosfat , sinkkromat eller rød bly blir også referert til som aktive pigmenter fordi de også har en kjemisk eller galvanisk rustbeskyttelseseffekt.
Som belegningsmaterialer påført i flytende, pasta- eller pulverform, brukes syntetiske harpikser som EP eller PU , plast som PVC og plastfilmer, oljer , lakk , gummi eller harde parafiner .
Uorganiske eller metalliske belegg kan dannes, for eksempel ved passivering eller ved å påføre konverteringslag med en mer ikke-metallisk karakter eller konverteringslag som fosfatering , kromering , anodisering , hardanodisering og varmforsinkning , som igjen danner en beskyttende passiveringslag, og hvis det er skadet, beskytter underlaget som en offeranode .
Store og lange rørledninger laget av stål for vanntransport er fortrinnsvis foret med et indre belegg av sementmørtel for korrosjonsbeskyttelse . Korrosjonsbestandigheten kan forbedres ytterligere ved å tilsette egnet plast. De viktigste fordelene med denne typen belegg er:
- lave kostnader
- stort sett motstandsdyktig mot etsende vann opp til en pH-verdi på ca.> 4,0; denne motstanden gjelder ikke avionisert vann .
- Selvhelbredelse av smale sprekker som går til jernoverflaten
Også, ved elektrolytisk eller kjemisk genererte, metalliske dekksjikt av tinn , gull , nikkel , kobber , krom , sink eller legeringsbelegg som nikkel-fosfor ( kjemisk nikkel ) eller nikkel-sink tilveiebringe en korrosjonsbeskyttelse. Finner også galvanisering (en varmeprosess) er mye brukt. Den beskyttende effekten av metallag er basert på egenskapene til ikke å tære på seg selv (edle metaller) eller på barriereeffekten gjennom dannelsen av et tett oksidlag på overflaten (såkalt passivt lag), som fungerer som korrosjonsbeskyttelse. Noen metaller er i stand til å danne et dekklag "av seg selv" som beskytter grunnmaterialet, slik som patina på kobber eller sink.
Når det gjelder metallag, avhenger den beskyttende effekten i tilfelle lagskader av lagstypen. Mindre edle lag beskytter arbeidsstykket katodisk og fungerer som en offeranode - laget løses fortrinnsvis og opprettholder dermed funksjonen til komponenten så lenge som mulig. Enda mindre feil eller skader i laget har derfor i utgangspunktet ingen alvorlige effekter (såkalt fjerneffekt). Et klassisk eksempel er galvanisering av stål , men også beskyttelse av hydrauliske konstruksjoner som Som skip, låser, spunt, båt deler og skinnene ved å feste offeranoder av sink - aluminium - eller magnesium - legeringer . Flere edle lag enn grunnmaterialet beskytter det anodisk, men har den største ulempen at hvis laget blir skadet, blir det mindre edle grunnmaterialet under oppløst raskere ( kontaktkorrosjon ).
En viss korrosjonsbeskyttelse tilbys av z. B. Tinnplate - her brukes tinn som belegningsmateriale slik at maten også kan pakkes med den. Imidlertid, etter en tid, hvis boksen er åpen, dannes tinnioner som er giftige for z. B. Cress-arbeid. Derfor bør boksen også males .
For rustomformere oppnås korrosjonsbeskyttelse ved å fjerne de originale, porøse jernoksidene og ytterligere oksidere det øvre jernlaget for å danne et Fe-oksid med en glatt overflate som forhindrer at vann absorberes og dermed forhindrer ytterligere rusting. Fosforsyre eller tannin brukes til dette, blandet med tilsetningsstoffer. Etter behandlingen er forsegling med polymerlakk vanlig for å oppnå permanent beskyttelse. Det tilbys også produkter som er ment å kombinere begge funksjonene.
Aktiv katodisk korrosjonsbeskyttelse
Aktiv katodisk korrosjonsbeskyttelse med ekstern strøm
Katodisk korrosjonsbeskyttelse - kort sagt KKS - kan oppnås ved å påføre en spenning til en ekstern strømanode . Når det gjelder råolje, gass, fjernvarme og vannledninger, for eksempel, senkes elektroder i bakken noen få kilometer i en avstand på noen hundre meter fra ledningen. Disse elektrodene danner en krets med rørledningen og bakken . Ved å gjøre dette skal spenningen til det galvaniske elementet som består av jord og metallrørledning balanseres, som er i størrelsesorden noen få volt . Motspenningen som kreves avhenger også av vanninnholdet og jordens sammensetning. For å skille individuelle KKS-områder brukes isolerende separasjonspunkter i ledningen, som avbryter ledningsevnen til rørledningen. Dette gjør det mulig å bedre kontrollere beskyttelsesstrømmen og å kunne isolere feil.
Ved brobygging , spesielt på motorveibroer, utføres KKS ved hjelp av en imponert strømanode. For dette formålet påføres et anodegitter laget av belagt titan på overflaten som skal beskyttes, og ca. 2 cm til 3 cm injiseres med sprøytebetong . Sprøytebetongen fungerer som en elektrolytt . Strømmen mates inn i armeringen via en likeretter og dermed oppnås katodisk beskyttelse. Tiltaket kontrolleres kontinuerlig med et automatisk overvåkingssystem.
I tillegg brukes elektroder laget av titanbelagt kobber ( engelsk: titanium clad kobber ) og sølv-sølvklorid for katodisk korrosjonsbeskyttelse .
Aktiv katodisk korrosjonsbeskyttelse uten ekstern strøm


Aktiv korrosjonsbeskyttelse uten ekstern strøm beskytter primært metaller som ofte kommer i kontakt med etsende stoffer som vann. Et mindre edelt stoff tjener som anoden, som ofres for det edlere metallet. For korrosjonsbeskyttelse ved bruk av offeranoder brukes anoder laget av forskjellige materialer, avhengig av applikasjonen. Offeranoden må være ledende koblet til metallet som skal beskyttes for å oppnå beskyttelse. En strøm på noen få milliampere strømmer i den resulterende kretsen, som mates fra redoksreaksjonen av oksydasjonen av denne offeranoden .
Når det gjelder jern og magnesium, fortsetter reaksjonen som følger: Så snart magnesium eller jern kommer i kontakt med vannet, oksyderes det til Mg 2+ eller Fe 2+ . I følge den elektrokjemiske serien er det en potensiell forskjell mellom magnesium og jern på 1,9 V (standardpotensialer ved 25 ° C; 101,3 kPa; pH = 0; ionaktiviteter = 1). Siden magnesium, med en potensiell forskjell på hydrogen på -2,362 V, har et betydelig mer negativt potensial enn jern med -0,41 V, oksyderes magnesium ved anoden og jernet reduseres ved å akseptere elektroner. Denne reaksjonen foregår veldig sakte, men kan akselereres ved endrede forhold. Elektronene treffer vannet dele den inn i H- 2 og 2-OH - . Jernet endres ikke fordi det kan ta opp elektronene som magnesium gir fra seg. Magnesium, derimot, oppløses gradvis og må fornyes etter at det er blitt helt nedbrutt.
Magnesiumanoden er plassert i midten av sfæriske beholdere, slik at potensialet forutsetter den samme verdien på alle overflater av beholderen. Når det gjelder sylindriske beholdere, er anoden festet på en slik måte at det er omtrent samme avstand fra beholderbunnen som fra de sirkulære beholderveggene. Anoden er derfor kortere enn dybden på beholderen. I mange tilfeller installeres anoden isolert fra beholderveggen, da ellers ville en høyere beskyttelsesstrøm strømme ved installasjonsstedet, mens resten av beholderen ville være mindre godt beskyttet. Kretsen lukkes deretter via en kabel som er koblet til anoden og beholderveggen på utsiden av beholderen. Et amperemeter for likestrøm kan også sløyfes inn i kabelen, som måler strømmen i milliampereområdet og dermed viser funksjonen til anoden.
For å beskytte skip laget av stål mot korrosjon fra sjøvannet, er magnesiumanoder festet på utsiden av skroget med jevne mellomrom.
I den elektrokjemiske serien er jern mer positivt enn sink , dvs. sink er mindre edelt enn jern og representerer anoden i det galvaniske elementet, og jern er katoden. Jern, som et edelt metall, er katodisk beskyttet til sink har korrodert bort.
Standardiserte miljøtester utføres for å bestemme korrosjonsbestandigheten til belegg. Her blir for eksempel overflater lett skadet med riper testanordninger og deretter utsatt for en saltspray .
eksempel
Et enkelt forsøk på korrosjonsbeskyttelse:
- En ubeskyttet jernspiker plasseres i forsuret saltvann. Etter en stund oppløses og korroderer jern (hvis det ikke er noen offeranode). Videre er hydrogen (H 2 er) dannet på jernnagler.
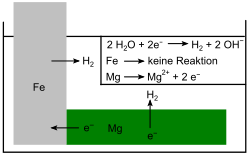
- Jernspikeren er beskyttet med mindre edelt magnesium. Et lokalt element dannes ved at magnesium (Mg) fungerer som en anode og dermed ofrer for jern (Fe). Også her dannes hydrogen H2 på Fe-katoden. Årsaken til dette er elektronstrømmen (e - ) fra Mg til Fe, siden Mg er mindre edel enn jern og derfor har en større reduserende kraft.
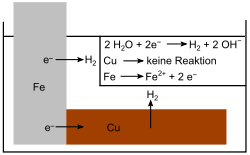
- Hvis det mer edle kobberet (Cu) brukes i stedet for magnesium, fungerer jernet som en anode, og kobberet kan ikke beskytte jernet mot korrosjon. Jernet oksyderes raskere enn om det ikke er noe kobber, fordi elektronstrømmen nå går fra Fe til Cu.
Se også
- Varmforsinking
- Filmgalvanisering
- Society for Corrosion Protection
- Sinkflakebelegg
- E-post
- Varmskruemasse
- Sherardisering (diffusjonsgalvanisering)
litteratur
- Bernhard Wietek : KKS i broreparasjoner . KKS-seminar i Innsbruck 2000.
- Ulrich Bette, W. Vesper: Lommebok for katodisk korrosjonsbeskyttelse . 7. utgave. Vulkan, 2005, ISBN 3-8027-2932-3 .
- RP Gieler, A. Dimmig-Osburg: Plast for bygningsvern og betongreparasjon . Birkhäuser Verlag, Berlin 2006, ISBN 3-7643-6345-2 .
Individuelle bevis
- ↑ Hva er aktiv korrosjonsbeskyttelse? Hentet 30. mars 2021 .
- ↑ DIN EN ISO 12 944 del 1
- ^ B. Heinrich, H. Hildebrand, M. Schulze, W. Schenk, i: 3R internasjonal. 17. bind, utgave 7. juli 1978, s. 455.
- ^ W. Schwenk, i: Zentralblatt für Industriebau. Volum 26, nr. 5, september 1980, s. 309.
- ^ W. Schwenk, i: Zentralblatt für Industriebau. Volum 26, nr. 5, september 1980, s. 308.
- ↑ hammerite.de: Teknisk datablad for rustbeskyttelsesmaling , åpnet 15. april 2016.
- ↑ motipdupli.com: Teknisk datablad Bob Rostversiegelung , åpnet 15. april 2016.