Zanamivir
| Strukturell formel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
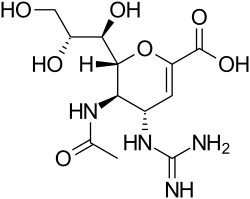
| ||||||||||||||||||||||
| Generell | ||||||||||||||||||||||
| Ikke-proprietært navn | Zanamivir | |||||||||||||||||||||
| andre navn |
(4 S , 5 R , 6 R ) -5-acetylamino-4-guanidino-6 - [(1 R , 2 R ) -1,2,3-trihydroxypropyl] -5,6-dihydro-4- H -pyran- 2-karboksylsyre |
|||||||||||||||||||||
| Molekylær formel | C 12 H 20 N 4 O 7 | |||||||||||||||||||||
| Eksterne identifikatorer / databaser | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Legemiddelinformasjon | ||||||||||||||||||||||
| ATC-kode | ||||||||||||||||||||||
| Narkotikaklasse | ||||||||||||||||||||||
| Virkningsmekanismen |
Inhibering av viral neuraminidase, inhibering av frigjøring av nydannede influensa A- og B-virus |
|||||||||||||||||||||
| eiendommer | ||||||||||||||||||||||
| Molarmasse | 332,31 g · mol -1 | |||||||||||||||||||||
| Fysisk tilstand |
fast |
|||||||||||||||||||||
| Smeltepunkt |
256 ° C (zanamivir sesqui hydrat ) |
|||||||||||||||||||||
| sikkerhetsinstruksjoner | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Så langt som mulig og vanlig, brukes SI-enheter . Med mindre annet er angitt, gjelder oppgitte data standardbetingelser . | ||||||||||||||||||||||
Zanamivir er det første stoffet fra gruppen som består av neuraminidasehemmere , som brukes til behandling av influensa (influensa) . Den narkotika Relenza ® ble utviklet av Biota Holdings , Australia , det har blitt markedsført av GlaxoSmithKline siden 1999 og krever en medisinsk resept .
tilstand av forskning
Som en hemmer av viral neuraminidase kan det forhindre frigjøring av ytterligere virus og dermed forekomsten eller progresjonen av sykdommen, forutsatt at den administreres i løpet av de første 48 timene. I 2014 avslørte forskning fra Cochrane Collaboration tvil om effektiviteten og sikkerheten til zanamivir og oseltamivir . En metaanalyse fra Cochrane Collaboration viste at behandling med zanamivir hos voksne reduserte sykdomsvarigheten fra 6,6 til 6 dager. Imidlertid hadde zanamivir ingen effekt på frekvensen av alvorlige sykdomsformer som lungebetennelse eller bronkitt.
applikasjon
Siden zanamivir bare mottas ca. 2% fra mage-tarmkanalen , må det være som et pulver ved bruk av inhalatoren Diskhaler .
Studier
terapi
De første kliniske studiene med zanamivir for behandling av infeksjoner med influensavirus fant sted i 1994/1995.
Hos unge pasienter med en gjennomsnittsalder på 30 år med påvist influensainfeksjon ble febervarigheten redusert fra 6,8 dager når den fikk placebo til 5,2 dager når den ble gitt zanamivir, forutsatt at den ble tatt innen 30 timer etter at symptomene begynte. Tiden til klinisk forbedring / frihet fra symptomer var 6,3 dager i placebogruppen mot 5,4 dager i zanamivir-gruppen.
Andre studier bekreftet i stor grad disse resultatene og attesterte zanamivir en reduksjon i febervarighet fra 6 dager under placebo til 4,5 dager eller en reduksjon i varigheten av symptomfri behandling med en dag.
I Tyskland erklærte den føderale komiteen for leger og helseforsikringsfond at stoffet kunne dispenseres i 2000.
profylakse
En randomisert studie viste ved 1.107 studenter i løpet av en influensa - epidemi at den daglige administrasjon Relenzas over en periode på 28 dager resulterte i en reduksjon i influensasykdom med 6% i placebogruppen til 2% i den Relenzagruppe: I 34 554 studiedeltakere i placebogruppen og 11 av 553 studiedeltakere i zanamivir-gruppen. 19 personer i placebogruppen og 3 i zanamivir-gruppen led av feber, noe som betyr at for hver 35 personer som ble behandlet, kunne en influensa forhindres.
Bivirkninger
De vanligste bivirkningene hos personer med bronkialastma eller kronisk obstruktiv lungesykdom er mer enn 20% reduksjon i lungefunksjon (FEV1 eller toppstrøm ). Noen ganger oppstod alvorlig bronkospasme med isolerte dødsfall her .
diskusjon
Det foreligger ingen data om effekten og sikkerheten til dette stoffet hos eldre pasienter og risikogrupper, og det er heller ikke klare data om effekten på forekomsten av komplikasjoner og dødsfall.
Det er fortsatt få data tilgjengelig om bruk av zanamivir hos pasienter med nedsatt nyre- eller leverfunksjon og ved hjertesvikt .
Produksjon
Forskjellige flertrinnssynteser for zanamivir, startende fra N - acetylneuramininsyre , er beskrevet i litteraturen.
Individuelle bevis
- ^ The Merck Index . En leksikon om kjemikalier, medisiner og biologiske stoffer . 14. utgave, 2006, s. 1744, ISBN 978-0-911910-00-1 .
- ↑ Det er ennå ikke en harmonisert klassifisering for dette stoffet . En merking av zanamivir i den klassifisering og merking Opptelling av den europeiske kjemikaliebyrået (ECHA), som ble hentet 12. juli 2020 blir gjengitt fra en selv klassifisering av distributøren .
- ↑ a b c Tom Jefferson, Mark A Jones, Peter Doshi, Chris B Del Mar, Rokuro Hama, Matthew J Thompson, Elizabeth A Spencer, Igho Onakpoya, Kamal R Mahtani, David Nunan, Jeremy Howick, Carl J Heneghan: Neuraminidase-hemmere for forebygging og behandling av influensa hos friske voksne og barn. I: British Medical Journal (2014), online forpublisering. doi : 10.1002 / 14651858.CD008965.pub4 .
- ↑ Monto AS, Robinson DP, Herlocher ML et al. Zanamivir i forebygging av influensa blant friske voksne: en randomisert kontrollert studie. JAMA. 1999 7. juli; 282 (1): 31-5, PMID 10404908 . Fulltekst , åpnet 26. september 2008.
- ^ Axel Kleemann , Jürgen Engel, Bernd Kutscher og Dietmar Reichert: Pharmaceutical Substances , 4. utgave (2000), 2 bind utgitt av Thieme-Verlag Stuttgart, ISBN 978-1-58890-031-9 ; online siden 2003 med halvårlige tillegg og oppdateringer.
