Atrieflimmer
| Klassifisering i henhold til ICD-10 | |
|---|---|
| I48.0 | Atrieflimmer, paroksysmal |
| I48.1 | Atrieflimmer, vedvarende |
| I48.2 | Atrieflimmer, kronisk |
| I48.9 | Atrieflimmer og atrieflimmer, uspesifisert |
| ICD-10 online (WHO versjon 2019) | |
Atrieflimmer , den vanligste formen og årsaken til absolutt arytmi , er en midlertidig ( paroksysmal eller intermitterende ) eller permanent (permanent) hjertearytmi med forstyrret aktivitet i atriene . Vanlige forkortelser er AF eller AFib (fra engelsk A trial Fib rillation ), Vfli, VoFli, VHF og VHFli .
Atrieflimmer er den vanligste signifikante hjerterytmeforstyrrelsen, rundt 300 000 mennesker i Tyskland alene har atrieflimmer. Pasienter merker ikke omtrent 70% av atrieflimmeranfall. De berørte klager vanligvis over uspesifikke klager som plutselig tap av ytelse, tretthet, hjertebank eller søvnproblemer. Palpitasjoner merker 70–80% av symptomene.
Atrieflimmer er assosiert med økt risiko for hjerneslag og hjertesvikt . Dødeligheten ( dødeligheten ) økes. For de fleste pasienter tillater medisinering eller invasiv behandling en normal eller nesten normal livsstil.
fordeling
Atrieflimmer forekommer hos 1–2% av befolkningen; Det er med andre ord rundt seks millioner mennesker berørt i Europa. De prevalens øker fra mindre enn 0,5% i alders i henhold 40 til opp til 15% hos personer over 80 år. Menn er oftere rammet enn kvinner, og livstidsrisikoen for mennesker over 40 er rundt 25%. Risikoen for atrieflimmer øker betydelig med alvorlighetsgraden av en eksisterende hjertesykdom. Ved hjertesvikt finnes atrieflimmer i 30–40% av tilfellene.
årsaker
Atrieflimmer kan forekomme uten en identifiserbar årsak (idiopatisk) eller uten en identifiserbar underliggende sykdom (ensom atrieflimmer) . Dette er tilfelle hos rundt en tredjedel av pasientene, oftere med paroksysmal (ca. 45%) enn med permanent atrieflimmer (ca. 25%). Omtrent 20-30% av pasientene lider av koronararteriesykdom , også ca 20-30% av arteriell hypertensjon (høyt blodtrykk), nesten 20% av en hjerteventilfeil (som alvorlig mitralventilstenose ) og ca. 15% fra en hjertemuskelsykdommer . Den vanligste ekstrakardiale årsaken til atrieflimmer hos rundt 0,5–3% av pasientene er manifest eller til og med latent overaktiv skjoldbruskkjertel ( hypertyreose , tyrotoksikose ) med fem til seks ganger økt risiko for atrieflimmer. Atrieflimmer kan også være forårsaket av en elektrisk ulykke eller oppstå etter operasjoner, spesielt de første dagene etter thoraxkirurgi (bypassoperasjoner, lungereseksjoner). Observasjonsstudier har vist at alkoholforbruk øker hyppigheten av atrieflimmer på en doseavhengig måte og er assosiert med strukturelle endringer i venstre atrium (forstørrelse, fibrose). Også, søvnapné syndrom er assosiert med en økt sannsynlighet for å utvikle atrieflimmer. En studie har vist at søvnapnébehandling reduserer risikoen for tilbakefall av atrieflimmer med 42%.
Elektrofysiologisk holdes to hovedmekanismer ansvarlige for atrieflimmer:
- Såkalte triggerarytmier ( atriale ekstrasystoler og høyfrekvente fokale atriale takykardier) som utløsere, som ofte har sitt utspring i en av lungevene , og
- Sirkulære eksitasjoner basert på atomerens anatomiske og elektrofysiologiske egenskaper, som fremmer utvikling og vedlikehold av atrieflimmer.
Atrieflimmer , andre supraventrikulære arytmier og påvirkningen av det autonome nervesystemet på hjertefrekvensen kan også føre til atrieflimmer. Atrieflimmer i seg selv fører også til "tilpasningsprosesser" av atriene (atriell ombygging) , som igjen kan opprettholde atrieflimmer ("atrieflimmer opprettholder atrieflimmer").
Denne "ombyggingen" påvirker atriens elektriske, kontraktile og ultrastrukturelle egenskaper.
- "Elektrisk ombygging" refererer til en forkortelse av handlingspotensialet og dermed også den atriale ildfaste perioden , forårsaket av en redusert tilstrømning av Ca 2+ -ioner i atriens muskelceller.
- Denne reduserte Ca 2+ tilstrømningen fører også til "kontraktil remodeling", et tap av kontraktil styrke i atriale muskler, som vedvarer i en stund selv etter vellykket kardioversjon .
- Svakheten i musklene fremmer også en økende utvidelse av atriene, som allerede er strukket av økt trykk. Denne utvidelsen fører igjen til hypertrofi , akselerert celledød og fibrose i atriale muskler, som er kjent som “ultrastrukturell ombygging”.
Bare de siste årene har det blitt funnet indikasjoner på genetisk predisposisjon for atrieflimmer:
- I 2002 og 2003, en hovedsakelig autosomal dominant arvelig mutasjon i den genet ble KCNQ1 beskrevet, noe som fører til en økt strøm av kaliumioner under repolarisering og således fremmer forekomsten av atrieflimmer.
- I 2004 Fox et al. Publiserte resultatene av en prospektiv studie på 2243 avkom til pasientene i Framingham Heart Study ; denne prospektive studien viste blant annet en dobbelt så høy risiko for atrieflimmer hvis minst en av foreldrene allerede hadde atrieflimmer.
- En økt forekomst av AF har blitt demonstrert for arvelig kort og lang QT-syndrom , for Brugada syndrom og også for noen former for hypertrofisk kardiomyopati . Forskjellige andre genetiske defekter er også beskrevet i mellomtiden.
Sykdomsutbrudd
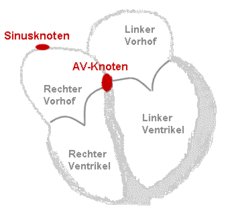
I normal tilstand, dvs. H. i sinusrytme stimuleres atriene og hjertekamrene i umiddelbar rekkefølge ca. 70 ganger per minutt (se fig. Hjertets struktur og ledning ). Atriens muskelsammentrekning fører til en ekstra blodfylling av kamrene, som også trekker seg sammen ca. 150 millisekunder senere. Denne funksjonen til atriene er sammenlignbar med en turboladere i en motor og øker hjertekamrenes slagvolum med ca. 15%.
Med atrieflimmer, derimot, går ikke-retningsbestemte elektriske eksitasjoner gjennom atriene. Dette fører til raske og uordnede bevegelser av veggene med en frekvens på 300 til 600 per minutt, flimringen . Under en frekvens på 300 per minutt er det en atrieflager . Et overgangsområde kalles atrieflimmer .
| Skjematisk fremstilling av spredning av eksitasjon i hjertet | ||
| med sinusrytme | med atrieflimmer | Legende |
Klinisk utseende
De viktigste konsekvensene av atrieflimmer er:
- Uregelmessig puls ( absolutt arytmi eller arytmi absoluta med pulsus irregularis et inaequalis ). Bremse- og filtreringsfunksjonen til AV-noden overfører bare omtrent 100 til 160 av de 350–600 atriale impulser per minutt til ventriklene med uregelmessige (noen ganger også med jevne mellomrom).
- Puls for fort ( takykardi ) i ubehandlet tilstand. Selv om AV-noden vanligvis beskytter ventriklene mot pulsfrekvenser på over 200 per minutt, er de typiske frekvensene 100 til 160 per minutt ikke økonomiske for hjertet på lang sikt og kan øke i løpet av dager til uker i tilfelle pasienter som er forberedt på å gjøre så alvorlig hjertemuskelsvakhet med hjertesvikt ( takykardiomyopati ). Det ekkokardiografiske bildet ligner på utvidet kardiomyopati (DCM)
- Puls for sakte ( bradykardi ), ofte forårsaket av medikamenter som reduserer pulsen. Sakte hjerterytme eller pauser kan være årsaker til besvimelse ( synkope ). Hvis det er en hyppig endring mellom raske og langsomme faser, snakker man om et bradykardi-takykardisyndrom.
- Tap av ordnet atriell sammentrekning med lett svekkelse av hjertets pumpekapasitet. I et ellers sunt hjerte spiller dette vanligvis ingen rolle og blir da vanligvis ikke lagt merke til. Ved et alvorlig skadet hjerte kan mangel på atriell sammentrekning føre til en betydelig forverring av treningskapasiteten.
- Økt risiko for emboli . Blodpropp ( tromber ) kan lett dannes i atriene (helst i venstre atriale vedheng ) på grunn av den endrede blodstrømmen . Disse tromber kan i sin tur løsne og føre til emboliske karoklusjoner i kroppen. Dannelsen av sfæriske tromber i venstre atrium kan også hindre utstrømningen av lungevene med mulig konsekvens av pulmonal hypertensjon . Cerebral emboli slag er spesielt fryktet . Mesenteriske infarkter på grunn av okklusjon av et tarmkar er også mindre vanlige .
- Svimmelhet eller tap av bevissthet kan oppstå når hjerteslaget stoppes etter at atrieflimmer (pre- automatisk pause ).
Klassifisering
Det er en rekke klassifiseringer for atrieflimmer.
Etter eksistensvarigheten , i henhold til de oppdaterte retningslinjene fra European Society of Cardiology (ESC) i
- først oppdaget,
- paroksysmal (eller intermitterende),
- vedvarende,
- langvarig vedvarende og
- permanent atrieflimmer
tildelt. Deretter blir atrieflimmer betraktet som paroksysmal hvis den avsluttes spontant innen 48 timer til syv dager etter det mistenkte utbruddet. Det kalles vedvarende hvis det stoppes av medisinsk eller elektrisk kardioversjon og behandles med rytmebehandling. Nylig, i den oppdaterte retningslinjen, har atrieflimmer som har eksistert i mer enn et år blitt beskrevet som vedvarende hvis det skal behandles på en rytmebevarende måte. Atrieflimmer klassifiseres som permanent hvis fortsettelse godtas og ingen rytmisk behandling utføres.
I 2011-versjonen av ICD-10-koden ble atrieflimmer kombinert med atrieflimmer og ikke videre delt inn. Som et resultat er epidemiologisk opptak i dette systemet praktisk talt ikke lenger mulig.
Avhengig av hjertefrekvensen målt i elektrokardiogrammet (EKG) , er også atrieflimmer i
- Bradyarytmi absoluta (langsom form for absolutt arytmi med en puls under 60 slag per minutt),
- normal frekvens absolutt arytmi (puls 60 til 100 slag per minutt) og
- Tachyarytmi absoluta (puls over 100 slag per minutt).
Relevant for bruk av nye legemidler i sammenheng med antikoagulantbehandling, men også for rytmekontroll, er klassifiseringen etter årsaken i
- klaffe , dvs. å starte fra den mitral ventil , og i
- ikke-valvulær atrieflimmer som tilsvarer andre årsaker (f.eks. høyt blodtrykk).
Hvis tidspunktet og situasjonen der atrieflimmer begynte er kjent, mellom
- vagal (vanligvis om natten) og
- sympatisk tone (ofte under stress, fysisk anstrengelse eller om morgenen etter å stå opp)
utløst atrieflimmer kan skille seg ut.
EHRA klassifisering
Klassifiseringen i henhold til symptomene i henhold til EHRA-poengsummen til European Heart Rhythm Association , basert på NYHA-klassifiseringen for hjertesvikt, er ny . Det kan brukes som et beslutningshjelpemiddel når det gjelder spørsmålet om rytmebehandling.
| scene | Alvorlighetsgraden av symptomer | definisjon |
|---|---|---|
| EHRA I | Ingen klager | Normal daglig aktivitet er ikke begrenset |
| EHRA II | Små klager | |
| EHRA III | Alvorlige klager | Normal daglig aktivitet er begrenset |
| EHRA IV | Massive deaktiverende klager | Normal daglig aktivitet er umulig |
Diagnose
Den diagnostisering av atrieflimmer må klar
- om det faktisk er atrieflimmer,
- om komplikasjoner har oppstått eller kan forventes,
- om det er en signifikant underliggende eller samtidig sykdom,
- hvilken behandlingsstrategi som gir mening og
- om og hvilken form for antikoagulasjon ( antikoagulasjon ) som er nødvendig.
Medisinsk historie ( anamnese ) er uunnværlig for å svare på disse spørsmålene , der særlig
- forrige varighet av atrieflimmer,
- varigheten og hyppigheten av tidligere episoder,
- muligens utløsende faktorer som alkoholforbruk, søvnunderskudd eller operasjoner,
- kjente sykdommer i hjerte eller skjoldbruskkjertelen,
- de nåværende symptomene under arytmi og
- terapier eller forsøk på terapi som allerede har funnet sted
er viktige.
Diagnostisering av atrieflimmer
En uregelmessig og vanligvis for rask puls er hovedsymptomet på atrieflimmer og oppdages nesten alltid under den fysiske undersøkelsen under palpasjon og auskultasjon .
De “forkammer-bølger” ( P-bølger ) mangler i EKG , i stedet er det ofte en uregelmessig “flimmer” av grunnlinjen. Uregelmessig forekommende " ventrikulære pigger" ( QRS-komplekser ) kan noen ganger bli bedre gjenkjent enn disse fibrilleringsbølgene. Regelmessig ventrikulær handling kan også sjelden forekomme ved atrieflimmer, for eksempel med AV-blokk III °, hos noen pasienter med pacemakere eller under ventrikulær takykardi .
Paroksysmal atrieflimmer kan ofte bare diagnostiseres i langvarig EKG ( langvarig EKG, vanligvis utført over 24 timer), ved hjelp av hendelsesregistrering (over flere dager eller måneder) eller av en implantert hendelsesregistrator (over år) , som det skjer igjen og igjen i mellomtiden. Det er faser av en normal regelmessig puls (sinusrytme) med en normal EKG.
Gjenkjenne komplikasjoner og komorbiditeter
En hjertesvikt som en viktig komplikasjon av atrieflimmer er mistenkt vanligvis basert på pasientens symptomer og deretter i ultralyd i hjertet ( ekkokardiografi bekreftet). Samtidig kan hjerteventilfeil (spesielt av mitralventilen ), andre hjertefeil eller hjerteinfarkt identifiseres som mulige årsaker til atrieflimmer under ekkokardiografi . I tillegg estimeres sannsynligheten for suksess for en kardioversjon ved å estimere atriens størrelse. Den laboratorie blodprøve er nødvendig for å utelukke en overaktiv skjoldbruskkjertelen eller elektrolytt lidelser . Tromboembolisme er trolig den viktigste komplikasjonen av atrieflimmer. Dette innebærer å løsne små blodpropper fra hjertets aurikler med påfølgende blokkering av arterier (f.eks. Arterier i hjernen som resulterer i hjerneslag). Små trombedannelser i atrieflimmer kan også føre til emboliske mikroinfeksjoner i hjernen og den tilknyttede raskere kognitive nedgangen, i det minste kommer en ny prospektiv observasjonsstudie med over 5000 pasienter til denne konklusjonen.
terapi
Den terapi av atrieflimmer det vesentlige tar sikte på to kjerne problemer,
- behandling av arytmi og
- unngå emboli .
Behandling av arytmi
Når atrieflimmer først oppstår, er målet å gjenopprette og opprettholde sinusrytme. Hvis dette ikke er lovende på lang sikt, er pulskontroll (ved å bremse ventrikelfrekvensen og redusere et pulsunderskudd og behandle forverringsfaktorer ) målet.
Ny atrieflimmer har høy "selvhelbredende hastighet". Hos mer enn halvparten av pasientene slutter det spontant innen 24 timer (spontan kardioversjon) . Av denne grunn, kan behandling i løpet av denne tiden vanligvis være begrenset til å redusere pulsfrekvensen med betablokkere eller kalsiumkanalblokkere av den verapamil eller diltiazem type. Hvis frekvensreduksjonen ikke er tilstrekkelig, kan Digitalis- preparater brukes til å hemme AV-ledning . Bruk av klasse I antiarytmika er mindre vanlig . Faktorer som kan påvirkes som favoriserer atrieflimmer, elimineres så langt som mulig. Høye blodtrykksverdier, elektrolyttforstyrrelser, sirkulasjonsforstyrrelser i hjertet og en overaktiv skjoldbruskkjertel bør vurderes. Vekttap kan også forbedre atrieflimmer.
Hvis atrieflimmer vedvarer, er to forskjellige behandlingsstrategier mulig:

- Rytmekontroll: Medikament eller elektrisk kardioversjon brukes til å forsøke å gjenopprette normal sinusrytme. Hvis atrieflimmer oppstår igjen ( tilbakefall ), utføres kardioverting igjen, og antiarytmika (f.eks. Amiodaron , flekainid ) eller betablokkere blir ofte foreskrevet for å forhindre tilbakefall . Hvis forløpet er utilfredsstillende under medikamentell terapi, kan skleroterapi ( ablasjon ) av deler av hjertets indre foring (endokardium) vurderes, som enten utføres kirurgisk (sjelden utført) eller som en del av en hjertekateterprosedyre (kateterablasjon) . Enten er langsgående lesjoner plassert i området til venstre atrium, eller muskelbunter fjernes i en ring ved munnen til lungevene ( lungeveneisolasjon ). Disse prosedyrene er tidkrevende (lange intervensjonstider) og belastes av mulige komplikasjoner (spesielt tromboembolisme og lungevene stenose). De langsiktige resultatene er inkonsekvente, og det kan forventes en forbedring hos 50–80% av pasientene. Forsøk på å undertrykke forekomsten av atrieflimmer ved hjelp av hjertepacemakerbehandling er også fortsatt eksperimentelle ; hos noen pasienter med paroksysmal atrieflimmer fører spesielle stimuleringsteknikker til en signifikant reduksjon i hyppigheten av anfall.
- Hastighetskontroll: Atrieflimmer blir igjen på plass, så det gjøres ikke noe kardioversjonsforsøk. Den optimale målpulsen hos pasienter med atrieflimmer er uklar. ESC-retningslinjer anbefaler hjertefrekvens <110 slag / minutt i hvile, med mindre symptomene krever strengere hastighetskontroll. Egnede medisiner for frekvenskontroll er betablokkere, digitalis, diltiazem eller verapamil.
Siden disse strategiene har vist seg å være prognostisk tilsvarende i flere store studier , omfanget av pasientens klager (de kliniske symptomer ) er nå avgjørende kriterium for valg av terapi.
Embolisk profylakse, CHADS 2- poengsum
Hvis atrieflimmer varer lenger enn 48 timer, øker risikoen for blodpropp ( tromber ) , spesielt i venstre atrium i hjertet. Disse tromber kan løsne seg, transporteres med blodstrømmen til fjerne fartøy og forårsake akutte vaskulære okklusjoner ( embolier ) der. Det er avgjørende at syke ikke føler normofrekvent atrieflimmer, som vanligvis varer lenge, og kun konsulterer legen i en takykardisk fase. Konverteringsterapi har farene ved tromboembolisme, og derfor bør denne risikoen reduseres på forhånd ved hjelp av TEE (transesophageal echocardiography, "svelging echo") eller ved medisininhibering av blodpropp ( antikoagulasjon ) i seks uker .
Denne medisinbaserte hemming av blodpropp (antikoagulasjon, også feil referert til som "blodfortynning") blir også vurdert i tilfelle vedvarende atrieflimmer; I tillegg, etter en vellykket kardioversjon, er antikoagulasjon nødvendig i omtrent fire uker, fordi atriet kan fortsette å utvise en såkalt "bedøvelse" med redusert sammentrekning så lenge og atriale tromber kan fortsette å danne til tross for sinusrytmen.
Flertallet av pasientene får acetylsalisylsyre (ASA) eller kumariner i tablettform, i Østerrike, Tyskland og Sveits for det meste fenprocoumon . Den tidligere nødvendige veiingen av fordelene ved denne behandlingen (mindre hyppig emboli, spesielt færre slag ) med mulige ulemper (økt tendens til blødning) krever mest mulig nøyaktig kunnskap om den individuelle risikoen for emboli. Denne risikoen øker statistisk 2,5 ganger i tidligere emboli, med alderen til 1,4 ganger per tiår til 1,6 ganger hos pasienter med høyt blodtrykk , 1,5 ganger hos koronarpasienter og 1,7 ganger hos diabetikere .
Et alternativ terapi for å forebygge tromboembolisme setter den "nye orale antikoagulanter" [Noak] som den orale direkte trombininhibitor dabigatranetexilat eller orale Faktor Xa-inhibitorer rivaroksaban , Edoxaban og apixaban representerer, i motsetning til standard behandlingen med kumariner en større terapeutisk bredde inneholder og er enklere å bruke fordi koagulasjonsovervåking ikke er nødvendig. Dette er ment å redusere risikoen for blødningskomplikasjoner med samme eller bedre effektivitet. De fire nevnte stoffene ble klinisk testet i store fase III-studier. Ytterligere aktive ingredienser er for tiden i kliniske studier.
På den annen side øker risikoen for blødning bare litt med alderen. Behandlingsbeslutningen er basert på følgende felles anbefalinger fra American Heart Association (AHA), American College of Cardiology (ACC) og European Society of Cardiology (ESC) fra 2006.
| Anbefalingsklasser og bevisnivå i ACC / AHA / ESC-format | |
|---|---|
| anbefaling klasse | |
| JEG. | Bevis eller generell enighet om at anbefalingen er gunstig, nyttig og effektiv. |
| II | Motstridende bevis eller meninger om fordelen og effektiviteten med enten en overveiende positiv (klasse IIa) eller mindre veletablert (klasse IIb) vurdering. |
| III | Bevis eller generell enighet om at behandlingen ikke er nyttig, effektiv og kan være skadelig. |
| Bevisnivå (bevisnivå) | |
| EN. | Data fra flere randomiserte studier eller metaanalyser. |
| B. | Data fra en randomisert studie eller ikke-randomisert forskning. |
| C. | Ekspertuttalelse, casestudier eller etablert behandlingsstandard. |
- Med unntak av pasienter med ensom atrieflimmer (før fylte 60 år uten hjertesykdom) og de med kontraindikasjoner , anbefales antikoagulantbehandling for alle pasienter med atrieflimmer (klasse I, bevisnivå: A) .
- Type koagulasjonshemming (ASA eller antikoagulasjon) bør bestemmes individuelt for hver pasient, avhengig av risikoen for hjerneslag på den ene siden og blødning på den andre (klasse I, bevisnivå: A) .
- Pasienter med høy risiko for hjerneslag (som allerede har fått emboli eller revmatisk mitralventilstenose ) uten kunstig hjerteventil og uten kontraindikasjoner, bør få vitamin K-antagonister i en dose som fører til en INR på 2,0 til 3,0 (klasse I, nivå Bevis: A) .
- Antikoagulasjon med vitamin K-antagonister anbefales til pasienter med mer enn en "moderat" risikofaktor (alder over 74 år, høyt blodtrykk, hjertesvikt, begrenset pumpefunksjon i venstre ventrikkel med en utkastningsfraksjon på mindre enn 35% eller diabetes mellitus ) (Klasse I, Bevisnivå: A) . Hvis bare en av disse risikofaktorene er til stede, kan ASA eller en vitamin K-antagonist brukes avhengig av risikoen for blødning, påliteligheten av antikoagulasjonen og pasientens forespørsel (klasse IIa, bevisnivå: A) . Det samme gjelder pasienter med minst en av de mindre velvaliderte risikofaktorene: kranspulsår, alder over 64 år eller kvinnelig kjønn (klasse IIa, bevisnivå: B) .
- Som et alternativ til vitamin K-antagonistene anbefales ASA i en dose på 81 til 325 mg daglig for kontraindikasjoner og for pasienter med lav risiko for hjerneslag (klasse I, bevisnivå: A) .
- Under behandling med vitamin K-antagonister bør INR kontrolleres minst en gang i uken i innstillingsfasen og minst en gang i måneden hvis innstillingen er stabil (klasse I, bevisnivå: A) .
- Antikoagulasjon hos pasienter med mekaniske hjerteklaffproteser med INR på minst 2,5 er basert på protesetypen (klasse I, bevisnivå: B) .
- Det er forsvarlig å velge antikoagulantbehandling uansett hvilken type forekomst av atrieflimmer (paroksysmal, vedvarende eller permanent) (klasse IIa, bevisnivå: B) .
- Et avbrudd i antikoagulasjon i opptil syv dager uten erstatning av heparin for diagnostiske eller kirurgiske inngrep med økt blødningsrisiko er fornuftig hos pasienter uten mekanisk hjerteklaffprotese (klasse IIa, bevisnivå: C) . Hvis det er et avbrudd i mer enn en uke, kan ufraksjonert eller lavmolekylært heparin administreres, selv om effektiviteten av denne metoden er usikker i denne situasjonen (klasse IIb, bevisnivå: C) .
- Pasienter med atrieflimmer etter PTCA eller bypass-kirurgi kan få ASA (mindre enn 100 mg per dag) og klopidogrel (75 mg per dag) i tillegg til antikoagulasjon, men dette er forbundet med økt risiko for blødning og er ikke undersøkt grundig ( Klasse IIb, bevisnivå: C) . I forbindelse med PTCA kan antikoagulasjon midlertidig avbrytes, men bør fortsettes så tidlig som mulig (klasse IIb, bevisnivå: C) .
- Langvarig antikoagulasjon anbefales ikke hos pasienter under 60 år uten hjertesykdom eller andre risikofaktorer for emboli (klasse III, bevisnivå: C) .
|
CHADS 2- poengsum for å estimere risikoen for hjerneslag ved atrieflimmer | ||
|---|---|---|
| Hvis det er ... | … Overgav seg | |
| C ( hjertesvikt ) | Strukturell hjertesykdom som forårsaker hjertesvikt |
1 poeng |
| H (hypertensjon) | Arteriell hypertensjon (også behandlet) |
1 poeng |
| A (alder) | Alder ≥ 75 år | 1 poeng |
| D (diabetes) | Sukkersyke | 1 poeng |
| S (hjerneslag) | Hadde et hjerneslag eller forbigående iskemisk anfall |
2 poeng |
CHADS 2- poengsum
Den såkalte CHADS 2- poengsummen, som også anbefales i litt modifisert form i gjeldende retningslinjer fra European Society of Cardiology, er nyttig for en enkel vurdering av hjerneslagrisikoen ved atrieflimmer . Hvis poengsummen = 0, dvs. det er ingen risikofaktor for hjerneslag, oppveier risikoen for alvorlig blødning risikoen og profylakse med acetylsalisylsyre (ASA, 100–300 mg / dag) bør brukes. Med en score = 1, må individuell veiing utføres fra sak til sak (avhengig av alvorlighetsgraden og hyppigheten av atrieflimmer, alvorlighetsgraden av risikofaktorene osv.) Og med en score> 1, antikoagulasjon med kumariner bør utføres (INR 2–3).
Selv med passende behandling med kumariner er hjerneemboli ganske vanlig hos risikopasienter. Ved bruk av sensitiv magnetisk resonansavbildning kunne hjerneinfarkt oppdages hos 21% av høyrisikopasienter innen tre år, hvorav mer enn halvparten ikke forårsaket noen symptomer. En høy risiko for emboli ble funnet hos pasienter med tette spontane ekko i venstre atrium, med en langsom blodstrømningshastighet i venstre atriale vedheng, og hos de som tidligere hadde fått emboli. Av pasientene uten noen av disse egenskapene, var det bare syv prosent som fikk hjerneemboli i løpet av de tre årene.
| CHA 2 DS 2 -VASc-poengsum (videreutvikling av CHADS 2- poengsummen) | ||
|---|---|---|
| Hvis det er ... | … Overgav seg | |
| C (hjertesvikt) | Strukturell hjertesykdom som forårsaker hjertesvikt |
1 poeng |
| H (hypertensjon) | Arteriell hypertensjon (også behandlet) |
1 poeng |
| A 2 (alder) | Alder> 75 år | 2 poeng |
| D (diabetes) | Sukkersyke | 1 poeng |
| S 2 (hjerneslag) | Hadde et hjerneslag eller forbigående iskemisk anfall |
2 poeng |
| V (vaskulær sykdom) | z. B. hadde hjerteinfarkt, PAD | 1 poeng |
| A (alder) | Alder 65-74 | 1 poeng |
| Sc (sexkategori) | kvinnelig kjønn | 1 poeng |
CHA 2 DS 2 -VASc score
I noen tid, spesielt i Europa, har en modifisering av CHADS 2- poengsummen, CHA 2 DS 2 -VASc-poengsummen , blitt brukt til risikovurdering, noe som kan gi bedre risikostratifisering ved bedre å skille mennesker med lav risiko. I denne modifikasjonen tildeles flere poeng for eksisterende vaskulære sykdommer og kvinnelig kjønn. I tillegg er alderen differensiert mer presist (fra 65 år ett poeng, fra 75 år et annet poeng). Som en spesiell funksjon skal det bemerkes at kvinnelige kjønn ikke er inkludert i poengsummen som en uavhengig risiko (0 poeng) hos kvinner under 65 år uten ytterligere risikofaktorer.
Personer som oppnår minst to poeng i CHA 2 DS 2- VASc-poengsummen, bør motta oral antikoagulasjonsmedisin med kumariner. Den ekstra fordelen var kontroversiell i en studie publisert i 2010.
Antikoagulasjon og risiko for blødning
For å vurdere risikoen for hjerneblødning under antikoagulasjon presenterte European Society of Cardiology en risikoscore i 2010 , HAS-BLED-poengsummen . Den akronym "har blødd" hjelp "har blødd".
| HAS-BLED-poengsum (ESC-retningslinjer 2010) | ||
|---|---|---|
| Siffer | klinikk | Poeng |
| H | Hypertensjon (RR systolisk over 160 mmHg) | 1 |
| EN. | Alvorlig lever- / nyredysfunksjon (1 poeng hver) | 1-2 |
| S. | Historie om hjerneslag | 1 |
| B. | Enhver blødning som har funnet sted eller har en tendens til å blø | 1 |
| L. | Ustabil innstilling (<60% av INR-verdiene i målområdet) | 1 |
| E. | Alder over 65 år | 1 |
| D. | Narkotika som NSAID eller alkoholmisbruk | 1-2 |
Fra en score = 3 er en relevant risiko for blødning som krever spesiell forsiktighet ved forskrivning av antikoagulantia.
Risikofaktorene for blødning overlapper f.eks. T. med de for emboli (hypertensjon, tidligere hjerneslag, alder). Pasienter med høy HAS-BLED-score i. d. Vanligvis også med høy risiko for hjerneslag. Derfor bør en høyere HAS-BLED-score ikke forstås som en absolutt kontraindikasjon for antikoagulasjon, men v. en. Også som en indikasjon for å optimalisere kontrollerbare risikofaktorer (ustabil INR-innstilling, samtidig medisinering).
Kirurgisk embolisk profylakse
Hos pasienter med økt risiko for blødning (HAS-BLED score> 3) eller kontraindikasjon mot antikoagulantia, er det mulig å minimere risikoen for emboli ved å okkludere venstre atriale vedheng, som er en typisk kilde til emboli. For dette formålet føres et atrialt implantat ( paraply ) frem til venstre atrium ved hjelp av et kateter gjennom punkteringen i en stor vene ved å gjennombore atrialseptumet . Der brettes implantatet ut og plasseres direkte ved tilgangen til atrialt vedheng. I de følgende månedene vokser atrialsparaplyen inn og dekkes fullstendig av hjertets indre foring . Atrialt vedheng er dermed permanent lukket, det kan ikke lenger dannes blodpropp der. I stedet for å ta et antikoagulant, er det langvarig å ta hemmer av blodplateaggregering . Tidligere studier har vist at embolisk profylakse ikke er dårligere enn oral antikoagulasjon. En studie publisert i 2009 presenterte en betydelig risiko for denne prosedyren. Hver 20. pasient utviklet perikardial effusjon , hver 50. pasient krevde åpen hjerteoperasjon og 1% av pasientene fikk hjerneslag forårsaket av luftemboli eller blodpropp.
Minimalt invasiv ablasjon av kateter
Kateterablasjon blir vurdert oftere og oftere . Ved hjelp av et spesielt kateter plasseres et arr i hjerteveggen via inguinalvenene for å stoppe de elektriske impulsene som utløser atrieflimmer. Arret påføres hovedsakelig hjertet av varme, men det er nå også prosedyrer som fungerer med kulde eller laser. Ablasjon gir gode resultater, spesielt hos pasienter med paroksysmal atrieflimmer. I noen tilfeller må imidlertid ablasjonen utføres flere ganger. Ablasjon er også et alternativ hos unge mennesker for å unngå livslang medisinering assosiert med bivirkninger. Denne minimalt invasive prosedyren har relativt lav risiko, men av og til oppstår mer alvorlige komplikasjoner som perikardial tamponade eller lungeemboli .
Permanent frihet fra sykdom er ikke garantert selv etter ablasjon av kateteret.
Den økende tendensen til å utføre slike inngrep møtte også kritikk fra noen medisinske spesialister. I en gjennomgangsartikkel i legemiddelbrevet fra november 2014 kom et team av forfattere til den personlige konklusjonen at man bare bør kateterablasjon hos sterkt symptomatiske pasienter hvis symptomer ikke kan lindres i tilstrekkelig grad med antiarytmika i klasse I og klasse III, vurderer. Bare ønske fra pasienten om ikke å ta mer medisiner ville ikke være en grunn til å utføre en ablasjon. Risikoen ved prosedyren bør også tydelig påpekes. Bokstavelig talt sto det: "Representasjoner om at ablasjonen er en ukomplisert rutineprosedyre med høy suksessrate er uholdbar."
Imidlertid er det flere og nyere studier som beviser overlegenhet med kateterablasjon sammenlignet med legemiddelrytmekontroll i kliniske studier , slik at det allerede er snakk om et paradigmeskifte fra medikamentell behandling til kateterablasjon. Dette kan nå bli vist i en multisenterstudie ( "CASTLE-AF") i 363 pasienter med atrial fibrillering og hjertesvikt fra NYHA II og mer, hvor, etter en median oppfølging av 38 måneder, 28,5% av pasientene i motsetning kateterablasjon 44,6% av de medikamentbehandlede pasientene hadde dødd eller måtte innlegges på grunn av hjertesvikt (hazard ratio HR = 0,62), med død hos 13,4% versus 25,0% (HR = 0,56), men bare til tross for kateterablasjon 63% av pasientene hadde sinusrytme etter 60 måneder (mot 22% i legemiddelgruppen). Det var syv alvorlige, ikke-dødelige komplikasjoner (4%) under kateterablasjon, inkludert tre blødninger som krever transfusjon , tre perikardiale effusjoner (med en perikardiell punktering ) og en asymptomatisk lungevene-stenose.
Spesielle situasjoner
Perioperativ atrieflimmer
Spesielt etter operasjoner på hjertet er atrieflimmer en vanlig komplikasjon . Det oppstår, avhengig av prosedyren som er utført og tidligere skade på hjertet, med en frekvens på 10–77%, vanligvis den andre dagen etter operasjonen. Det er mer vanlig for inngrep på mitralventilen (opptil 73%) enn for bypassoperasjoner (10–33%) Andre risikofaktorer inkluderer alderdom, forstørret venstre atrium , lange operasjonstider, høyt blodtrykk og tidligere atrieflimmer. Den prognose for perioperativ atrieflimmer er god: sinusrytmen kan gjenopprettes på omtrent 90% av pasientene og en svekkelse av sannsynligheten for overlevelse kunne ikke fastslås. Kalium- og magnesiuminfusjoner samt betablokkere og andre antiarytmika brukes for å unngå perioperativ atrieflimmer .
Atrieflimmer og sentralstimulerende midler - Holiday Heart Syndrome
Hos noen mennesker, inkludert de med sunne hjerter, kan atrieflimmer provoseres av alkohol . I noen studier hadde mer enn halvparten av tilfellene av paroksysmal atrieflimmer skjedd etter alkoholforbruk. Vanligvis begynner arytmi noen timer etter inntak av en uvanlig høy dose alkohol, ofte i andre halvdel av natten, i helgen eller etter fysisk anstrengelse. For denne konstellasjonen, spesielt observert hos yngre menn, ble begrepet "Holiday Heart Syndrome" opprettet basert på en publikasjon fra 1983 . Hos nesten alle pasienter slutter arytmien innen 24 timer uten spesiell behandling. I den danske diettkreft- og helsestudien som ble publisert i 2004, ble det funnet at menn med et alkoholforbruk på mer enn 20 g per dag hadde en 44% økt risiko for atrieflimmer. Menn som drakk 12 g eller mindre per dag, som kvinner, hadde normal risiko. I en kontrollert studie fra Australia ble det også vist at gjentakelse av atrieflimmer hos pasienter som regelmessig konsumerte alkohol, kan reduseres ved i stor grad å avstå fra alkohol. Legemiddelbrevet anbefaler derfor avholdenhet fra alkohol i tilfelle paroksysmal atrieflimmer. Dette er mer tålelig enn å øke dosen av antiarytmika eller komplekse ablasjonsprosedyrer.
Forbruket av kaffe eller te , som tidligere ble sett på som en risiko , viste seg derimot å være ufarlig i den samme studien i forbindelse med atrieflimmer. Med regelmessig forbruk skjedde det til og med litt sjeldnere.
Utsiktene til helbredelse
Den dødelighet ved atrieflimmer er omtrent dobbelt så høy som i mennesker av samme alder med en normal hjerterytme, som hovedsakelig eller utelukkende på grunn av de mer hyppige hjertesykdommer. I gjennomsnitt lider rundt seks prosent av pasientene med atrieflimmer et hjerneslag hvert år, og 15-20% av alle hjerneslag oppstår med atrieflimmer.
I 2006 forventes omtrent 2,5 millioner amerikanere og 4,5 millioner EU- borgere å ha atrieflimmer. Kostnadene forårsaket av atrieflimmer er estimert til EUR 13,5 milliarder årlig for EU-landene. Antall sykehusinnleggelser for atrieflimmer økte med 66% fra 1996 til 2006.
Forekomst hos dyr
For hund og katt Oppstår atrieflimmer ved frekvenser opptil 700 slag per minutt. Selv om det kan sees regelmessig hos hunder, blir katter sjelden påvirket.
hund
Hos hunder blir medlemmer av store raser oftest berørt, med den resulterende hjerterytmefrekvensen på over 230 slag i minuttet. Forklaringen på opprinnelsen kan sees i prinsippet i de samme mekanismene som forklart ovenfor. I tillegg kommer teorien om den “kritiske massen” av hjertet. Små raser med tilsvarende små hjerter har langt mindre sannsynlighet for å utvikle atrieflimmer enn større hunder. Atrieflimmer kan forekomme i noen gigantiske raser uten en påvisbar underliggende sykdom. Vanligvis er det imidlertid sekundært til en utvidelse av hjertets forkamre. Tøyning av atriale vegger kan ha innflytelse her. Den "elektriske ombyggingen" som allerede er nevnt ovenfor ser ut til å være uttalt hos hunder, da atrieflimmer en gang ikke lenger kan elimineres hos mange dyr.
Den vanligste atrieflimmer forekommer som en sekundær forekomst hos hunder med den underliggende sykdommen utvidet kardiomyopati . Andre mulige utløsere er sykdommer med kronisk volumoverbelastning i hjertet ( mitralventilregurgitasjon , uløst vedvarende ductus arteriosus ). Idiopatisk atrieflimmer ses relativt sjelden . Hjertesykdom eller høyt blodtrykk forekommer sjelden hos hunder i motsetning til mennesker og er derfor ubetydelige som årsaker.
Målet med behandlingen er å redusere hjertefrekvensen til 100–140 per minutt i hvile. I tillegg til å behandle den underliggende sykdommen, som i tilfelle utvidet kardiomyopati er den vanligste utløseren ved administrering av pimobendan til hunder, blir medisiner som digitalis , atenolol eller diltiazem administrert til hunder og katter for å redusere hjertefrekvensen. Embolismeprofylakse er ikke nødvendig hos hunder.
katt
Hos katter finnes atrieflimmer mye sjeldnere, igjen hovedsakelig som et resultat av overdreven utvidelse av atriene, som hovedsakelig skyldes kardiomyopati (for det meste hypertrofisk, sjeldnere restriktiv, svært sjelden utvidet). Den resulterende pulsen kan nå 320 per minutt. Legemidlene beskrevet ovenfor brukes terapeutisk. I tillegg er embolismeprofylakse (vanligvis med acetylsalisylsyre ) helt nødvendig for å unngå høy risiko for emboli hos katter i enden av aortagrenen (såkalt ridende aorta-trombe , → iskemisk myopati hos katter ), nyrekarene , de mesenteriske karene ( arteria mesenterica cranialis ) eller den nedre kragebenarterien og kaudalarterien for å unngå.
litteratur
- AJ Camm et al.: 2012 fokusert oppdatering av ESC-retningslinjene for håndtering av atrieflimmer: En oppdatering av ESC-retningslinjene for 2010 for behandling av atrieflimmer * Utviklet med det spesielle bidraget fra European Heart Rhythm Association. I: European Heart Journal . Volum 33, nr. 21, november 2012, s. 2719-2747, ISSN 1522-9645 . doi: 10.1093 / eurheartj / ehs253 . PMID 22922413 .
- Hans-Joachim Trappe: Atrieflimmer - det etablerte og det nye . I: Deutsches Ärzteblatt International . teip 109 , nr. 1-2 , 2012, s. 1–7 ( gjennomgangsartikkel ).
- A. Schuchert et al.: Kommentar til ACC / AHA / ESC-retningslinjene 2001 om forebygging av arteriell tromboembolisme hos pasienter med atrieflimmer. I: Journal of Cardiology. Volum 92, utgave 7, april 2003, s. 694-703, doi: 10.1007 / s00392-003-0992-6 ( fulltekst som PDF ).
- E. Hoffmann, S. Janko, C. Reithmann, G. Steinbeck: Utløsermekanismer for atrieflimmer . I: Journal of Cardiology. Volum 91, utgave 1, januar 2002, s. 24-32, doi: 10.1007 / s392-002-8368-6 .
- Philip R. Fox, David Sisson, Sydney N. Moïse et al: Textbook of Canine and Feline Cardiology. 2. utgave. Saunders, Philadelphia et al. 1999, ISBN 0-7216-4044-3 , s. 331-391.
- Wilhelm Haverkamp: Atrieflimmer oppdatert: diagnose / terapi / behandling av spesielle tilfeller . close2real Verlag, Berlin 2018, ISBN 978-3-00-058868-6 .
weblenker
- Kompetansenettverk atrieflimmer - Nasjonal forening av internister, kardiologer og hjertekirurger for utvikling av nye metoder for diagnostisering og behandling av atrieflimmer
- CHA 2 DS 2 -VASc score kalkulator
Individuelle bevis
- ↑ Mewis, Riessen, Spyridopoulos (red.): Kardiologie compact - Alt for avdeling og spesialistundersøkelse . 2. utgave. Thieme, Stuttgart / New York 2006, ISBN 3-13-130742-0 , s. 532, 535, 536 .
- ↑ Alan John Camm et al.: 2012 fokusert oppdatering av ESC-retningslinjene for håndtering av atrieflimmer: En oppdatering av ESC-retningslinjene for 2010 for håndtering av atrieflimmer * Utviklet med det spesielle bidraget fra European Heart Rhythm Association. I: European Heart Journal . Volum 33, nr. 21, november 2012, s. 2719-2747, ISSN 1522-9645 . doi: 10.1093 / eurheartj / ehs253 . PMID 22922413 . (Engelsk)
- ↑ a b c d A. John Camm, et al.: Retningslinjer for behandling av atrieflimmer . I: European Heart Journal . teip 31. 2010, s. 2369–2429 , doi : 10.1093 / eurheartj / ehq278 ( online [PDF]). Retningslinjer for behandling av atrieflimmer ( Minne til originalen datert 17. november 2011 i Internet Archive ) Info: Arkivlenken ble satt inn automatisk og har ennå ikke blitt sjekket. Vennligst sjekk originalen og arkivlenken i henhold til instruksjonene, og fjern deretter denne meldingen.
- ↑ Harald Feldmann, Tilman Brusis: Uttalelse fra øre, nese og hals lege . Thieme, 2012, ISBN 978-3-13-160047-9 ( google.com [åpnet 31. mai 2016]).
- ^ A. Voskoboinik et al.: Alcohol and Atrial Fibrillation: A Sobering Review . I: Journal of the American College of Cardiology . teip 68 , nr. 23. 2016, s. 2567 ( sciencedirect.com ).
- ↑ Søvnapné atrieflimmer - OSAS-behandling kan hjelpe. I: SeegartenKlinik Heidelberg. 4. februar 2020, åpnet 11. mai 2020 (tysk).
- ↑ U. Schotten et al.: Atrieflimmer: Grunnleggende forskning gir nye terapeutiske tilnærminger. I: Deutsches Ärzteblatt . 2006, bind 103, s. B1491-B1497.
- ↑ Herbert Reindell , Helmut Klepzig: Sykdommer i hjertet og karene. I: Ludwig Heilmeyer (red.): Lærebok for indremedisin. Springer-Verlag, Berlin / Göttingen / Heidelberg 1955; 2. utgave ibid. 1961, s. 578-580 ( Hypertensjonen i stor og liten opplag ).
- ↑ a b P Kirchhoff, et al.: Kommentar til retningslinjene til ESC om atrieflimmer . I: Kardiologen . Bind 6, februar 2012, s. 12-27. doi : 10.1007 / s12181-011-0395-2 .
- ^ EL Thacker, B. .. McKnight, BM Psaty et al.: Atrieflimmer og kognitiv tilbakegang: En langsgående kohortestudie. I: Nevrologi. S., doi: 10.1212 / WNL.0b013e31829a33d1 .
- ↑ Anne Paschen: Hjerte. I: Jörg Braun, Roland Preuss (red.): Clinic Guide Intensive Care Medicine. 9. utgave. Elsevier, München 2016, ISBN 978-3-437-23763-8 , s. 185–283, her: s. 230 ( frekvensregulering ).
- ↑ Hany S. Abed, Gary A. Wittert et al. Effekt av vektreduksjon og kardio risikofaktor ledelse på Symptom Burden og alvorlig hos pasienter med atrieflimmer. I: JAMA. Volum 310, 2013, s. 2050, doi: 10.1001 / jama.2013.280521 .
- ↑ ESC Pocket Guideline: Håndtering av atrieflimmer. Versjon 2016.
- ↑ Stuart J. Connolly et al.: Dabigatran versus warfarin hos pasienter med atrieflimmer. I: The New England journal of medicine . Volum 361, nr. 12, september 2009, s. 1139-1151, ISSN 1533-4406 . doi: 10.1056 / NEJMoa0905561 . PMID 19717844 .
- ↑ Manesh R. Patel et al. Rivaroxaban versus Warfarin i Nonvalvular atrieflimmer. I: The New England Journal of Medicine . Volum 365, nr. 10, september 2011, s. 883-891, ISSN 1533-4406 . doi: 10.1056 / NEJMoa1009638 . PMID 21830957 .
- ↑ CB Granger et al.: Apixaban versus warfarin hos pasienter med atrieflimmer. I: The New England Journal of Medicine . Volum 365, nummer 11, september 2011, s. 981-992, ISSN 1533-4406 . doi: 10.1056 / NEJMoa1107039 . PMID 21870978 .
- ^ A b V. Fuster et al.: ACC / AHA / ESC 2006 retningslinjer for behandling av pasienter med atrieflimmer: en rapport fra American College of Cardiology / American Heart Association Task Force on Practice Guidelines og European Society of Cardiology Committee for praksisretningslinjer (skrivekomité for å revidere retningslinjene for 2001 for behandling av pasienter med atrieflimmer). I: Journal of the American College of Cardiology . 2006, bind 48, artikkel: e149-246, PMID 16904533 .
- ↑ a b American College of Cardiology; American Heart Association Task Force; European Society of Cardiology Committee for Practice Guidelines; European Heart Rhythm Association; Heart Rhythm Society et al.: ACC / AHA / ESC 2006 retningslinjer for behandling av pasienter med atrieflimmer: en rapport fra American College of Cardiology / American Heart Association Task Force om retningslinjer for praksis og European Society of Cardiology Committee for Practice Guidelines (Skrivekomité for å revidere retningslinjene for 2001 for behandling av pasienter med atrieflimmer) utviklet i samarbeid med European Heart Rhythm Association og Heart Rhythm Society. I: Europace. Volum 8, nr. 9, september 2006, s. 651-745, ISSN 1099-5129 . doi: 10.1093 / europace / eul097 . PMID 16987906 .
- Bern P. Bernhardt, H. Schmidt, T. Sommer, B. Lüderitz, H. Omran: Atrieflimmer - pasienter med høy risiko for hjerneemboli. I: Klinisk forskning i kardiologi. Volum 95, nr. 3, mars 2006, s. 148-153, ISSN 1861-0684 . doi: 10.1007 / s00392-006-0344-4 . PMID 16598527 .
- ↑ Lip GYH: Forbedring av slag og tromboembolisme risiko lagdeling i kronisk hjerteflimmer . I: E-Journal of the ESC Council for Cardiology Practice. Volum 8, nr. 36, 9. juni 2010.
- ↑ Laurent Azoulay, Teresa Simon, Sophie Dell'Aniello, Christel Renoux, Samy Suissa Sammendrag 18044: Sammenligning av CHADS 2 og CHA 2 DS 2 -VASc-poengene i forutsigelse av hjerneslaghendelser hos pasienter med atrieflimmer. I: Sirkulasjon. Volum 122, artikkel: A18044 / 2010.
- ↑ F. Meincke, K.-H. Kuck, MW Bergmann: Intervensjonell atriell vedleggslukking. Alternativ til antikoagulasjon ved hjerneslagprofylakse for atrieflimmer. I: hjerte. Nr. 38, 2013 ISSN 0340-9937 , s. 239-246
- ↑ Perkutan lukking av venstre atriale vedlegg versus warfarinbehandling for forebygging av hjerneslag hos pasienter med atrieflimmer: en randomisert ikke-underlegenhetsstudie, abstrakt. I: The. August 2009, åpnet 28. februar 2014.
- ↑ Kateterablasjon - Kompetisjonsnett for atriefibrillering . Nettsted for nettverkshovedkvarteret ved Münster universitetssykehus. Hentet 29. august 2014.
- ↑ Atrial ablasjon for atrieflimmer. I: Medisinbrevet . November 2014, åpnet 27. april 2017 (bind 48, nr. 11, november 2014).
- ↑ Mark S. Link: paradigmeskifte for behandling av atrieflimmer i hjertesvikt. I: New England Journal of Medicine . 2018, bind 378, utgave 5, 1. februar 2018, s. 468–469, DOI: 10.1056 / NEJMe1714782 .
- ↑ Nassir F. Marrouche, Johannes Brachmann , Dietrich Andresen, Jürgen Siebels, Lucas Boersma, Luc Jordaens, Béla Merkely, Evgeny Pokushalov, Prashanthan Sanders, Jochen Proff, Heribert Schunkert, MD, Hildegard Kristus, Jürgen Vogt, Dietmar Bänsch for CASTLE AF Forsker: Kateterablasjon for atrieflimmer med hjertesvikt. I: New England Journal of Medicine . 2018, bind 378, utgave 5. februar 201, s. 417-427, DOI: 10.1056 / NEJMoa1707855 .
- ^ Voskoboinik A et al.: Alcohol Abstinence in Drinkers with Atrial Fibrillation . I: New England Journal of Medicine . teip 382 , 2020, s. 20-28 .
- ↑ Færre gjentakelser av atrieflimmer med mindre alkoholforbruk? I: Ludwig WD, Schuler J (red.): Legemiddelbrevet . teip 54 , 2020, s. 11 .