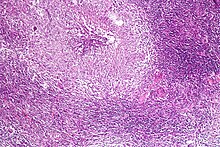
tuberkulose
| Klassifisering i henhold til ICD-10 | |
|---|---|
| A15 | Tuberkulose i luftveiene, bakteriologisk eller histologisk bekreftet |
| A16 | Tuberkulose i luftveiene, verken bakteriologisk eller histologisk bekreftet |
| A17 | Tuberkulose i nervesystemet |
| A18 | Tuberkulose i andre organer |
| A19 | Miliær tuberkulose |
| ICD-10 online (WHO versjon 2019) | |
Den Tuberkulose (forkortet TB eller TB , så kalt fra Würzburg klinikere Johann Lukas Schönlein på grunn av den karakteristiske histopatologiske bilde av latin tuberkulose , fra latin tuberkel , liten tumor ') er en multi bakterielle infeksjonssykdommer . Sykdommen er forårsaket av ulike typer mykobakterier ( Mycobacterium tuberculosis complex ), og som lungetuberkulose påvirker det ofte lungene hos mennesker . Hvis det er en immundefekt , påvirker det også i økende grad lungene.
Tuberkulose, som rammer rundt 10 millioner mennesker over hele verden hvert år, fører den globale statistikken over dødelige smittsomme sykdommer. I følge Verdens helseorganisasjon (WHO) Global tuberculosis report , døde rundt 1,4 millioner mennesker av tuberkulose i 2015. I tillegg var det 400 000 dødsfall fra flere HIV- smittede. Tuberkulose er oftest forårsaket (i det minste nå i Tyskland) av Mycobacterium tuberculosis , sjeldnere - i synkende rekkefølge - av Mycobacterium bovis , Mycobacterium africanum eller Mycobacterium microti .
Beskrivelsen av patogenet Mycobacterium tuberculosis av Robert Koch i 1882 var en milepæl i medisinsk historie. Tuberkulose kalles derfor også Kochs sykdom . Navnene tuberkulose ( phthisis eller phthisis ) eller på folkemunne møll , hvite pest og Hvit død er utdatert, samt vilkårene Lungendärre , Darre og Dorre .
Bare rundt fem til ti prosent av de som er smittet med Mycobacterium tuberculosis blir faktisk syke i løpet av livet; mennesker med svekket immunforsvar eller genetisk mottakelighet er spesielt berørt . Overføringen skjer vanligvis gjennom dråpeinfeksjon av syke mennesker i nærheten. Hvis bakterier kan påvises i sputumet , snakker man om åpen tuberkulose. Hvis bakterier oppdages i andre eksterne kroppssekresjoner, blir det referert til som potensielt åpen tuberkulose. Hosting skaper en smittsom aerosol som mister smitteevnen gjennom sedimentering, ventilasjon og naturlige UV-lyskilder. Siden storfe også kan utvikle tuberkulose, pleide ( upasteurisert ) rå melk å være en utbredt infeksjonskilde i Vest-Europa og er fremdeles en vanlig smittekilde i deler av verden. Fordi det kan overføres fra dyr til mennesker, er tuberkulose en zoonose . Omvendt er overføring fra mennesker til dyr et viktig aspekt ved bevaring av sjeldne primater.
Bare med direkte påvisning av patogenet eller dets genetiske materiale blir sykdommen bekreftet av laboratoriediagnostikk. Indirekte, d. H. Immunologiske funn eller hudtester bidrar bare til diagnosen, da de ikke kan skille mellom en sykdom og en infeksjon som har funnet sted. De kan også vise seg å være falske negative hvis immunforsvaret har kollapset.
Forskjellige antibiotika er tilgjengelige for behandling , som er spesielt effektive mot mykobakterier og kalles derfor også antituberkulotika . For å unngå utvikling av motstand og tilbakefall, må disse tas i kombinasjon og i samsvar med WHOs retningslinjer i minst seks måneder, dvs. langt utover symptomene. Det er vaksinasjon, men det har ikke blitt anbefalt i Tyskland siden 1998 på grunn av utilstrekkelig effektivitet og er ikke lenger tilgjengelig. En primær profylakse med et antituberkulös effektivt medikament anbefales i Tyskland, hovedsakelig hos barn eller alvorlig immunkompromitterte kontakter. Hos voksne som har et intakt immunsystem (og derfor blir referert til som immunkompetent ), derimot, finner sekundær profylakse eller forebygging først sted etter at infeksjon er bestemt ved hjelp av forebyggende administrering av antituberkuløse medikamenter, med tanke på motstandssituasjon. Tuberkulose er underlagt registrering ved navn i EU og det meste av verden .
Epidemiologi og relevans for helsepolitikken
Verdensomspennende
Omtrent en tredjedel av verdens befolkning er smittet med tuberkulosepatogener. Imidlertid fører bare en liten andel av infeksjonene til sykdom. I følge WHOs globale tuberkuloserapport 2016 var det 10,4 millioner nye infeksjoner og 1,8 millioner dødsfall over hele verden i 2015. Begge tallene har falt jevnt og trutt siden 1990.
Behandlingsmulighetene er ofte utilstrekkelige fordi det krever dyre antibiotika, tar lang tid og ofte er umulig å ta i betraktning de sosiale forholdene til de berørte. Laboratorier for diagnose og behandling mangler ofte i berørte regioner. Spesielt i Øst-Europa har det vært en bekymringsfull økning i tuberkulose på grunn av fattigdom og mangler i helsesystemet , særlig med multiresistente patogenstammer. Sykdommen er også oftere og oftere forårsaket av slike medikamentresistente tuberkulosestammer rundt om i verden.
En tuberkuloseinfeksjon er spesielt problematisk hos HIV- infiserte personer med manifest AIDS . På grunn av immunmangel , øker HIV sannsynligheten for et utbrudd av tuberkulose mange ganger. Sammen med aids er tuberkulose den viktigste dødsårsaken i Afrika. Begge sykdommene forekommer i nær sammenheng med hverandre, spesielt hos innbyggere i storbyområder. Immunmangel forårsaket av HIV fører ofte til negative resultater i rutinemessige tuberkuloseundersøkelser, selv om sykdommen er til stede (se også feil 1 og 2 ). Dette er fordi hudtestene ( tuberkulintest , tintest) kontrollerer den immunologiske reaksjonen på patogenkomponenter, men dette hemmes av AIDS. Forløpet av tuberkulose akselereres da betydelig. I fattige land er TB et tegn på AIDS-utbruddet og dreper de fleste mennesker med HIV. Den WHO ber derfor for og fremmer global koordinering av tuberkulose og AIDS-forskning.
Overraskende fant en italiensk studie en forekomst (sykdomsfrekvens) av latente tuberkuloseinfeksjoner på ni prosent blant sunne ansatte i helsesektoren og 18 prosent blant godt 400 personer med psoriasis . 30 prosent av de med lungebetennelse og lungekreft var også latent smittet.
Tyskland, Østerrike og Sveits
I 2016 ble 5915 tuberkuloselidende rapportert til Robert Koch Institute (RKI) i Tyskland, inkludert 233 barn under 15 år (2005: 230). I 2016 var det 7,2 sykdommer per 100.000 innbyggere i Tyskland. Den offisielle statistikken indikerte 100 dødsfall for 2015. Dataene burde ikke helt svare til de reelle tallene, ettersom antallet ikke rapporterte tilfeller for denne sykdommen er relativt høyt på grunn av dens uspesifikke symptomer. Ifølge en patologistudie fra Tyskland ble diagnosen bare en tredjedel av tuberkulose diagnostisert etter mortem diagnostisert i løpet av livet.
I Tyskland er sykdommen spesielt utbredt i Hamburg , Bremen og Berlin . Når det gjelder syke mennesker født i landet, dominerer de eldre aldersgruppene på grunn av tilbøyeligheten til å aktivere og reaktivere som et resultat av det reduserte immunforsvaret. Middelaldersgruppene dominerer blant migrantene, ettersom det er mer sannsynlig at ferske infeksjoner utløser sykdommen. Den foreløpige statistikken for tuberkulose for 2017 viser et platå i Tyskland på nivå med 2016 etter at en økning i tuberkulosesykdommer på grunn av økt innvandring ble registrert høsten 2015. I Sveits og Østerrike gikk også antall saker ned noe frem til 2017. Den fryktede større økningen i antall saker på grunn av bølgen av migranter i 2017 har derfor ennå ikke skjedd.
I 2015 ble 583 sykdommer påvist med tuberkulose, Sveits i 546 sykdommer i Østerrike .
Tabellen nedenfor viser antall nye tilfeller per 100.000 innbyggere ( forekomst ) og antall nye tilfeller per år i Tyskland (D), Sveits (CH) og Østerrike (A).
| år | Forekomst D |
Rapporterte saker (nye saker) D | Forekomst CH |
Rapporterte saker (nye saker) CH | Forekomst A |
Rapporterte saker (nye saker) A | Forekomst DDR |
|---|---|---|---|---|---|---|---|
| 1940 | 156,8 | 109.508 (rikets territorium) | omtrent 100 | 3.127 | bare tall for rikets territorium | ||
| 1950 | 277 | 137,721 (bare Tyskland) | 68.1 | ca. 8200 | omtrent 500 | ||
| 1960 | 126,6 | 70 325 (bare Tyskland) | omtrent 40 | ca. 4600 | ca. 210 | ||
| 1970 | 79.3 | 48262 (bare Tyskland) | ca. 25 | 2850 * | omtrent 80 | ||
| 1980 | 42.1 | 27845 (bare Tyskland) | ca. 20 | 1.396 | 2191 * | ||
| 1990 | 19.6 | 12184 (bare Tyskland) | 18.4 | 1.278 | 20.4 | 1.521 * | |
| 2000 | 11.0 | 9,064 | 8.7 | 629 | 15.3 | 1.226 | |
| 2006 | 6.5 | 5,402 | 6.9 | 520 | 10.8 | 894 | |
| 2007 | 6.1 | 5.020 | 6.3 | 478 | 10.7 | 891 | |
| 2008 | 5.5 | 4,543 | 6.7 | 520 | 9.9 | 817 | |
| 2009 | 5.4 | 4444 | 7.1 | 556 | 8.4 | 697 | |
| 2010 | 5.4 | 4.388 | 6.9 | 548 | 8.2 | 688 | |
| 2011 | 5.3 | 4.317 | 7.1 | 577 | 8.2 | 687 | |
| 2012 | 5.2 | 4.220 | 5.7 | 463 | 7.7 | 648 | |
| 2013 | 5.3 | 4,318 | 6.5 | 526 | 7.7 | 649 | |
| 2014 | 5.6 | 4,488 | 5.7 | 473 | 6.8 | 582 | |
| 2015 | 7.3 | 5865 | 6.4 | 546 | 6.7 | 583 | |
| 2016 | 7.2 | 5915 | 7.2 | 611 | 7.2 | 634 | |
| 2017 | 6,7 ** | 5476 ** | 6,3 ** | 536 ** | 6,5 ** | 569 ** | |
| 2018 | 6.5 | 5.513 | |||||
| 2019 | 4,735 |
* smittsom bare ** foreløpige tall
Tuberkulosepatogen
Hovedårsaken til tuberkulose, Mycobacterium tuberculosis, er en aerob gram-positiv stavformet bakterie som deler seg hver 16. til 20. time. Sammenlignet med andre bakterier som har delingshastigheter i størrelsesorden minutter, er dette ekstremt tregt. Den mikroskopiske påvisningen er mulig med de typiske fargestoffegenskapene: Bakterien beholder fargen etter behandling med en sur løsning og blir derfor referert til som en syrebestandig stang. I den vanligste fargingen av denne typen, Ziehl-Neelsen-fargestoffet , skiller de rødfargede bakteriene seg ut mot en blå bakgrunn. Deteksjonen er fremdeles mulig ved fluorescensmikroskopi og ved auramin-rodamin-farging . Mykobakterier er knapt synlige i Gram-flekken, men strukturen til peptidoglykanen er veldig lik den for gram-positive bakterier, slik at M. tuberculosis formelt er klassifisert som gram-positiv. Dette ble bekreftet ved sekvensanalyser av RNA .
Andre mykobakterier , som også regnes som patogener for tuberkulose, tilhører samme gruppe bakterier : M. bovis , M. africanum og M. microti . Disse patogenene finnes bare sporadisk i tuberkuløse sykdommer i Tyskland. M. kansasii og M. avium kan i sjeldne tilfeller, i likhet med en rekke andre mykobakterier, forårsake tuberkulose-lignende kliniske bilder. Imidlertid er det generelt ingen risiko for infeksjon fra atypiske mykobakterier ( andre mykobakterier enn tuberkulose, MOTT ).
M. tuberculosis, M. bovis, M. africanum, M. microti, M. canetti , M. pinnipedi , M. caprae og vaksinestammen Bacillus Calmette-Guérin (BCG) er oppsummert som Mycobacterium tuberculosis complex.
Overføringsruter
Innånding av smittsomme dråper ( aerosoler ) er den vanligste og derfor den viktigste overføringsveien: I dette tilfellet er innånding av noen få mikrodråper (2–5 µm i diameter), som hver inneholder 1-3 patogener, tilstrekkelig for en infeksjon . Overføring via blodet, organtransplantasjoner eller andre kroppssekreter er langt mindre vanlig. I prinsippet er noen av følgende overføringsveier mulige og beskrevet som sikre i litteraturen:
- aerogen , dvs. via mikrodropper i luften som inneholder patogenet Mycobacterium tuberculosis , med inngangsportene alveoler , åpne sår, friske tatoveringer og slimhinner
- gastral ved inntak av mykobakterienhaltiger matvarer (melk, rå kjøtt osv.)
- parenteralt ved hjelp av diagnostiske og terapeutiske instrumenter forurenset med blod og sekreter (transfusjoner, sprøyter, nåler, skalpeller, lansetter, biopsinåler, endoskoper, etc.)
- Transplantatrelatert gjennom heterogene transplantater av infisert vev (nyrer osv.)
- seksuell (bare hvis kjønnsorganer påvirkes)
- gjennom smøreinfeksjoner på den ikke-intakte huden (sprekker, eksem eller skader)
- intrauterin for infeksjoner i livmoren
- sub partu (under fødsel) som et resultat av urogenital tuberkulose hos moren
Infeksjonen av kakerlakker og avføringen med Mycobacterium tuberculosis er gjentatte ganger bevist . Dette faktum siteres regelmessig av skadedyrbekjempere. En gjennomgang av litteraturen avslørte ikke en eneste bekreftet overføringssak.
Ekskretorisk tuberkulose er et medisinsk begrep som ikke lenger brukes for de former for tuberkulose der patogener spres gjennom ekskresjonsorganene i kroppen og fører til en sekundær angrep av andre organer.
De luftbårne infeksjonene stammer vanligvis fra voksne, siden mengden bakterier som skilles ut hos barn er for liten, selv med åpen lungetuberkulose (paucibacillary = low-pathogen tuberculosis). Organinvolvering utenfor lungene, med unntak av svært smittsom laryngeal tuberkulose (laryngeal tuberculosis), utgjør bare en risiko for infeksjon hvis infeksjonsfokusene er forbundet med utsiden av kroppen via naturlige ruter (mage-tarmkanalen) eller fisteldannelse, eller hvis nålestikkskader eller kontakt oppstår under diagnostiske punkteringer / inngrep, kommer til sår. En historisk signifikant, nå nesten glemt spesiell form, er lik tuberkler (engelske prosectorsvorte), der anatomister, patologer, slaktere osv. Smittes igjen gjennom håndsår. Infeksjon fra smittet melk er også mulig. Imidlertid har slike infeksjoner blitt svært sjeldne i industrialiserte land, der storfeflokker i stor grad er tuberkulosefrie og melken pasteurisert. Nyfødte fra mødre med lungetuberkulose blir sjelden smittet gjennom blodet. Imidlertid, hvis tuberkuloseinfeksjonen har beslaglagt morkaken , kan barnet bli smittet ved å svelge bakteriell fostervann. Hvis mors urinveier og dermed seksuelle organer påvirkes, kan den nyfødte bli smittet ved fødselen.
Immunologi og patologi
Etter smitte er patogenene i de fleste tilfeller allerede frastøtt i luftveiene. Av alle de smittede utvikler bare omtrent en tidel faktisk tuberkulose. Hvorvidt en organisme kan forsvare seg tilstrekkelig mot mykobakteriene, avhenger av mange faktorer. Ernæringsstatus, en genetisk disposisjon (det er omtrent 20 kjente genpolymorfier som øker risikoen for sykdom opp til en faktor 5), samt et medikament, infeksjonsrelatert eller giftig undertrykkelse av immunforsvaret , men også mengden av inntatt bakterier og kontaktfrekvensen er viktig. Roms størrelse og ventilasjon og mangel på UV-lyskilder kan også spille en rolle som faktorer.
Spesialiserte fagocytter ( alveolære makrofager ) i de pulmonale alveolene representerer et første forsvar skansekledning . Disse kan absorbere patogener inn i deres indre av cellen ( phagocytize ), men da kan ikke drepe dem. Selv andre fagocytter som har blitt kalt, er ikke i stand til å gjøre dette. Prosessen med fagocytose aktiveres av forskjellige stoffer på overflaten av patogener. Dette kan være komponenter i celleveggen, men også vertsmolekyler som har bundet seg til inntrengerens cellevegg. Mykobakterier forhindrer cellekomponentene i fagosomene de befinner seg i, de såkalte fagosomene, i å modnes ytterligere. Dette sikrer overlevelse av Mycobacterium tuberculosis. Den immunsystemet danner således en vegg av flere ringer av forskjellige forsvarsceller rundt den initiale infeksjonsfokus. Denne forsvarsveggen til åtselceller (makrofager), såkalte epitelceller, Langhans gigantiske celler og lymfocytter dannes rundt et sentralt fokus for betennelse med vevsdestruksjon ( nekrose ). Denne spesielle formen for nekrose, som også er patognomonisk for TBC, kalles caseating nekrose . Hele strukturen kalles tuberkuløst granulom (eller tuberkulom ). Den isolerer Mycobacterium tuberculosis ved inngangsstedet og forhindrer at den sprer seg. Dette krever en fungerende interaksjon mellom de forskjellige immuncellene, som kaller og aktiverer hverandre via forskjellige messenger-stoffer ( cytokiner ). Spesielt forårsaker frigjøring av tumornekrosefaktor nitrosativ stress i fagosomet, som sammen med innkapslingen tvinger bakterien til å gå i sovende tilstand.
Mykobakteriene reagerer på sin side på innkapslingen med en endring i deres aktivitetstilstand. Siden genomet til de viktigste mykobakterielle stammene ble dechifrert i 1998, er forskjellige mekanismer for dette blitt oppdaget. De er i stand til midlertidig å stoppe stoffskiftet i granulom eller justere det på en slik måte at de metaboliserer fettene som forekommer her og dermed krever spesielt lite oksygen. Du er nå i fasen av dvalen , d. det vil si at de deler enda sjeldnere. Denne sovende primære infeksjonen kan utvikle seg til (post-primær) aktiv tuberkulose gjennom en fornyet overgang til en aktiv tilstand. Siden det er bevist at dette også kan skyldes en (eksogen) reinfeksjon (eksogen flytting), må det antas at en tidligere infeksjon ikke gir tilstrekkelig beskyttelse mot sykdomsutbrudd ved fornyet kontakt. Dette gjør det klart hvorfor det er så vanskelig å utvikle en effektiv vaksine mot tuberkulose.
Symptomer
I utgangspunktet er sykdomsforløpet i tuberkulose delt inn i forskjellige stadier. Tegn på sykdommen som manifesterer seg umiddelbart etter infeksjon kalles primær tuberkulose . Siden bakteriene er sovende i kroppen for livet selv med et intakt immunforsvar uten symptomer eller etter at primær tuberkulose har passert og kan reaktiveres når som helst, kalles en innledende infeksjon som ikke fører til sykdommen latent tuberkuloseinfeksjon (LTBI ) eller, etter en første sykdom, post-primær tuberkulose eller sekundær tuberkulose. Siden infeksjonen stort sett foregår i lungene, men i prinsippet også i ethvert annet organ, er lungetuberkulose også differensiert fra organtuberkulose .
Primær tuberkulose, lukket tuberkulose, tidlig form
Etter infeksjon via smittede dråper, dannes små betennelser med involvering av den tilknyttede lymfeknuten (primærkompleks) i lungene til den aktuelle personen i løpet av de tre til seks ukene som en reaksjon på bakteriene . Fokus for betennelse (tidlige infiltrater) er omsluttet av blodforsvarsceller. Små knuter (tuberkler) dannes. Innkapslet på denne måten forårsaker tuberkulosefoci ingen klager og har vanligvis ingen forbindelse til luftveiene ( bronkialsystemet ). Denne primære tuberkulosen (tidligere også primær urtese eller primær tuberkulose ) kalles lukket tuberkulose, som per definisjon ikke er smittsom da ingen patogener skilles ut. Mykobakteriene kan overleve i kroppen i årevis.
Hvis det infiserte individet ikke er i stand til å kapsle patogenet på denne måten, kan en aktiv infeksjon med for det meste ukarakteristiske symptomer (B-symptomer) oppstå fordi patogenet fortsetter å spre seg. Disse kan inkludere tretthet og svakhet, tap av matlyst og vekttap, hovne lymfeknuter , lav feber , spesielt om ettermiddagen, nattesvette og konstant hoste uten mye slem. Heshet kan indikere at strupehodet er involvert i økt risiko for infeksjon. Hos alvorlig syke mennesker kan disse symptomene være svake og noen ganger fraværende til tross for infeksjonsfare. Dannelsen av ekssudat som en del av en infeksjon i lungehinnen kan også føre til en pleural effusjon i tuberkulose (pH-verdien i pleuravæsken viser deretter acidose ). Alvorlige forløp med blodig sputum ( hemoptyse ), alvorlig anemi og undervekt er heller ikke sjeldne i Sentral-Europa. Antall dødsfall fra tuberkulose har flatet seg langt mindre enn det totale antallet tilfeller de siste tiårene. Siden 1980-tallet har det særlig vært en nedgang i lettere lukkede former.
Hvis mykobakterier blir sådd hos en svekket person via blodbanen med involvering av begge halvdelene av lungene og mange organer samtidig, snakker man om miliær tuberkulose . Det er oppkalt etter miliæren ( hirse-lignende , fra latinsk milium "hirse, hirse korn ") såing ( metastase ) vist på røntgenbildet og presenterer seg som et seriøst klinisk bilde med betydelig svekkelse av den generelle tilstanden, feber, tap av appetitt, vekttap, hoste og kortpustethet. Også meningitt (tuberkulær hjernehinnebetennelse ) kan utvikle seg på denne måten. Dette viser seg først i ukarakteristiske symptomer som irritabilitet og personlighetsendring. Senere kan meningittiske tegn med hodepine, nakkestivhet, hallusinasjoner, nedsatt bevissthet, kramper og feber, dvs. en alvorlig svekkelse av den generelle tilstanden, oppstå. Hvis den ikke behandles, fører det til koma og død. Det kan også forekomme tuberkel av choroid (Chorioidaltuberkel). Ekstremt svake immunforsvar kan føre til fulminant sepsis , vanligvis dødelig, som ofte blir referert til som Landouzy sepsis .
Post-primær tuberkulose, sekundær tuberkulose
Hos minst ti prosent av mennesker som har fått tuberkulose, bryter sykdommen ut senere som sekundær tuberkulose . Pasientene klager ofte på forskjellige symptomer: hoste vedvarende i flere uker med hoste opp gulgrønn slim, utmattelse, tretthet, subfebrile temperaturer om kvelden og nattesvette. Brystsmerter og kortpustethet kan oppstå når du hoster. Blodig sputum kan være et uttrykk for erosjon av bronkiene eller slimhinnen i luftrøret (bronkial tuberkulose, luftrør slimhinne tuberkulose), ofte er en åpen, smittsom sykdom allerede til stede. Blodig sputum bør derfor avklares umiddelbart av en lege.
Tuberkulosebakteriene formerer seg i lungene og ødelegger vevet. Hvis mindre eller mellomstore grener av bronkietreet eroderes, blir det ødelagte vevet koblet til luftveiene og hostes deretter opp. Sputumet inneholder nå bakterier - pasienten har åpenbar tuberkulose. I det avanserte stadiet kan ytterligere organer angripes ved å så bakteriene via blodet (hematogen spredning) . Da vises for eksempel smertefulle hevelser på knærne og andre ledd ( Poncets sykdom eller Poncets sykdom , oppkalt etter kirurgen Antonin Poncet, som beskrev tuberkuløs revmatoid eller revmatisme tuberculosus i 1897) eller ryggraden ( leddet tuberkulose, bein tuberkulose ). En spesiell form for tuberkulose er hudtuberkulose (lupus vulgaris) , som i Mellom-Europa tidligere ble sett på som et resultat av å drikke rå melk og den tilknyttede infeksjonen med Mycobacterium bovis , men har nå blitt svært sjelden . Ikke-helbredende små sår, sprekker, vorte-lignende foci av pus og omskrevne sår inkluderer. typiske symptomer på hudtuberkulose.
Organ tuberkulose, ekstrapulmonal tuberkulose
I tillegg til involvering av lungene, som er det desidert hyppigst berørte organet på rundt 80%, kan tuberkulose også manifestere seg i mange andre organer. Dette organet tuberkulose (tidligere også kjent som organ phthisis ) kan oppstå enten gjennom primærinfeksjon ved andre enn luftveiene eller ved spredning via blodstrømmen som en del av primær tuberkulose i lungene inngangspunkter. Dette påvirker igjen lymfeknuter ( lymfeknute tuberkulose ) hyppigst.
- Hudtuberkulose ( Skrophuloderm , se Skrophulosis ) kan utvikle seg hvis det er en tendens til å smelte ned i de osteaktige vevsavsetningene ( nekroser ) som er typiske for tuberkulose.
- Tuberkulose i muskler og seneskede kan også forekomme.
- Den nedre bryst- og korsryggen påvirkes ofte og betennelsen fører til mykning og deformasjon med gibbusdannelse (såkalt Potts sykdom ). Tidligere var det ofte vanskelig å stille differensialdiagnosen av rakitt. Denne manifestasjonsformen kan føre til dannelse av en abscess i området av psoas-muskelen . Lokaliseringen nær ryggmargen og nervekanalene som går der, er ofte klinisk merkbar i form av nevrologiske underskudd eller nevropatisk smerte som ofte stråler ut i bena og baken.
- Tuberkulose i hjernen eller hjernehinnene (tuberkuløs hjernehinnebetennelse, tuberkuløs hjernehinnebetennelse) kan visualiseres med dagens bildebehandlingsmetoder. Det kan sikres mikrobiologisk ved en lumbal punktering. Det påvirker hovedsakelig de basale (nedre) delene av hjernen og fører klinisk ofte til skade på hjernenervene som kommer ut der .
- Involvering av nyrene , binyrene , urinveiene og kjønnsorganene kalles nyretuberkulose, kjønns tuberkulose eller urogenital tuberkulose og forekommer vanligvis gjennom blodstrømmen.
- Beintuberkulose (med skadede bein, også kjent som beinkaries ) er en sjelden form for manifestasjon som oppstår gjennom blodbanen.
- Den intestinal tuberkulose er meget sjelden, men det forekommer oftest gjennom en primær infeksjon med Mycobacterium bovis i infiserte melk.
- Når strupehulen tuberkulose ( Larynxtuberkulose ) er en svært smittsom komplikasjon av (åpen) lungetuberkulose.
- En sjelden manifestasjon er tuberkulose i tennene, munnslimhinnen og tungen, som vanligvis kan skyldes bronkogen spredning i allerede eksisterende lesjoner. Orale funn kan omfatte tanngranulomer, sår i tannkjøttet og munnslimhinnen og en forstørret tunge. Oral involvering er funnet hos rundt 1,4% av de som lider av tuberkulose, ifølge studier. Oral tuberkulose kan også forekomme isolert.
Diagnose
En historie med infeksjon , en tuberkulinhudtest, en interferon-γ blodprøve, vevsundersøkelser, bildediagnostikk og, hvis det er mulig, påvisning av kulturpatogenet bidrar til diagnosen. Diagnosen blir bare bekreftet dersom tilfeldefinisjonene, i Tyskland, av Robert Koch Institute , er oppfylt, for eksempel hvis det i tillegg til det kliniske bildet er bevis for et kulturelt patogen av Mycobacterium tuberculosis . Disse metodene kan suppleres med moderne molekylærbiologiske eller immunologiske testprosedyrer for spesielle spørsmål . Imidlertid blir en pålitelig diagnose vanskeliggjort av den ekstremt forskjellige presentasjonen.
Tuberkulin hudtesting
Ved tuberkulinhudtest ble en definert mengde renset og filtrert (også kalt Mantoux-test) antigener av mykobakterier (tuberkulin) i huden ( epidermis injisert). Vanlige stempelprøver er også veldig upålitelige og anbefales derfor ikke. Hvis immunforsvaret til den testede allerede har hatt kontakt med mykobakterier, oppstår en forsvarsreaksjon på det aktuelle punktet innen tre dager med immunceller som migrerer inn i huden, noe som fører til fortykning. Dette er en type IV-reaksjon (ifølge COOMBS). Testen blir positiv bare seks uker etter infeksjon med TBC.
En håndgripelig herding på teststedet kalles en positiv reaksjon. Dette kan bety at en tuberkuloseinfeksjon har funnet sted. Imidlertid sier testen ingenting om en sykdom. En positiv testreaksjon er også mulig etter en tuberkulosevaksinasjon. Hvis huden på teststedet forblir uendret, eller hvis den bare viser rødhet, blir dette vurdert som negativ. En tuberkuloseinfeksjon blir da utelukket med stor sannsynlighet.
Tuberkulintesten er ufarlig og godt tolerert. Det kan også utføres uten å nøle for gravide, ammende eller små barn.
Tuberkulintester er bare pålitelige i begrenset grad. På den ene siden kan de forbli negative, spesielt i alvorlige tilfeller, for eksempel miliær tuberkulose. På den annen side fører en tidligere vaksinasjon eller kontakt med atypiske mykobakterier ( andre mykobakterier enn tuberkulose, MOTT ) til en falsk positiv reaksjon.
Imaging
Hvis det er mistanke om tuberkulose basert på symptomer og tidligere historie, røntgenundersøkelser eller, i tilfelle spesielle spørsmål, CT i lungene er nyttige avbildningsmetoder, selv om tuberkulintesten er negativ . De avslører ofte det karakteristiske, møllspiste bildet av lungeangrep av tuberkulose, som har gitt sykdommen kallenavnet møllen . Disse undersøkelsene viser også et funn i lukket tuberkulose. Ulempen er imidlertid at en røntgen ikke kan skille mellom tuberkulose og andre lungesykdommer med tilstrekkelig sikkerhet.
Hos barn under 15 år og gravide kvinner, hvis tuberkulose mistenkes, bør en immunologisk testmetode som γ-interferontest eller en tuberkulinhudtest foretrekkes i stedet for en røntgen .
Patogen deteksjon
Diagnosen tuberkulose bekreftes når det er kulturelt bevis for patogenet. Dette er imidlertid bare mulig uten videre fra sputum i tilfelle åpen tuberkulose, dvs. når tuberkuløse vevsendringer er koblet til bronkialsystemet , urinveiene eller tarmene og kan skilles ut. Ellers kan det forsøkes å skaffe materiale gjennom punkteringer med nåler eller direkte ved å fjerne vev. Fordelen med kulturelle bevis ligger i muligheten for å kunne utføre en motstandstest og bør derfor alltid være rettet mot, siden behandlingen da kan utføres målrettet.
Siden barn for det første knapt har sputum og for det andre bare noen få bakterier hoster opp, er en konvensjonell sputumprøve neppe pålitelig for dem. Magefastesaften blir derfor undersøkt i barndommen, fordi det er her all sekresjonen som barna hostet opp om natten og deretter svelget, samler seg . Mykobakteriene er igjen syrebestandige og kan overleve i magesaft. Sørafrikanske forskere var i stand til å bevise at patogenoppdagelsen også er mulig hos spedbarn og barn fra sputum. Hvis du lar dem inhalere på forhånd med en saltoppløsning med høy prosentandel (indusert sputum), er påvisning av mykobakterier fra den senere hostede sekresjonen like pålitelig som fra magesaft.
På grunn av den langsomme veksten av bakteriene, må du vente i fire til seks uker på et resultat på konvensjonelle, solide kulturmedier. I flytende kulturer med moderne påvisningsmetoder for mykobakteriell vekst, kan påvisningen lykkes etter omtrent to uker. Dyreforsøket som ofte ble brukt tidligere, hvor marsvin ble injisert med materialet som skulle undersøkes i bukhulen, brukes ikke lenger. Moderne deteksjonsmetoder inkluderer molekylære genetiske metoder som polymerasekjedereaksjon .
Immunologiske testprosedyrer
I tillegg til tuberkulinhudtesten har en ytterligere immunologisk testprosedyre, den såkalte γ-interferontesten , vært tilgjengelig som et ytterligere diagnostisk alternativ siden 2005 . Forsvarsceller fra testpersonens blod stimuleres med en blanding av antigener fra Mycobacterium tuberculosis . Hvis vedkommende allerede har hatt kontakt med patogenet på grunn av en tuberkuloseinfeksjon, produserer de i økende grad messenger-stoffet interferon-γ . Konsentrasjonen av dette interferon-γ kan bestemmes i cellesupernatanten, og i blodprøver fra infiserte mennesker er det betydelig høyere enn i en negativ kontroll som skal utføres . Siden de valgte antigenene bare skal forekomme i Mycobacterium tuberculosis , men ikke i de fleste av de atypiske mykobakteriene og heller ikke i vaksinestammene av mycobacteria som brukes til BCG-vaksinering, kan denne metoden teoretisk brukes til å passere mellom infeksjoner hvis tuberkulinhudtesten er positiv Differensier tuberkulosebakterier og atypiske mykobakterier. Den følsomhet av disse testene er gitt i forskjellige studier med 82% til 100%, er spesifisiteten med 98%.
Imidlertid er det å utføre testene forbundet med vanskeligheter og usikkerheter i praksis. Tidsvinduet for inkubasjonen og den nødvendige temperaturkonstanten på 37 ° C gir feilkilder, samt den nødvendige erfaringen med metoden i selve laboratoriet. De angitte verdiene for følsomhet og spesifisitet er derfor langt fra oppnådd i øve på. Med de to testene som ble introdusert, ser det ut til at ELISPOT (spesielt T-SPOT- testen) har en fordel, spesielt hos barn og med et ekstremt lavt antall hjelperceller. Men også her er det feilkilder i den preanalytiske fasen.
Som med alle undersøkelsesmetoder, hvis følsomhet og spesifisitet ikke er 100%, avhenger den informative verdien også av hyppigheten av den virkelige infeksjonen. Derfor er disse in vitro-testene også uegnet til screening av befolkning eller yrkesgrupper med lave forurensningsnivåer. I tilfelle tvilsom eksponering og positiv svikt eller bekreftet nær eksponering og negativ svikt, anbefales en presis klinisk undersøkelse ved bruk av Mendel-Mantoux-metoden og om nødvendig en repetisjon med den alternerende Y-interferontesten. Infeksjonstidspunktet kan heller ikke bestemmes med de nyere in vitro testmetodene. Testen blir ofte negativ igjen de neste tiårene etter at infeksjonen har grodd. Det har vært rapporter om forstyrrelser fra tidligere BCG-vaksinasjoner eller boostervirkninger etter tidligere testing i henhold til Mendel-Mantoux.
I 2010 presenterte en britisk forskningsgruppe en test basert på endringer i transkripsjonsignaturen i nøytrofile. Denne testen skal gjøre det mulig å skille mellom en fortid og en aktiv infeksjon. Markedsberedskapen gjenstår å se.
terapi
Siden patogenene deler seg veldig sakte og også kan hvile lenge i tuberkulære granulomer, er risikoen for å utvikle resistens i mykobakterier spesielt høy. Ved bekreftet tuberkulose eller til og med høy grad av mistanke om tuberkulose, må alle pasienter derfor behandles med en kombinasjonsbehandling av flere antibiotika (også kjent som antituberkulotika) som er spesielt effektive mot Mycobacterium tuberculosis . I tillegg, på grunn av den lave delingsgraden, må behandlingsvarigheten være lang nok til å unngå tilbakefall.
Standard terapi
I henhold til 2011-retningslinjene, bør behandling av ukomplisert tuberkulose bestå av en firdoblet kombinasjon av isoniazid , rifampicin , ethambutol og pyrazinamid og skal først utføres i to måneder. Deretter må behandlingen med isoniazid og rifampicin fortsettes i ytterligere fire måneder. Så det tar til sammen minst seks måneder. Hos barn brukes i utgangspunktet bare en trippel kombinasjon (uten ethambutol). I spesielt milde tilfeller er dette unntaksvis mulig for voksne. Streptomycin er også tilgjengelig som reservemedisin i tilfelle intoleranse . Thiacetazone , et sjette stoff, brukes ikke i industriland på grunn av dets ugunstige bivirkningsprofil. Det anbefales ikke for behandling av samtidig infiserte pasienter med HIV. Imidlertid er flertallet av tuberkuloselidere i noen fattige land, der stoffet fortsatt brukes på grunn av den lave prisen, også HIV-positive.
Den vanligste bivirkningen av isoniazid er perifer polyneuropati . Videre, som med rifampicin og pyrazinamid, kan leverskade også forekomme. Etambutol kan forårsake betennelse i synsnerven , mens streptomycin skader nyrene og det indre øret . Disse organene bør undersøkes før oppstart og overvåkes i løpet av behandlingen.
Siden pasientene ofte føler seg relativt sunne, tar mange av dem ikke lenger tablettene regelmessig etter en viss periode (dette blir referert til som lav etterlevelse ). Etter at flere nye tuberkulosemedisiner er i ferd med å bli godkjent, blir musestudier allerede utført for å avgjøre hvilken legemiddelkombinasjon som kan forkorte behandlingstiden. Med kombinasjonen av TMC207, pyrazinamid og rifapentin / moxifloxazine, ble 100 prosent av bakteriene drept i musen, til tross for forkortelse til to måneder.
Skulle man finne resistens i den mikrobiologiske bakteriekulturen, må en endring til andre antibiotika, som den spesifikke bakteriestammen faktisk er følsom overfor, vurderes i forhold til en spesifikk terapi. I flytende kulturer (Bactec MGIT) kan vekst av mykobakterier påvises etter en uke med høy initial konsentrasjon og uten forbehandling. En positiv vekst i det flytende kultursystemet alene tillater ikke en artsdiagnose av mykobakteriene, men den representerer grunnlaget for en eksakt artsdifferensiering ved hjelp av ytterligere diagnostiske metoder. Den parallelle inkubasjonen av faste kulturmedier (Löwenstein-Jensen og Stonebrink medium ) tar vanligvis lengre tid, men tillater en vurdering av kolonimorfologi. Det endelige resultatet av kulturen er tilgjengelig i festivalkulturen etter maksimalt 8-10 uker. Den konvensjonelle motstandstesten av standardmedisinene tar minst ti dager. Det er nå kommersielle rasktester som kan oppdage motstand tidligere ved hjelp av molekylærbiologiske metoder. Imidlertid har disse nyere metodene ennå ikke bevist seg i praksis.
Terapi av multiresistent tuberkulose
Hvis det er resistens mot standardmedisinene, etter behandling av alle tilgjengelige antituberkulotika, bør behandlingen utvides til å omfatte minst to effektive stoffer. Anvende kombinasjoner av ulike aktive forbindelser: De aminoglykosider capreomycin og kanamycin , de fluorokinolonene , ofloxacin / levofloksacin , ciprofloksacin og moxifloxacin de thionamides ethionamide , prothionamide , så vel som et bakteriostatisk aktive substanser 4-aminosalisylsyre (PAS), og cykloserin eller terizidone .
For sekundærbehandling i tilfelle resistens kan streptomycin, amikacin og protionamid også vurderes.
I noen tid ble antibiotika linezolid ansett som et mirakelvåpen mot multiresistent tuberkulose og brukes fremdeles i dag i spesielt alvorlige tilfeller. I en nylig studie av Lee kan imidlertid 82% av pasientene ha utviklet linezolid-assosierte bivirkninger. De vanligste bivirkningene er myelosuppresjon med anemi og nøytropeni, optisk nevropati og perifer nevropati.
Behandlingen av multiresistent tuberkulose ( engelsk multiresistent tuberkulose - MDR-TB ) tar flere legemidler samtidig over en periode på minst 21 måneder. De første tre månedene får pasientene en blanding av fem forskjellige medisiner. I prinsippet er sjansene for vellykket behandling av multiresistent tuberkulose lavere enn ved behandling av ukomplisert tuberkulose, selv om pasienten får den mest effektive behandlingen.
Bruk av ofloxazine og levofloxazine er neppe gjennomførbart i fattige land på grunn av de relativt høye produktprisene. Begge aktive ingrediensene er patentert av produsenten. Capreomycin selges bare av en enkelt produsent ( Eli Lilly ) til en pris som begrenser bruken enormt.
I mellomtiden er også nyere medisiner inkludert i behandlingen av multiresistent tuberkulose. Så ble en musemodell vellykket kombinasjoner av Bedaquiline , PA-824 og Sutezolid og rifapentine brukt.
Bedaquiline (handelsnavnet Sirturo ) er i mellomtiden godkjent av EU-kommisjonen . To andre legemidler - den nye kjemiske enheten Delamanid (handelsnavn: Deltyba ; produsent: Otsuka Pharmaceuticals ) og det velkjente stoffet 4-aminosalicylsyre (handelsnavn: Granupas ; produsent: Lucane ) - ble godkjent over hele Europa i mai 2014.
I en tyrkisk studie resulterte tilleggsbruk av lungereseksjon i permanent kur hos 12 av 13 MDR-TB-pasienter.
Blant annet reduserer tioridazin aktiviteten til antibiotikaresistens i Mycobacterium tuberculosis, og det blir derfor undersøkt bruken av den i kombinasjon med antibiotika.
Terapi av kompleks tuberkulose
I tilfelle ytterligere komplikasjoner, som for eksempel obstruksjon av en del av luftveien gjennom en involvert lymfeknute, bør behandlingen utvides til totalt ni til tolv måneder. Miliær tuberkulose eller tuberkuløs hjernehinnebetennelse (hjernehinnebetennelse) krever en første firedobbelt behandling, selv i barndommen, i mer enn tre måneder og en forlengelse av den totale behandlingsvarigheten til ni til tolv måneder. I tillegg bør pasientene behandles i minst seks uker med prednisolon eller, i tilfelle hjernehinnebetennelse, med deksametason i synkende doser.
Behandling av tuberkulose hos samtidig HIV-infiserte pasienter utgjør en spesiell terapeutisk utfordring, spesielt standardmedisinen rifampicin må ikke administreres samtidig med visse aktive ingredienser som brukes til å behandle HIV-infeksjon på grunn av betydelige interaksjoner. Derfor må enten HIV-terapi eller tuberkulostatisk terapi endres av passende erfarne spesialister.
Støttende behandling
På grunn av vanskeligheten og lengden på standardterapien ble det gjort forsøk på å støtte behandlingen ved å tilsette forskjellige stoffer. Det mest lovende var L- arginin , en aminosyre som antas å støtte dannelsen av reaktive nitrogenarter i makrofager , for eksempel gjennom daglig inntak av 30 peanøtter, som inneholder ca. 1 g L-arginin, og vitamin D , dets generelle støttende rolle i infeksjoner er okkupert. Begge stoffene er utilstrekkelig tilgjengelige hos syke mennesker.
I en randomisert studie av Queen Mary University of London akselererte høy-dose vitamin D-behandling hos pasienter med lungetuberkulose til og med akselerert mikroskopisk sputumkonvertering. H. hvor lang tid pasienter er smittsom, reduserte betydelig fra 36 til 23 dager. Konsentrasjonen av forskjellige inflammatoriske cytokiner og kjemokiner i blodet ble redusert og livstruende inflammatoriske symptomer reduserte raskere enn i kontrollgruppen.
I en studie med kaniner undersøkte Subbian og andre også innflytelsen fra en PDE-4-hemmer på den medfødte immunresponsen i lungene og effekten som deres svekkelse i sin tur hadde på ekspresjonen av forskjellige bakterielle gener. Det var redusert ekspresjon av INH-resistensgenene, og relatert til dette, en bedre clearance av vevet etter behandling med isoniazid .
En annen mulighet er å svekke granulomdannelsen i lungene ved hjelp av laktoferrin . Det er ingen kliniske studier på dette ennå.
Forebygging
Siden det foreløpig ikke er noen effektiv vaksinasjon mot tuberkulose, er det viktigste forebyggende tiltaket å oppdage smittede så tidlig som mulig og behandle dem både raskt og effektivt. På grunn av det lave antallet tilfeller i Tyskland, er ikke serieundersøkelser i form av tuberkulintester eller røntgenundersøkelser nyttige. Det aktive søket etter smittede i form av en omliggende undersøkelse av kontaktpersoner til pasienter med smittsom tuberkulose er en uunnværlig forutsetning for å redusere forekomsten av sykdommen. Gruppen mennesker med økt risiko for tuberkulose som bør lages aktivt etter en infeksjon inkluderer for eksempel også personer fra land med høy tuberkulosefrekvens, hjemløse, rusmisbrukere, innsatte i fengsel, men også HIV-positive. Den personlige risikoen for sykdom kan nå vurderes algoritmisk under hensyntagen til viktige påvirkningsfaktorer . Et sofistikert eksempel på dette, som også tar hensyn til legemiddelintoleranse , er den online TST / IGRA-tolk, som ble utviklet ved McGill University i Canada av Dick Menzies og hans kolleger.
vaksinasjon
Fram til 1998 ble det i Tyskland utført en aktiv vaksinasjon (levende vaksinasjon) med den svekkede mykobakterievaksinestammen Bacillus Calmette-Guérin (BCG) mot tuberkulose. På grunn av den avtagende beskyttende effekten, lokale komplikasjoner og bivirkninger og den endrede epidemiologiske situasjonen, har indikasjonen for BCG-vaksinasjon bare sjelden blitt gjort i Tyskland siden 1998. Da vaksinen ble introdusert, skjedde Lübeck-vaksinasjonsulykken i Lübeck i 1930 . 208 barn ble smittet med virulente tuberkulosebakterier gjennom feil behandling av BCG-kulturen hentet fra Paris til en vaksine. 77 av dem døde. På grunn av denne vaksinasjonsulykken vet vi nå mye om sykdomsforløpet fra å observere disse barna. Innføringen av vaksinasjon i Tyskland ble forsinket til etter andre verdenskrig. BCG-vaksinering anbefales ikke lenger av den stående vaksinasjonskommisjonen fordi den begrensede effektiviteten ikke kunne oppveie vaksinasjonskomplikasjonene. I tillegg er tuberkulintesten hos vaksinerte mennesker tidvis litt til moderat positive selv etter flere tiår. Av denne grunn blir denne testen (f.eks. Etter kontakt med en person som lider av åpen TBC) bare vurdert positivt hvis det er en sterkere reaksjon i form av en herdet hevelse (induration) på mer enn 15 mm over underarmsaksen. BCG-vaksinasjonen klarte heller ikke å dempe spredningen av tuberkulose over hele verden, selv om den er en av de mest utbredte vaksinasjonene. Bare de spesielt fulminante og fryktede kursene i barndommen i form av tuberkuløs hjernehinnebetennelse eller miliær tuberkulose kan BCG-vaksinasjonen være i stand til å forhindre relativt pålitelig. Forskjellige forskere prøver for øyeblikket å øke effekten av BCG-vaksinestammen gjennom gentekniske endringer der vaksinebakteriene produserer flere antigener som gjør at immunforsvaret kan reagere bedre på de virkelige mykobakteriene.
BCG-vaksinen er svært dårlig , spesielt i tropene og subtropene . Dyremodeller så vel som vaksinasjonsstudier med mennesker har vist at dårlig effektivitet skyldes eksisterende immunresponser mot jord og (drikke) vannlevende, ikke- patogene Mycobacterium- arter. Mange av mykobakteriene har kryssreaktive antigener , slik at infeksjon med det ene mykobakteriet gir en viss beskyttelse mot infeksjon med det andre. Dette har konsekvenser for vaksinasjonsbeskyttelse: På den ene siden er det antistoffer mot BCG live vaksine - vaksinen blir ødelagt av kroppen før den kan stimulere selve immunforsvaret. Og for det andre gir mykobakteriene som inntas i dagliglivet så god beskyttelse mot tuberkulosebakterien at vaksinasjonen ikke gir noen ekstra beskyttelse det er verdt å nevne. Det antas at bedre hygiene og drikkevannsbehandling i industriland mangler denne naturlige vaksinasjonen, og at BCG-vaksinering har vært effektiv hittil. På 1970-tallet ble det gjennomført en tuberkulosevaksinestudie på 260 000 mennesker i India. Dette viste at flere tilfeller av tuberkulose oppstod hos vaksinerte enn hos uvaksinerte.
En fase I-studie med en ny vaksine VPM1002 ble testet i Neuss i 2009 og 2010 med 80 frivillige og vurdert som godt tolerert. Vaksinen VPM1002 vil bli testet i en fase III-studie hos 2000 mennesker i India frem til 2020.
Den hittil lovende vaksinen MVA85A viste svakheter i fase II-studien i 2013. Det er ingen forbedring i forhold til den forrige vaksinen hos vaksinerte, friske og HIV-negative spedbarn. Det gjenstår imidlertid å se om vaksinen vil være til nytte for voksne eller HIV-positive mennesker (som ikke har lov til å motta den levende vaksinen). I tillegg til dette er 12 andre tuberkulosevaksiner for tiden i klinisk fase, AERAS-402 / Crucell Ad35 og GSK M72 blir for tiden testet på voksne og barn i Sør-Afrika.
På slutten av 2010 ble det vist at intranasal vaksinasjon med mRNA (Hsp-65) av M. leprae effektivt og trygt beskytter mot infeksjon med M. tuberculosis i en musemodell .
En annen ny utvikling er H4: IC31. Dette er et rekombinant fusjonsprotein H4 og adjuvansen IC31. H4 består av tuberkelantigenene Ag85B og TB10.4. Ag85B kalles også α-antigen og er en mycolyl - transferase . TB10.4 er et av tre veldig like proteiner i ESAT-6-gruppen av Mycobacterium tuberculosis. En test i Sør-Afrika på BCG-vaksinerte ungdommer var lovende.
Kjemoprofylakse og kjemoprevensjon
Siden små barn under fem år blir syke oftere og raskere enn voksne etter en infeksjon (ifølge litteraturen blir 20% av de smittede barna syke med en minimum latensperiode på rundt tre uker til år eller til og med tiår), gjelder spesielle forhold for dem etter kontakt med tuberkuloselidende Forebyggende tiltak. Selv om tuberkulintesten er negativ, bør de behandles profylaktisk med antituberkulotika (f.eks. Isoniazid ) i to måneder i henhold til retningslinjene i Swiss Lung League . Hvis tuberkulintesten fortsatt er negativ etter disse to månedene, kan behandlingen stoppes. Men hvis tuberkulintesten har blitt positiv i mellomtiden, må aktiv tuberkulose utelukkes ved en røntgenundersøkelse av lungene. I Europa gjøres dette gjennom et brystfoto; utenlands, som i Australia, derimot, anbefales tomografi av brystorganene, spesielt for barn. Behandling med medisinen mot tuberkulose fortsetter deretter i flere måneder som kjemoprevensjon. Hvis patogenet ved infeksjonskilden er kjent for å være resistent mot det antituberkulotiske stoffet, må selvfølgelig kjemoprofylakse utføres med en annen aktiv ingrediens, fortrinnsvis rifampicin . Ved flere motstander, bør det til og med utføres med to forskjellige aktive stoffer.
Rapporteringskrav
I Tyskland er menneskelig tuberkulose ”behov for behandling” en meldepliktig sykdom i henhold til infeksjonsbeskyttelsesloven (IfSG), selv om det ikke foreligger bakteriologiske bevis ( § 6 (1) setning 1 nummer 1a bokstav a IfSG). Sykdom og død skal rapporteres. I tillegg må folkehelseavdelingen rapporteres "hvis personer som er syke med lungetuberkulose som krever behandling, nekter eller avslutter behandlingen" ( § 6 (1) setning 2 IfSG). I tillegg er det også varslingsplikt for forvaltning av fellesanlegg i henhold til § 34 (6) IfSG.
Når det gjelder dyr, er sykdommen i Tyskland en meldepliktig dyresykdom i henhold til § 26 i dyrehelseloven (TierGesG) i forbindelse med avsnitt 1 og vedlegget til forordningen om meldepliktige dyresykdommer. Unntak er Mycobacterium bovis - inkludert underartinfeksjoner, som til og med er meldepliktige dyresykdommer i henhold til seksjon 4 TierGesG i forbindelse med § 1 i forordningen om anmeldelsespliktig dyresykdom .
I Østerrike er tuberkulose hos mennesker en meldepliktig sykdom i samsvar med § 3 i tuberkuloseloven . I følge dette må alle bevis på et tuberkulosepatogen, enhver aktiv eller smittsom tuberkulose sykdom samt alle dødsfall som kan tilskrives det rapporteres. I tillegg må enhver mistanke om tuberkulose rapporteres dersom personen med tuberkulose unngår diagnostisk opparbeidelse. Ifølge § 2 Tuberkulose loven, er det også en forpliktelse til å søke behandling (behandling plikt).
I Østerrike er storfittuberkulose meldepliktig i henhold til seksjon 16 i dyresykdomsloven.
I Sveits tuberkulose hos mennesker også en pliktige sykdom , og at etter at Epidemider Act (EPG) i forbindelse med epidemisk forordning og vedlegg 1 av den Regulering av EDI på rapportering av observasjoner av smittsomme sykdommer hos mennesket. Start av behandling med tre forskjellige antituberkulotika eller bevis på mykobakterier i tuberkulosekomplekset i klinisk materiale må rapporteres.
I Sveits er tuberkulose meldepliktig som en dyresykdom som skal utryddes i henhold til artikkel 3 i dyresykdomsforordningen (TSV) med omfattende forpliktelser i henhold til artikkel 158–165a.
Tuberkulose i andre levende ting
Tuberkulose forekommer i nesten alle virveldyr, og kan i tillegg til M. tuberculosis utløses av mange andre mykobakterier i Mycobacterium tuberculosis-komplekset .
Mycobacterium tuberculosis
M. tuberculosis kan forårsake sykdom hos både husdyr og ville dyr (som hjort og springbok ). Infeksjonen er beskrevet på grunn av nærmere kontakt med mennesker i mange tamme arter, f.eks. B. hos husdyr , huskatter og papegøyer og i dyreparker som elefanter .
I de fleste dyrearter er hovedfokuset hovedsakelig i lungene, så sykdommen ligner lungetuberkulose hos mennesker. Hos griser påvirkes mesenteriske lymfeknuter nesten utelukkende . Hos storfe fortsetter infeksjonen med M. tuberculosis vanligvis uten patologiske prosesser, men det som er viktig er at patogenet skilles ut med melken, og det er derfor pasteurisering av melken var et viktig tiltak for å bekjempe tuberkulose hos mennesker. Rå melk bør kun konsumeres fra tuberkulosefrie flokker.
Andre mykobakterier
Den tuberkulose i kveg er fra dyr til mennesker tuberkulose mest signifikant. Patogenene deres, Mycobacterium bovis og Mycobacterium caprae , har relativt høy vertsspesifisitet, men kan også forårsake sykdommer hos mennesker og andre pattedyr (inkludert mange husdyr og mange ville dyr), noe som gjør det til et zoonotisk patogen. Bovin tuberkulose er en meldepliktig dyresykdom . For infeksjoner hos andre husdyr som storfe, så vel som hos ville pattedyr, er rapporteringsplikten .
Den fjærkre tuberkulose er M. avium årsaker. Det var en av de vanligste sykdommene hos tamkyllinger , men er sjelden i dag. I prinsippet er alle fuglearter , men også mennesker, storfe , griser , sauer , geiter , katter og fremfor alt kaniner utsatt. Fugletuberkulose er en av de meldepliktige dyresykdommene .
Hos slanger er tuberkulose sjelden og går vanligvis kronisk infisert med tuberkel i de indre organene, den subkutane eller i munnen. De viktigste patogenene er M. thamnopheos , M. marinum og M. chelonae . Hos øgler er sykdommen også sjelden og kjører som en ikke-spesifikk generell sykdom eller med manifestasjoner i huden. De viktigste patogenene er M. ulcerans , M. marinum og M. thamnopheos. M. ulcerans forårsaker Buruli-sår hos mennesker .
Den fisk tuberkulose er M. marinum, M. fortuitum og M. chelonae produsert og påvirker både ferskvanns- og saltvannsfisk. Ved mating til infisert fisk kan M. chelonae også forårsake sårendringer i øvre fordøyelseskanal, lungebetennelse og hudsykdommer i skilpadder .
Den paratuberculosis er en av M. paratuberculosis indusert tarmsykdom av drøvtyggere .
Pseudotuberkulose
To forskjellige kliniske bilder som ligner veldig på tuberkulose, men som ikke er forårsaket av mykobakterier, blir referert til som pseudotuberculosis .
Pseudotuberculosis hos geiter og sauer - storfe, hester, griser og i økende grad kameler blir sjeldnere rammet - er en smittsom sykdom forårsaket av bakterien Corynebacterium pseudotuberculosis, som er relatert til mykobakteriene . Hos mennesker kan infeksjoner med lymfeknuteinflammasjon oppstå etter massiv kontakt med Corynebacterium pseudotuberculosis .
Likeledes Yersiniose forårsaket av Yersinia pseudotuberculosis i kaniner, gnagere og fugler er kalt pseudotuberculosis, og hos gnagere er det også kalles rodentiosis. Yersinia pseudotuberculosis er potensielt patogen for mange pattedyr- og fuglearter , inkludert mennesker.
historie
Paleolittisk og neolittisk
Undersøkelser av et omtrent 500.000 år gammelt fossil fra den tidlige mannen Homo erectus fra Tyrkia viste at tuberkulose skjedde mye tidligere i menneskets historie enn tidligere antatt. På hodet av hodeskallen var det spor etter hjernehinnebetennelse forårsaket av tuberkulose ( leptomeningitis tuberculosa ). Forskerne spekulerer i at denne tidlige mannen, som kom fra Afrika, var mørkhudet og derfor var i stand til å produsere betydelig mindre D-vitamin sammenlignet med lyshudede mennesker , noe som kunne ha gjort ham spesielt utsatt for denne sykdommen. Denne antagelsen om en sykdom med tuberkulose, som bare er basert på morfologiske skjelettendringer, så vel som den videre, nå for første gang bekreftet molekylærbiologisk funn av en 9000 år gammel prøve antagelsen om moderne forskning om at tuberkulose ikke skjedde i yngre steinalder under domesticering av storfe fra dem til hoppede mennesker, men utviklet seg parallelt med Homo erectus i en lang periode som begynte mye tidligere . Også skjelettrester av forhistoriske mennesker som dateres tilbake til ca 4000 f.Kr. BC viser spor etter sykdommen. Det er heller ikke et spørsmål om geografisk isolerte funn; heller, Mycobacterium tuberculosis ble oppdaget allerede i 2001 i Wyoming , Nord-Amerika, i 17.000 år gamle funn.
antikken
Tuberkulær ødeleggelse ble funnet i beinene til egyptiske mumier fra 3000 til 2400 f.Kr. Lignende funn fra det gamle Amerika dateres til rundt 2000 f.Kr. I følge skriftlige opptegnelser er det bevis for en tuberkuloseepidemi i India rundt 1300 f.Kr. Chr.
I det 5. århundre f.Kr. Chr. Fremhevet Hippocrates consumptive ( gresk. Φθίσις Phthisis tap, sløsing) som en av epidemiene, som nesten alltid var dødelig. Imponerende beskrivelser av sykdommer har kommet til oss fra ham.
middelalderen
I tidlig middelalder spilte tuberkulose en underordnet rolle i Europa på grunn av den sparsomme befolkningen. Det var bare sterkere representert i de få storbyområdene. Dette inkluderte først og fremst Byzantium . Datidens tuberkuloseofre kom fra alle klasser og opp til medlemmer av den keiserlige familien. Den medisinske litteraturen fra Byzantium beskriver tuberkulære sykdomsmønstre til enhver tid. Betydelige nyvinninger innen behandling av tuberkulose ble imidlertid ikke introdusert i middelalderen. Inntil den tidlige moderne perioden ble nivået av hippokratiske skrifter og deres Galen opprettholdt . Et av få unntak var Alexander von Tralleis fra Lydia på 600-tallet , som videreutviklet eller differensierte terapeutiske tiltak.
Tidlig moderne tid
Etter et tidligere utbrudd i Italia i andre halvdel av 1400-tallet begynte den største og lengste historiske bølgen av tuberkulose på 1600-tallet. Den nådde sitt høydepunkt på 1700-tallet, og fortsetter i den siste foten til i dag etter en midlertidig oppblussing av epidemien kort tid etter første og andre verdenskrig.
Når det gjelder oppfatningen av patogenese, eksisterte forskjellige tradisjoner i de europeiske landene på 1700-tallet. Mange medisinske forfattere den gangen anså tuberkulosen eller ikke alltid så synonymt forbruk (fra mellomhøy tysk Swinden "svinner, går ned i vekt, går ned i vekt osv.") Som den verste blant den da kjente sykdommen. Årsaken de så var en ujevn fordeling av kroppsvæsker , illevarslende fordampning fra jorden, urbanisering eller forfall av moral. I Italia derimot var det en tradisjonell tendens til smittsom, dvs. H. smittsom årsak. Følgelig innførte Republikken Venezia på midten av 1700-tallet obligatorisk skriftlig melding om sykdommer forårsaket av phthisis (forbruk på grunn av lungetuberkulose). De personlige effektene til de som døde av sykdommen ble brent for å redusere risikoen for infeksjon.
I England og Norden ble det derimot ofte antatt at sykdommen skyldtes en arvelig (arvelig) årsak. Et stort unntak i England var publikasjonen Benjamin Martens fra 1720: A New Theory of Consumptions, der Marten tilskrev årsaken til sykdommen til en infeksjon av mikroorganismer 162 år før Robert Koch . Martens som ble publisert i lite antall, fant imidlertid ikke noe videre mottak. I Frankrike, Tyskland og Sveits blandet representanter for begge skolene seg. I noen tilfeller var den arvelige teorien uttrykkelig representert her, men samtidig ble det innført tiltak for å redusere risikoen for smitte.
Johann Jakob Wepfer i Schaffhausen spilte en fremtredende rolle blant ftisiologene i sin tid , som hadde vedtatt ideen om smittsom etiologi av sykdommen under sitt studiebesøk i Italia . Han var den første som beskrev dannelsen av lungehuler ( hanc calamitatem ) fra tuberkler ( tubercula ). Hans arbeid og studier om epidemiologi av tuberkulose gikk på mange måter kvalitativt utover prestasjonene de neste to århundrene. De ble bare publisert postumt av sønnen i 1727 og forble ukjente utenfor en liten ekspertkrets.
1800-tallet
På grunn av det store antallet av symptomene ble sykdommen ikke differensiert fra andre med symptomer som ligner på scrofula, som er sjelden i dag, før på 1800-tallet . Det var først i 1819 at René Laënnec forklarte ensartetheten av tuberkler med miliærknuter og (tuberkuløse) huler og erkjente at tuberkuløs materie også kan dannes i andre organer i tillegg til lungene. Først i 1839 laget Johann Lukas Schönlein det ensartede begrepet tuberkulose.
Tuberkulose fikk allmenn interesse som den endemiske sykdommen hos de urbane fattige på 1800- og begynnelsen av 1900-tallet . I 1815 var en fjerdedel av dødsfallene i England og i 1918 i Frankrike en sjettedel av dødsfallene forårsaket av tuberkulose. I aldersgruppen 15 til 40-åringer skyldtes annenhver død i Tyskland rundt 1880 denne sykdommen. Tuberkulose var også den vanligste dødsårsaken i landlige områder. Av 2188 dødsfall registrert i Liechtenstein kommune Triesen mellom 1831 og 1930 skyldtes 15% tuberkulose.
På 1800-tallet ble luftkuret , der pasienter måtte ligge i det fri i flere timer om dagen, den foretrukne behandlingen for tuberkulose. Dette skjedde i våre egne tuberkulose sanatorier ( lunge sanatorier ); Hermann Brehmer bygde den første i verden i 1855 i Görbersdorf, Nedre Schlesien (i dag Sokołowsko , Polen).
Etter at det i nord ble erkjent at sykdommen var smittsom, ble tuberkulose meldt om i Storbritannia på 1880-tallet. Den gang var det kampanjer for å unngå å spytte ut på offentlige steder. De smittede fattige ble oppfordret til å gå til sanatorier som var mer som fengsler. Til tross for den påståtte bruken av frisk luft og arbeidet i sanatoriet, døde 75 prosent av de innsatte innen fem år (1908).
I tillegg til slike tiltak, som fremdeles var knyttet til konseptet hygienisk-diettbehandling, var det også veldig forskjellige lokale behandlingskonsepter på 1800-tallet med stadig bedre kirurgiske alternativer. Spesielt pneumothorax- teknikken eller pneumolysen fant utbredt bruk i mange varianter. En berørt lunge ble kunstig kollapset for å bringe lungen til stillstand og forandringene til å gro. Den italienske legen Carlo Forlanini anses å være oppfinneren av denne kollapsterapi for lungetuberkulose (siden 1892). Denne teknikken hadde liten nytte og ble gradvis avviklet etter 1946. I tillegg ble det utviklet stadig finere reseksjonsprosedyrer som de berørte lungeseksjonene ble fjernet med. Den internasjonalt anerkjente franske hjertekirurgen Théodore Tuffier var den første som resekterte lungespissen i tuberkulose.
Bakterien Mycobacterium tuberculosis ble beskrevet av Robert Koch 24. mars 1882. I 1905 mottok han Nobelprisen i fysiologi eller medisin for sin oppdagelse av patogenet . Koch trodde ikke at storfe og human tuberkulose var like, noe som forsinket påvisningen av infisert melk som sykdommens kilde. Denne kilden ble senere eliminert av pasteurisering . I 1890 brygget Koch et glyserinekstrakt av tuberkelbasillene som et hjelpemiddel for behandling av tuberkulose og kalte det tuberkulin . Det var imidlertid ikke effektivt når det ble brukt euforisk. Observasjonen av lokale hudreaksjoner ved bruk av tuberkulin førte senere til utviklingen av en testprosedyre for påvisning av infeksjon eller sykdom av Clemens von Pirquet i 1907, Felix Mendel og Charles Mantoux rundt 1910.
I 1883 oppdaget Robert Koch først tuberkelbasiller i vevet av lupus vulgaris, en hudsykdom som først ble beskrevet som en uavhengig sykdom på begynnelsen av 1800-tallet, og som dermed viste årsaken som hudtuberkulose. I følge erfaringen fra en lege fra Bielefeld ved navn Gerson, viste en diett rik på mineraler, men saltfri, tilsynelatende (angivelig i 448 av 450 tilfeller) av kirurgen Ferdinand Sauerbruch i München, hvor han hadde satt opp en lupusavdeling ved universitetsklinikken. (i første kvartal av det 20. århundre)) Suksesser i behandlingen av hudtuberkulose.
Det 20. århundre
Albert Calmette og Camille Guérin hadde den første suksessen med immunisering mot tuberkulose i 1906 med sin BCG- vaksine. Den ble først brukt på mennesker i Frankrike 18. juli 1921. Nasjonalistiske strømninger, som brukte Lübeck-vaksinasjonsulykken for egne formål, forhindret utbredt bruk i Tyskland før etter andre verdenskrig .
Likevel falt dødsraten forårsaket av tuberkulose betydelig i Europa i hundre år fra 1850 til 1950 fra 500 til 50 per år, basert på 100 000 innbyggere. Forbedringer i det offentlige helsevesenet, spesielt etableringen av et tett nettverk av tuberkulose velferdskontorer fra 1905, reduserte antall sykdommer allerede før innføring av antibiotika. Konseptet endret seg flere ganger. Fram til 1945 var fokuset på behandling av tidlige og lettere syke tilfeller. Konseptet for innleggelse ble fundamentalt endret i 1945 basert på opplevelsen av de krigspåvirkede årene 1917 til 1919. Primært bare alvorlig syke og smittsomme pasienter kom til sanatoriene. Medisinske fasiliteter er blitt oppgradert når det gjelder utstyr for å kunne tilby maksimal pleie, inkludert lungekirurgiske prosedyrer.
Med utviklingen av antibiotika streptomycin i 1943 ble aktiv behandling mulig i tillegg til forebygging. Suksessen skjulte imidlertid den hyppige motstanden til mykobakteriene mot streptomycin. Den nesten samtidige produksjonen av para-aminosalicylsyre (PAS) fikk i utgangspunktet liten oppmerksomhet, selv om kombinasjonen av disse to stoffene gjør dannelsen av resistente stammer vanskeligere. Fra 1952 fant isoniazid økende bruk som et annet tuberkulosemedisin. Kombinasjonsterapi for å unngå utvikling av resistens ble standarden for tuberkulosebehandling fra denne tiden av. Gjennombruddet innen behandling mot tuberkulose, som fortsetter den dag i dag, ble oppnådd på 1960-tallet med tilsetning av ethambutol og sist rifampicin.
På grunn av avskaffelsen av det offentlige helsevesenet i New York på 1970-tallet var det en økning i sykdommer der på 1980-tallet. Antallet som ikke klarte å ta medisinene, var høyt. Som et resultat fikk over 20.000 mennesker i New York en infeksjon som kunne forebygges med antibiotikaresistente stammer.
Siden fremveksten av antibiotikaresistente stammer (dvs. resistent mot minst rifampicin og isoniazid) på 1980-tallet, har håpet om at sykdommen kunne bli utryddet helt blitt redusert. Det var 50 000 tilfeller av tuberkulose i Storbritannia rundt 1955. Fra 1987 til 2001 økte antallet tuberkuloselidende i Storbritannia igjen fra 5500 til over 7000 bekreftede tilfeller.
Oppblomstringen av tuberkulose førte til at WHO erklærte en global helsesituasjon i 1993. I 1996 erklærte hun 24. mars verdens tuberkulosedag .
det 21. århundre
I land utenfor Europa og Nord-Amerika, som B. Bangladesh er tuberkulose fortsatt et stort helseproblem i det 21. århundre . En fornyet økning i saker har flere ganger vært knyttet til problemet med klimaendringer .
Tuberkulose i art
På grunn av sin enorme betydning gjenspeiles sykdommen på mange måter i kunsten. Noen kunstnere taklet konfrontasjonen med deres tidlige (egen) død på en imponerende måte. Selv i egypternes scenekunst, fra middelriket og fremover, ble representasjonen av gibbusen, det slående ytre uttrykket for Potts sykdom, funnet . Lignende fremstillinger har også kommet til oss fra gamle amerikanske kulturer.
- I de siste årene av sitt liv viste den tyske forfatteren Friedrich Schiller flere og flere symptomer på tuberkulose. I løpet av denne tiden ble et av hans viktigste verk opprettet, dramaet Wilhelm Tell . 9. mai 1805 døde forfatteren av akutt lungebetennelse forårsaket av tuberkulose i Weimar.
- Tre av de seks Brontë-søsknene døde av tuberkulose. Charlotte Brontë tok opp emnet i romanen Jane Eyre , der Janes venn Helen Burns dør av det. Tuberkulose er også et tema i søsteren Emily Brontés roman Sturmhöhe . Hindleys kone, Frances, dør av tuberkulose i veldig ung alder.
- Allerede i 1848 hadde Alexandre Dumas den eldre J. i romanen La Dame aux Camélias - Lady of the Camellias (EA Paris, Alexandre Cadot) den viktigste kvinnelige karakteren som dør av tuberkulose. Materialet ble brukt av Giuseppe Verdi (musikk) og Francesco Maria Piave (libretto) i operaen La traviata (italiensk: The Stumped or The Derailed), som hadde premiere i 1853 . I dette omkommer Violetta Valery realistisk tre handlinger av den hvite pesten . På tidspunktet for opprettelsen var det nesten en skandale å iscenesette døden så realistisk.
- I romanen Anna Karenina lar forfatteren Leo Tolstoj karakteren Nikolaj Dmitrijewitsch Levin dø av tuberkulose.
- I operaen La Bohème av Giacomo Puccini , som hadde premiere i 1896 , døde hovedpersonen Mimì av tuberkulose i fjerde akt.
- Også i Knut Hamsuns historie Victoria (1898) døde heltinnen sist av tuberkulose.
- Den tsjekkiske dikteren Jiří Wolker døde av tuberkulose i en alder av 24 år; han taklet sykdommen og den nært forestående døden i sitt senere arbeid.
- Et av de mest kjente eksemplene er trolig Thomas Mann's Zauberberg (første utgave fra 1924). Inspirert av sykdommen til kona Katia , finner han plottet til den verdensberømte romanen i Davos om gangen uten effektiv medisinering.
- Franz Kafkas lungetuberkulosesykdom, som han døde av i et østerriksk sanatorium nær Wien i 1924, er gjenstand for den biografiske romanen The Glory of Life av Michael Kumpfmüller (2011). I Franz Kafkas lignelse Auf der Galerie lider rytteren nevnt i første del av tuberkulose, kalt "lungeavhengighet" der. Franz Kafka led av tuberkulose hele livet.
- Den amerikanske countrymusikeren Jimmie Rodgers synger flere sanger om sin TB-sykdom, som han døde i 1933 i en alder av 35 år (TB Blues, 1931; Whippin 'That Old TB, 1933).
- I sangen TB Sheets , utgitt i 1967, beskriver den nordirske musikeren Van Morrison lidelsen til en ung jente som dør på tuberkuloseavdelingen på et sykehus fra kjærestens perspektiv som er helt overveldet av situasjonen.
- I John Schlesingers film Asphalt-Cowboy (1969) forsvinner den lille skurken Ratso - spilt av Dustin Hoffman - av tuberkulose.
- I romanen The Diary of Jutta S. av Inge Stolten er de diagnostiske og terapeutiske metodene fra 1950-tallet beskrevet i detalj, inkludert et lengre opphold i klimakuren for hovedpersonen.
- I romanen Les trois quarts du temps (Jeg vil leve) beskriver Benoîte Groult behandlingsmetodene som ble brukt i 1945 til den syke Jean-Marie døde.
- Den franske grafikeren Józef Gielniak , som døde av tuberkulose i et sanatorium i 1972, portretterte hovedsakelig tuberkulosefaget med dets helsemessige og sosiale konsekvenser og den lukkede verden av sanatorier i linosnittene.
- Den ene bærer den andres byrder ... (1987), prisvinnende DEFA- film, regissør: Lothar Warneke : I DDRs dager måtteen politibetjent og en protestantisk pastor dele et rom i en tuberkuloseklinikk. De diskuterer Gud, kjærlighet, meningen med livet, død og sykdom. Den første aversjonen blir til vennskap.
- Thomas Bernhard , som selv hadde led av tuberkulose fra tidlig alder, taklet sykdommen i nesten alle planter. Mange av hovedpersonene hans er syke og lider. Dette blir spesielt tydelig i hans selvbiografiske bind Die Kälte og Der Atem . Bernhard døde i 1989 av konsekvensene av denne sykdommen.
- I sin roman The Eternal Gardener beskriver John le Carré en konspirasjon fra 2001 av et multinasjonalt selskap som bruker en ny type medikament mot tuberkulose som fremdeles er under utvikling i et feltforsøk på lokalbefolkningen i Kenya uten deres kunnskap, og derved overgår etiske grenser.
- Ytterligere eksempler fra litteratur og film er i romaner av Fyodor Dostojewski Ippolít Teréntjeff i The Idiot og Katerina Ivanovna i Guilt and Atonement ; Julika Stiller-Tschudy i Stiller (roman av Max Frisch ); Patrice Hollmann (Pat) i Erich Maria Remarques roman Three Comrades ; Lilian i Remarkes roman Heaven has no minions ; Ruby Gillis i Anne på Kingsport (roman av Lucy Maud Montgomery ); Red Stovall (spilt av Clint Eastwood ) i filmen Honkytonk Man (US 1982); Satine (spilt av Nicole Kidman ) i filmen Moulin Rouge (USA 2001), basert på Verdis opera eller Dumas 'roman, se ovenfor.
- Angorichina er en roman fra Marion Grace Wolley fra 2011 om mennesker i et tuberkulosesanatorium i Australia på 1930-tallet.
- I 2014- filmen Winter's Tale , med Colin Farrell i hovedrollen , dør Beverly Penn, kjæresten til hovedhelten, spilt av Jessica Brown Findlay , av tuberkulose.
- I romanen, Ana i Venezia av João Silvério Trevisan, en av hovedpersonene, lider den svarte tidligere slave Ana i de siste årene av tuberkulose.
- I videospillet Red Dead Redemption 2 blir hovedpersonen syk av tuberkulose i løpet av spillet.
museum
1. desember 2011 ble museet for tuberkulose åpnet i Rohrbacher Schlösschen i Heidelberg på grunnlag av Thorax- klinikken. I stor grad består den av utstillinger og faglitteratur fra det tidligere tuberkulosearkivet i Fulda , som ble ledet av lungespesialisten Robert Kropp; det har vært åpent for publikum siden begynnelsen av 2012.
Verdens tuberkulosedag
Verdens tuberkulosedag finner sted 24. mars hvert år . Det ble proklamerte av Verdens helseorganisasjon (WHO) og støttes av European Medicines Agency (EMA). Hensikten er å øke offentlighetens bevissthet og påpeke at tuberkulose fortsatt er en epidemi i mange land rundt om i verden, hovedsakelig i utviklingsland . Datoen feirer dagen da Robert Koch kunngjorde i 1882 at han hadde oppdaget det forårsakende middelet til tuberkulose.
litteratur
1800-tallet
- August Predöhl: Historien om tuberkulose. Leipzig 1888; Opptrykk: Sendet, Wiesbaden 1966.
Det 20. århundre
- ML Holbrook: Forebygging, hygienisk behandling og kur av lungeforbruk. Concord, München 1900. (digitalisert versjon)
- Erich Stern : Psyken til lungepasienten. Innflytelsen av lungetuberkulose og sanatorium på sjels sjel. Halle på Saale i 1925.
- Kurt Lydtin: Lungetuberkulose som indikasjonsområde. I: Reichsärztekammer (red.): Retningslinjer for avslutning av graviditet og sterilitet av helsemessige årsaker. Redigert av Hans Stadler. J. F. Lehmanns Verlag, München 1936, s. 58-79.
- Norman Meachen: En kort historie om tuberkulose. London 1936; Omtrykk New York 1978.
- Richard Bochalli : Historien om forbruk . Leipzig 1940.
- Wilhelm Roloff : Lungetuberkulosen. Springer, Berlin / Göttingen / Heidelberg 1948.
- Wilhelm Roloff: Tuberkuloseleksikonet. 2. utgave. Thieme, Stuttgart 1949.
- Walter Schaich: Tuberkulose. I: Ludwig Heilmeyer (red.): Lærebok for indremedisin. Springer-Verlag, Berlin / Göttingen / Heidelberg 1955; 2. utgave, ibid. 1961, s. 224-308.
- Paul-Georg Schmidt: Lungetuberkulose - diagnose og terapi. Georg Thieme Verlag, Stuttgart, 3. Utgave 1956
- Michel Oury: Tuberkulosehistorie. I: Illustrert medisinhistorie. Tysk tilpasning av Richard Toellner , Salzburg 1980–1982 og som spesialutgave der i 1986, bind V, s. 2734–2755.
Nyere litteratur
- T. Schaberg, T. Bauer, F. Brinkmann et al.: S2k retningslinje: Tuberkulose i voksen alder. I: Pneumologi. Volum 71, 2017, s. 325-397.
- German Society for Pediatric Infectious Diseases V. (DGPI) (Red.): Håndbokinfeksjoner hos barn og ungdom. 4. utgave. Futuramed, München 2003, ISBN 3-923599-90-0 .
- Werner E. Gerabek : Lungetuberkulose. I: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil , Wolfgang Wegner (red.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4 , s. 871 f.
- Juan Carlos Palomino, Sylvia Leão, Viviana Ritacco og andre: Tuberkulose 2007. Fra grunnleggende vitenskap til pasientbehandling. (PDF; 8,3 MB) TuberculosisTextbook.com, vinner av Amedeo Textbook Award (engelsk), godt illustrert oversikt
- Peter D. Davies, Peter Barnes, Stephen B. Gordon: Klinisk tuberkulose. Hodder Arnold Publishers, 2008, ISBN 978-0-340-94840-8 .
- Marianne Abele-Horn: Antimikrobiell terapi. Beslutningsstøtte for behandling og profylakse av smittsomme sykdommer. Med samarbeid mellom Werner Heinz, Hartwig Klinker, Johann Schurz og August Stich, 2., revidert og utvidet utgave. Peter Wiehl, Marburg 2009, ISBN 978-3-927219-14-4 , s. 238–245.
- German Society for Pneumology and Respiratory Medicine (red.): 100 års tysk pneumologi. Springer, Berlin / Heidelberg 2010, ISBN 978-3-642-11453-3 .
- Christine Wolters: Tuberkulose og menneskelige forsøk i nasjonalsosialisme. Nettverket bak TB-eksperimentene i konsentrasjonsleiren Sachsenhausen. Steiner, Stuttgart 2011, ISBN 978-3-515-09399-6 .
- Jörg Braun: Smittsomme sykdommer. I: Jörg Braun, Roland Preuss (red.): Clinical Guide Intensive Care Medicine. 9. utgave. Elsevier, München 2016, ISBN 978-3-437-23763-8 , s. 437-519, her: s. 462 f. ( Tuberkulose ).
- Ulrike Moser: Forbruk. Nok en tysk sosialhistorie. Matthes og Seitz, Berlin 2018, ISBN 978-3-95757-556-2 .
Artikler i magasiner
- Hans Gertler: Historie om diagnose og terapi av tuberkulose. I: Medical Monthly Bulletin 11, 1957, s. 386-388.
- American Thoracic Society: Diagnostiske standarder og klassifisering av tuberkulose hos voksne og barn. I: American journal of respiratory and critical care medicine. Nr. 161, 2000, s. 1376-1395. PMID 10764337
- Flurin Condrau : behandling uten kur. Om den sosiale konstruksjonen av behandlingssuksess for tuberkulose tidlig på 1900-tallet. I: Medisin, samfunn og historie. Volum 19, 2000, s. 71-94.
- B. Hauer, D. Rohde, R. Loddenkemper: Tuberkulose. I: Pulmonologen. Nr. 4, Heidelberg 2005, s. 291-306, ISSN 1613-5636
- Horst Kremling : Historiske hensyn til forebyggende medisin. I: Würzburg sykehistoriske rapporter. 24, 2005, s. 222-260, her s. 225-227.
- Peter-Philipp Schmitt: Patogen bak piggtråd. I: Frankfurter Allgemeine Zeitung . 13. april 2007, s.9.
- S. Ahmad: Patogenese, immunologi og diagnose av latent Mycobacterium tuberculosis infeksjon . I: Klinisk og utviklingsimmunologi . Vol. 2011, 2011, s. 814943 , doi : 10.1155 / 2011/814943 , PMID 21234341 , PMC 3017943 (gratis fulltekst).
- K. Luong, LT Nguyen: Innvirkning av vitamin D i behandlingen av tuberkulose. I: Det amerikanske tidsskriftet medisinsk vitenskap. Bind 341, nr. 6, juni 2011, s. 493-498. doi: 10.1097 / MAJ.0b013e3182070f47 , PMID 21289501 . (Anmeldelse).
- SH Kaufmann: Fakta og fiksjon i tuberkulosevaksineforskning: 10 år senere. I: The Lancet Infectious Diseases . Volum 11, nr. 8, august 2011, s. 633-640. doi: 10.1016 / S1473-3099 (11) 70146-3 , PMID 21798463 . (Anmeldelse).
- M. Möller, EG Hoal: Nåværende funn, utfordringer og nye tilnærminger i human genetisk mottakelighet for tuberkulose. I: Tuberkulose. Volum 90, nr. 2, mars 2010, s. 71-83. doi: 10.1016 / j.tube.2010.02.002 , PMID 20206579 . (Anmeldelse).
- Thaddäus Zajaczkowski : Genitourinary tuberculosis: historisk og grunnleggende vitenskapelig gjennomgang: fortid og nåtid. I: Central European Journal of Urology, 65, 2012, s. 182-187.
- Urs Ehehalt: Tbc - vanlig over hele verden. I: Hamburger Ärzteblatt, 10/2014, s. 12–15.
- Rüdiger Döhler , Loukas Konstantinou: Skjelett tuberkulose - en av de eldste sykdommene i menneskeheten. I: Chirurgische Allgemeine , bind 16, utgave 10 (2015), s. 556–558.
- Isabelle Suárez et al.: Diagnose og terapi av tuberkulose. I: Deutsche Ärzteblatt. Volum 116, utgave 43, 25. oktober 2019, s. 729-735.
Kringkastingsrapport
- Claudia Doyle, Mathias Tertilt: Kamp mot tuberkulose i India - "Vi vil avslutte epidemien" , Deutschlandfunk - Vitenskap i fokus fra 11. februar 2018
weblenker
- Tuberkulose - Informasjon fra Robert Koch Institute
- Nettsted for det nasjonale referansesenteret for mykobakterier ved Borstel Research Center
- Nettsted for den tyske sentralkomiteen for bekjempelse av tuberkulose
- Bilder av tuberkulose cutis luposa endringer i DermIS
- Bilder av tuberkulose cutis verrucosa endringer i DermIS
- Bilder av tuberkulose Primaria Cutis Endringer i DermIS
- TB-spesifikk side. WHOs regionale kontor for Europa
- stoptb.org - Initiativ Stopp TB (engelsk) åpnet 8. november 2009
- Tuberkulose i Europa og Nord-Amerika, 1800-1922. Harvard University Library, Open Collections Program, Contagion, Historical Views of Diseases and Epidemics
- Tysk spedalskhet og tuberkulosehjelp e. V.
- Kompetansesenter tuberkulose (Sveits)
- German Lung Foundation
- Detaljert informasjon om tuberkulose hos HIV-pasienter
- Tuberkulose. Lungeninformationsdienst.de
- Tidsregistrering av det tyske tuberkulosearkivet (2009). (PDF)
- Carola Otterstedt: Barna til Scheidegg. (Rapporter fra et barnesanatorium for lunge- og bein tuberkulose, dokumentasjon).
- Tuberkulose - Informasjon fra Federal Office of Public Health (Sveits)
Merknader
- ↑ Tuberkulose anses å være en AIDS-definerende sykdom. Jörg Braun (2016), s. 462.
- ↑ Global tuberkuloserapport 2016. (PDF) WHO , s. 1 , åpnet 11. juni 2017 .
- ↑ Visste innvandrere bringer “White Death” for oss? News.de fra 10. november 2015.
- ^ Max Höfler: tysk bok med sykdomsnavn. München 1899, s. 93 og 99.
- ↑ Matthias Kreienkamp: St. Georgen Rezeptar. En alemannisk farmakopé fra 1300-tallet fra Karlsruhe Codex St. Georgen 73 , del II: Kommentar (A) og tekstlig sammenligning, medisinsk avhandling Würzburg 1992, s. 68 f.
- ↑ JT Lejeune, PJ Rajala-Schultz: Mattrygghet: upasteurisert melk: en fortsatt trussel mot folkehelsen. I: Kliniske smittsomme sykdommer . Volum 48, nummer 1, januar 2009, s. 93-100. doi: 10.1086 / 595007 . PMID 19053805 . (Anmeldelse).
- Act Faktablad tuberkulose. WHO, per oktober 2019; åpnet 31. desember 2019.
- ↑ V. Bordignon, p Bultrini u a:.. Høy forekomst av latent tuberkulose i autoimmune sykdommer: som psoriasis og i kroniske luftveissykdommer, Inkludert lungekreft. I: Tidsskrift for biologiske regulatorer og homeostatiske midler. Volum 25, nr. 2, apr-juni 2011, s. 213-220. PMID 21880210 .
- ^ Rapport om epidemiologi av tuberkulose i Tyskland for 2016. (PDF) (Ikke lenger tilgjengelig online.) Robert Koch Institute , 2018, s. 112 , tidligere i originalen ; åpnet 26. mars 2018 . ( Siden er ikke lenger tilgjengelig , søk i nettarkiver ) Info: Linken ble automatisk merket som defekt. Vennligst sjekk lenken i henhold til instruksjonene, og fjern deretter denne meldingen.
- ↑ Federal Gazette N ° 27, 10. juli 1947 (informasjon for 1940)
- ↑ HP Pöhn, G. Rasch: Statistikk for rapporteringspliktige sykdommer. BGA Schriften 5/1993, MMV Verlag, München, 1004.
- ^ Robert Koch Institute : Arkiv over rapporter om epidemiologi av tuberkulose i Tyskland (siden 2001). Hentet 13. november 2011 .
- ↑ a b c tuberkulose. RKI-guide for leger. Robert Koch Institute , åpnet 13. november 2011 .
- ↑ RKI-rapport om epidemiologi av tuberkulose i Tyskland for 2011. (PDF) Robert Koch Institute , åpnet 18. mars 2013 .
- ↑ Ikke helt klart for tuberkulose. I: Deutsches Ärzteblatt, 18. mars 2013.
- ↑ Epidemiologisk bulletin fra RKI nr. 3/2020 (PDF) 16. januar 2020
- ↑ A. Koul et al. Utfordringen med nye medikamentoppdagelse for tuberkulose . I: Natur . teip 469 , nr. 7331 , 2011, s. 483-490 , PMID 21270886 .
- ^ R. Riley: Luftformidling av lungetuberkulose . I: Am Rev Tuberc . teip 76 , nr. 5980 , 1957, s. 931-941 , PMID 13488004 .
- ↑ a b German Society for Pediatric Infectious Diseases V. (DGPI) (Red.): Håndbokinfeksjoner hos barn og ungdom. 4. utgave. Futuramed, München 2003, ISBN 3-923599-90-0 .
- ^ Walter Schaich: Tuberkulosen. 1961, s. 282 ( Tuberkuloma i lungene. ).
- L JL Flynn, MM Goldstein, J. Chan et al.: Tumornekrosefaktor-alfa er nødvendig i den beskyttende immunresponsen mot Mycobacterium tuberculosis hos mus . I: Immunitet . teip 2 , nei 6 , juni 1995, s. 561-572 , PMID 7540941 .
- ^ ST Cole et al.: Dechifrere biologien til Mycobacterium tuberculosis fra hele genomssekvensen. I: Natur . Nr. 393, London 1998, s. 537-554. PMID 9634230 .
- ^ Walter Schaich: Tuberkulosen. 1961, s. 251-254.
- ↑ a b T. Ulrichs et al.: Immunologi av tuberkulose og nye vaksinemetoder. I: Monthly Pediatrics. Nr. 154, Springer, Berlin 2006, ISSN 0026-9298 , s. 132-141.
- ^ Walter Schaich: Tuberkulosen. 1961, s. 233 f. Og 265 f.
- ↑ Berthold Jany, Tobias Welte: Pleural effusjon hos voksne - årsaker, diagnose og terapi. I: Deutsches Ärzteblatt. Volum 116, nr. 21, (mai) 2019, s. 377-385, her: s. 379-383.
- ↑ a b c K. Magdorf: Tuberkulose i barndommen. Patogenese, forebygging, klinikk og terapi. I: Monthly Pediatrics. Nr. 154, Springer, Berlin 2006, ISSN 0026-9298 , s. 124-132.
- ↑ Karl Wurm, AM Walter: Smittsomme sykdommer. 1961, s. 131.
- ↑ Karl Wurm, AM Walter: Smittsomme sykdommer. 1961, s. 131.
- ^ Walter Schaich: Tuberkulosen. 1961, s. 281 f.
- ↑ Ludwig Heilmeyer , Wolfgang Müller: De revmatiske sykdommene. I: Ludwig Heilmeyer (red.): Lærebok for indremedisin. Springer-Verlag, Berlin / Göttingen / Heidelberg 1955; 2. utgave, ibid. 1961, s. 309-351, her: s. 322.
- ^ A. Poncet: Polyarthrite tuberculeuse simulant des lésions rhumatismales chroniques déformantes. I: Gaz. Hôp. Volum 70, (Paris) 1897, s. 1219.
- ↑ Barbara I. Tshisuaka: Poncet, Antonin. I: Werner E. Gerabek , Bernhard D. Haage, Gundolf Keil , Wolfgang Wegner (red.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4 , s. 1175.
- ^ Walter Schaich: Tuberkulosen. 1961, s. 286-289.
- Ald Gerald Metz: Arkivet til Würzburg University Clinic for Skin and Venereal Diseases og dets beholdninger. I: Würzburg sykehistoriske rapporter. Volum 9, 1991, s. 37-55, her: s. 47, 50.
- ^ Walter Schaich: Tuberkulosen. 1961, s. 291 f.
- ↑ S. Jodra, C. Alvarez: Bilder i klinisk medisin. Potts sykdom i thorax-ryggraden. I: N Engl J Med. 368 (8), 2013, s. 756. doi: 10.1056 / NEJMicm1207442 . PMID 23425168 .
- Üd Rüdiger Döhler, Loukas Konstantinou: Skjelett tuberkulose - en av de eldste sykdommene i menneskeheten. I: Kirurgisk general. Volum 16, utgave 10 (2015), s. 556–558.
- ^ Walter Schaich: Tuberkulosen. 1961, s. 283-285.
- ^ Walter Schaich: Tuberkulosen. 1961, s. 289 f.
- ↑ A. Müller, RW Schlecht, Alexander Früh, H. Still Veien til helse: En trofast og uunnværlig guide for friske og det syke. 2 bind, (1901; 3. utgave 1906, 9. utgave 1921) 31. til 44. utgave. CA Weller, Berlin 1929 til 1931, bind 2 (1929), s. 266 f.
- ^ Walter Schaich: Tuberkulosen. 1961, s. 285 f.
- ↑ Ravikran Orgole: Textbook of Oral Medicine, Oral Diagnosis and Oral Radiology, Elsevier Health Services, 2014, s.215.
- ↑ a b A. Detjen et al.: Immunologisk diagnose av tuberkulose - interferon-γ-tester. I: Monthly Pediatrics. Nr. 154, Springer, Berlin 2006, ISSN 0026-9298 , s. 152-159.
- ↑ DD Singh, M. Vogel et al.: TB eller ikke TB? Vanskeligheter med diagnosen tuberkulose hos HIV-negative innvandrere til Tyskland. I: European journal of medical research. Volum 16, nr. 9, september 2011, s. 381-384. PMID 22024436 .
- ↑ Anbefalt tiltak for å håndtere pasienter med mistanke om tuberkulose ved GPR
- ↑ HJ Zar et al.: Indusert sputum versus gastrisk skylle for mikrobiologisk bekreftelse av lungetuberkulose hos spedbarn og små barn, en prospektiv studie. I: The Lancet. Vol. 365, nr. 9454, London 2005, s. 130-134. PMID 15639294 .
- ↑ M. Pwiwitzer et al.: Falskt positiv interferon-γ-test? I: Pneumologi. 2007.
- ↑ Nina Pollock et al.: Screening Health Care Workers with Quantiferon-Gold: Mulige falske negative resultater hos personer med høy pre-test sannsynlighet for latent tuberkuloseinfeksjon. I: Bryst. 2007.
- ↑ Matthew PR Berry, Christine M. Graham, Finlay W. McNab, Zhaohui Xu, Susannah AA Bloch et al. Et interferon-induserbart nøytrofil-drevet blod transkripsjonell signatur i human tuberkulose. I: Natur. Vol. 466, 19. august 2010, s. 973-977 ( abstrakt som html ).
- ↑ J. van INGEN, RE Aarnoutse et al. Hvorfor bruker vi 600 mg rifampicin i tuberkulosebehandlingen? I: Kliniske smittsomme sykdommer: en offisiell publikasjon av Infectious Diseases Society of America. Volum 52, nr. 9, mai 2011, s. E194 - e199. doi: 10.1093 / cid / cir184 , PMID 21467012 (anmeldelse).
- ↑ R. Tasneen, SY Li u a:.. Sterilisering aktivitet av nye TMC207- og PA-824-inneholdende regimer i en musemodell av tuberkulose. I: Antimikrobielle midler og cellegift . Volum 55, nr. 12, desember 2011, s. 5485-5492. doi: 10.1128 / AAC.05293-11 . PMID 21930883 . PMC 3232786 (fri fulltekst).
- ↑ Tuberkulose - brosjyre for leger. ( Memento fra 29. september 2007 i Internet Archive ) Robert Koch Institute
- ↑ Marianne Abele-Horn (2009), s. 239.
- ↑ M. Lee, J. Lee et al. Linezolid for behandling av kronisk omfattende resistent tuberkulose. I: The New England Journal of Medicine . Volum 367, nummer 16, oktober 2012, s. 1508-1518. doi: 10.1056 / NEJMoa1201964 . PMID 23075177 . PMC 3814175 (fri fulltekst).
- ^ S. Heinzl: Antibiotisk behandling av tuberkulose: Linezolid for svært resistente patogener. I: Dtsch Arztebl. 109 (49), 2012, s. A-2467 / B-2020 / C-1976.
- ^ FDAs rådgivende panel støtter J&J TB-medikament , Reuters, 29. november 2012.
- ↑ K. Williams, A. Minkowski et al.: Sterilisering aktiviteter av nye kombinasjoner som mangler første- og annenlinjemedikamenter i en murin modell av tuberkulose. I: Antimikrobielle midler og cellegift. Volum 56, nummer 6, juni 2012, s. 3114-3120. doi: 10.1128 / AAC.00384-12 . PMID 22470112 . PMC 3370712 (gratis fulltekst).
- ↑ Sammendrag av den europeiske offentlige vurderingsrapporten (EPAR) for Sirturo - Bedaquiline , EPAR for EMA, åpnet 7. april 2014.
- ↑ a b World TB Day - tre nye medisiner anbefalt i løpet av de siste seks månedene for pasienter med multiresistent tuberkulose , rapporterte EMA i anledning World TB Day 21. mars 2014, åpnet 7. april 2014.
- ↑ Deltyba - Delamanid , EMA-varsel i anledning CHMPs positive avstemning 21. november 2013, åpnet 7. april 2014.
- ↑ Para-aminosalicylsyre Lucane , EMA-varsling i anledning CHMPs positive avstemning 21. november 2013, tilgjengelig 7. april 2014.
- ↑ Sammendrag av den europeiske offentlige vurderingsrapporten (EPAR) for Deltyba delamanid , EPAR for EMA, tilgjengelig 22. mai 2014.
- ↑ Sammendrag av den europeiske offentlige vurderingsrapporten (EPAR) for Para-aminosalicylsyre Lucane , EPAR fra EMA, tilgjengelig 22. mai 2014.
- ↑ S. Yaldiz, S. Gursoy et al. Surgery tilbud høye herdehastigheter i multiresistent tuberkulose. I: Ann Thorac Cardiovasc Surg. Bind 17, nr. 2, april 2011, s. 143-147. PMID 21597410 .
- ↑ L. Amaral, A. Martins, G. Spengler, A. Hunyadi, J. Molnar: Den mekanisme ved hvilken den Fenotiazin Tioridazin bidrar til bedre Cure problematisk stoff resistente former av lungetuberkulose: Nylige patenter for "Ny bruk". I: Nylige patenter på oppdagelse av infeksjoner. [Elektronisk publisering før utskrift] Desember 2013, PMID 24320229 .
- ↑ L. Amaral, M. Viveiros: Hvorfor tioridazin i kombinasjon med antibiotika herder i stor utstrekning medikamentresistente Mycobacterium tuberculosis infeksjoner. I: Internasjonal journal over antimikrobielle midler. Volum 39, nummer 5, mai 2012, s. 376-380. doi: 10.1016 / j.ijantimicag.2012.01.012 . PMID 22445204 .
- Sh S. Sharma, A. Singh: Fenotiaziner som anti-tuberkulære midler: mekanistisk innsikt og kliniske implikasjoner. I: Ekspertuttalelse om undersøkelsesmedisiner Volum 20, nummer 12, desember 2011, s. 1665-1676. doi: 10.1517 / 13543784.2011.628657 . PMID 22014039 .
- ↑ K. Magdorf et al.: Tuberkulose. I: Retningslinjer for barn. München 2006, ISBN 3-437-22060-8 .
- ↑ T. Schön, J. Idh et al.: Virkninger av et næringstilskudd rik på arginin i pasienter med smøre positiv lungetuberkulose - en randomisert studie. I: Tuberkulose. Volum 91, nummer 5, september 2011, s. 370-377. doi: 10.1016 / j.tube.2011.06.002 . PMID 21813328 .
- ^ AP Ralph, PM Kelly, NM Anstey: L-arginin og vitamin D: nye tilleggsimmunoterapier i tuberkulose . I: Trender Microbiol. teip 16 , nr. 7. juli 2008, s. 336-344 , doi : 10.1016 / j.tim.2008.04.003 , PMID 18513971 .
- ^ LT Ho-Pham, ND Nguyen, TT Nguyen et al.: Assosiasjon mellom vitamin D-insuffisiens og tuberkulose i en vietnamesisk befolkning . I: BMC Infect. Dis . teip 10 , 2010, s. 306 , doi : 10.1186 / 1471-2334-10-306 , PMID 20973965 , PMC 2978214 (fri fulltekst).
- ↑ M. Fabri, S. Stenger et al.: D-vitamin er nødvendig for IFN-gamma-mediert antimikrobiell aktivitet av humane makrofager. I: Science Translational Medicine . Volum 3, nummer 104, oktober 2011, s. 104ra102. doi: 10.1126 / scitranslmed.3003045 . PMID 21998409 . PMC 3269210 (fri fulltekst).
- ↑ Tuberkulose: D-vitamin akselererer den antibiotiske virkningen. I: Deutsches Ärzteblatt. 5. september 2012.
- Co AK Coussens, RJ Wilkinson u a.: Vitamin D ACCELERERER oppløsning av inflammatoriske responser under tuberkulosebehandling. I: Proceedings of the National Academy of Sciences . Volum 109, nummer 38, september 2012, s. 15449-15454. doi: 10.1073 / pnas.1200072109 . PMID 22949664 . PMC 3458393 (fulltekst).
- ↑ S. Subbian, L. Tsenova et al.: Fosfodiesterase-4-hemming endrer genekspresjon og forbedrer isoniazid-mediert clearance av Mycobacterium tuberculosis i kanin lungene. I: PLOS patogener . Volum 7, nummer 9, september 2011, s. E1002262. doi: 10.1371 / journal.ppat.1002262 . PMID 21949656 . PMC 3174258 (fulltekst).
- ↑ KJ Welsh, SA Hwang et al.: Laktoferrin-modulering av mykobakteriell ledningsfaktor trehalose 6-6'-dimykolatindusert granulomatøs respons. I: Translasjonsforskning: tidsskriftet laboratorium og klinisk medisin. Volum 156, nummer 4, oktober 2010, s. 207-215. doi: 10.1016 / j.trsl.2010.06.001 . PMID 20875896 . PMC 2948024 (fri fulltekst).
- ^ McGill University: Den online TST / IGRA-tolk. Hentet 24. mars 2014 .
- ↑ P. Andersen, TM Doherty: Suksessen og svikt av BCG - implikasjoner for en ny tuberkulosevaksine. I: Naturomtaler. Mikrobiologi. Volum 3, nr. 8, august 2005, s. 656-662. doi: 10.1038 / nrmicro1211 , PMID 16012514 . (Anmeldelse).
- ^ BCG: dårlige nyheter fra India. I: Lancet. Volum 1, nummer 8159, januar 1980, s. 73-74. PMID 6101419 .
- ↑ L. Grode, CA Ganoza, C. Brohm, J. Weiner, B. Eisele, SH Kaufmann: sikkerhet og immunogenisitet av det rekombinante BCG vaksine VPM1002 i en fase en åpen, randomisert klinisk forsøk . I: Vaksine . 2012, doi : 10.1016 / j.vaksine.2012.12.053 , PMID 23290835 .
- ↑ MPG: Vaksinekandidat mot tuberkulose i fase II / III-studien
- ↑ MD Tameris, M. Hatherill, BS Landry, TJ Scriba, MA Snowden, S. Lockhart, JE Shea, JB McClain, GD Hussey, WA Hanekom, H. Mahomed, H. McShane: Sikkerhet og effekt av MVA85A, en ny tuberkulose vaksine, hos spedbarn som tidligere var vaksinert med BCG: en randomisert, placebokontrollert fase 2b-studie. I: The Lancet. doi: 10.1016 / S0140-6736 (13) 60177-4 .
- ↑ Aeras Utvikler nye tuberkulosevaksiner for hele verden
- ↑ JC Lorenzi, AP Trombone, CD Rocha et al.: Intranasal vaksinasjon med messenger RNA som en ny tilnærming i genterapi: bruk mot tuberkulose . I: BMC Biotechnol . teip 10 , 2010, s. 77 , doi : 10.1186 / 1472-6750-10-77 , PMID 20961459 , PMC 2972232 (fri fulltekst).
- ↑ Elisa Nemes, Hennie Geldenhuys, Virginie Rozot, Kathryn T. Rutkowski, Frances Ratangee: Forebygging av M. tuberculosis-infeksjon med H4: IC31 Vaksine eller BCG Revaksinasjon . I: New England Journal of Medicine . 11. juli 2018, doi : 10.1056 / NEJMoa1714021 , PMID 29996082 , PMC 5937161 (gratis fulltekst) - ( nejm.org [åpnet 21. desember 2018]).
- ↑ JT Belisle, VD Vissa, T Sievert, K Takayama, PJ Brennan, GS Besra: Rollen til hovedantigenet til Mycobacterium tuberculosis i celleveggbiogenese. I: Vitenskap . teip 276 , 1997, s. 1420-1422 .
- ↑ Tuberkulose: RKI-Ratgeber. Rapporteringsplikt i henhold til IfSG. I: rki.de. Robert Koch Institute, 21. februar 2013, åpnet 15. mars 2020 .
- ↑ Tuberkulose: RKI-Ratgeber. Meldingsplikt i henhold til IfSG. I: rki.de. Robert Koch Institute, 21. februar 2013, åpnet 15. mars 2020 .
- ↑ a b Varslingsdyresykdommer. Forbundsdepartementet for mat og jordbruk (BMEL), 2. august 2019, åpnet 16. mars 2020 .
- ↑ Notifiserbare dyresykdommer. Forbundsdepartementet for mat og jordbruk (BMEL), 2. august 2019, åpnet 14. mars 2020 .
- ↑ Hele lovlige regulering av tuberkuloseloven i den gjeldende versjonen.
- ↑ Swiss Federal Council: Animal Disease Ordinance (TSV). I: admin.ch. Hentet 16. mars 2020 (Swiss Standard German, fra 27. juni 1995 (fra 1. januar 2020)).
- ↑ Tuberkulose hos dyr og mennesker. Federal Food Safety and Veterinary Office FSVO, 10. mars 2010, åpnet 16. mars 2020 (Swiss Standard German): “Tuberkulose er en dyresykdom som må utryddes og derfor meldes. Alle som holder på eller passer på dyr, må rapportere mistenkte tilfeller til flokkdyrlegen. [...] "
- ^ TA Gous, MC Williams: Patologien til tuberkulose forårsaket av Mycobacterium tuberculosis i en flokk med semi-fritt springende bok (Antidorcas marsupialis) . I: Onderstepoort J. Vet. Res. Band 76 , nr. 4. desember 2009, s. 419-441 , PMID 21344792 .
- ^ R. Murphree, JV Warkentin et al.: Elephant-to-human transmission of tuberculosis, 2009. I: Emerging Infectious Diseases . Volum 17, nr. 3, mars 2011, s. 366-371. PMID 21392425 .
- ↑ Forordning om meldepliktige dyresykdommer i versjonen publisert 19. juli 2011 ( Federal Law Gazette I s. 1404 ), endret ved artikkel 3 i forordningen av 3. mai 2016 ( Federal Law Gazette I s. 1057 )
- ↑ Notifiserbare dyresykdommer på nettstedet til Federal Ministry of Food and Agriculture, åpnet 19. mars 2020
- ↑ Vedlegg til avsnitt 1 i forordningen om meldepliktsdyresykdommer (TKrMeldpflV) i versjonen publisert 11. februar 2011 ( Federal Law Gazette I s. 252 ), sist endret ved artikkel 381 i forordningen 31. august 2015 ( Federal Law Gazette I s. 1474 )
- ↑ Chemical and Veterinary Investigation Office (CVUA) Stuttgart: Pseudotuberculosis (Corynebacterium pseudotuberculosis) infeksjoner øker.
- ↑ J. Kappelman, MC Alçiçek et al. Først Homo erectus fra Tyrkia og implikasjoner for vandringer i tempererte Eurasia. I: Amerikansk journal for fysisk antropologi. Volum 135, nr. 1, januar 2008, s. 110-116. doi: 10.1002 / ajpa.20739 , PMID 18067194 .
- ↑ Stefan Weller: Eldste bevis på tuberkulose hos mennesker? Universitätsmedizin Göttingen - Georg-August-Universität, pressemelding fra 23. april 2012 på Informationsdienst Wissenschaft (idw-online.de), tilgjengelig 20. desember 2014.
- ↑ I. Hershkovitz, HD Donoghue et al.: Påvisning og molekylær karakterisering av 9000 år gamle Mycobacterium tuberculosis fra en neolitisk bosetning i det østlige Middelhavet. I: PloS en. Volum 3, nr. 10, 2008, s. E3426. doi: 10.1371 / journal.pone.0003426 , PMID 18923677 . PMC 2565837 (fri fulltekst).
- ↑ Bruce M. Rothschild, Larry D. Martin, Galit Lev, Helen Bercovier, Gila Kahila Bar-Gal, Charles Greenblatt, Helen Donoghue, Mark Spigelman, David Brittain: Mycobacterium tuberculosis Complex DNA from an Extinct Bison datert 17.000 år før nåtiden. I: Clin Infect Dis. 33 (3), 2001, s. 305-311. doi: 10.1086 / 321886 .
- ^ Evert Dirk Baumann : De phthisi antiqua. I: Janus 34, 1930, s. 209-225 og 253-272.
- ↑ Hippokrates: Epidemier.
- ↑ Walter von Brunn : Paracelsus og hans forbruksteori. Leipzig 1941.
- ↑ Martin Risch: Dødsårsaksstatistikk for samfunnet Triesen fra 1831 til 1930 . I: Årbok for den historiske foreningen for fyrstedømmet Liechtenstein . teip 36 , 1936, s. 54 .
- ↑ Christoph Weißer: Brystkirurgi. I: Werner E. Gerabek , Bernhard D. Haage, Gundolf Keil , Wolfgang Wegner (red.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4 , s. 1397.
- ↑ Om kollapsbehandling av lungetuberkulose, se også Walter Schaich: Die Tuberkulose. 1961, s. 305-307.
- ↑ Barbara I. Tshisuaka: Tuffier, Théodore. I: Werner E. Gerabek , Bernhard D. Haage, Gundolf Keil , Wolfgang Wegner (red.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4 , s. 1424.
- ↑ Albrecht Scholz: Lupus vulgaris. I: Werner E. Gerabek , Bernhard D. Haage, Gundolf Keil , Wolfgang Wegner (red.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4 , s. 872 f., Her: s. 873.
- ^ Ferdinand Sauerbruch, Hans Rudolf Berndorff : Det var livet mitt. Kindler & Schiermeyer, Bad Wörishofen 1951; sitert: Lisensiert utgave for Bertelsmann Lesering, Gütersloh 1956, s. 180–286.
- ↑ Jf. Om virksomheten til kommunesamlingen av kilder om tysk sosialpolitikk 1867 til 1914 , III. Avdeling: Utvidelse og differensiering av sosialpolitikk siden begynnelsen av det nye kurset (1890–1904), bind 7, Poor Care and Communal Welfare Policy , redigert av Wilfried Rudloff, Darmstadt 2016.
- ↑ Md Abdul kuddus, Emma S. McBryde, Oyelola A. Adegboye: Forsinkelse effekt og byrden av vær-relaterte tuberkulosetilfeller provinsen i Rajshahi, Bangladesh, 2007-2012 . I: Vitenskapelige rapporter . teip 9 , nr. 1 , 3. september 2019, ISSN 2045-2322 , s. 12720 , doi : 10.1038 / s41598-019-49135-8 ( nature.com [åpnet 19. september 2020]).
- ↑ tb-archiv.de
- ↑ Eckart Roloff , Karin Henke-Wendt: Gammel sykdom med nye problemer. (Det tyske tuberkulosearkivet og -museet) I: Besøk legen din eller apoteket. En tur gjennom Tysklands museer for medisin og farmasi. Volum 2: Sør-Tyskland. Verlag S. Hirzel, Stuttgart 2015, ISBN 978-3-7776-2511-9 , s. 51-53.
- ↑ Stop TB partnerskapet. De savnede tre millionene. Kunngjøring for verdens tuberkulosedag 24. mars 2014; Hentet 8. april 2014.