T-lymfocytt
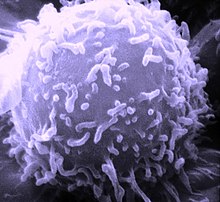
T-lymfocytter, eller kort fortalt T-celler , danner en gruppe hvite blodlegemer som brukes til immunforsvar . T-lymfocytter, sammen med B-lymfocytter, representerer den ervervede (adaptive) immunresponsen . T i navnet står for thymus der cellene modnes.
Som alle blodceller blir T-celler laget i beinmargen . Derfra vandrer de inn i thymus, der MHC- reseptorer dannes på overflaten. Gjennom et første positivt utvalg, etterfulgt av et negativt utvalg , avvises alle de som reagerer på kroppens egne proteiner eller som ikke kan gjenkjenne kroppens egne MHC-reseptorer. De resterende, gjenværende T-celler kan deretter bare gjenkjenne eksogene antigener og således ikke bekjempe kroppen selv Proteinene i de utvalgte cellemembraner, også kalt. T-cellereseptorer (TCR), kan deretter - i likhet med de av B-lymfocytter antistoffer produsert - gjenkjenne eksogene stoffer. I motsetning til antistoffer gjenkjenner T-celler imidlertid bare fremmede stoffer hvis antigenene er bundet til deres MHC på overflaten av andre celler. Frie antigener er kun gjenkjennes av T-lymfocytter når de blir aktivt vist med så - som kalles antigenpresenterende - -presenterende celler (såkalt MHC restriksjons).
funksjon
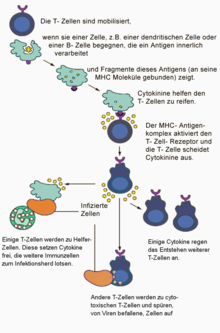
T-celler vandrer gjennom organismen og overvåker kontinuerlig membransammensetningen i kroppens celler for patologiske endringer. Utenlandske eller forandrede stoffer på celleoverflaten kan for eksempel være forårsaket av en virusinfeksjon eller av en mutasjon av genetisk materiale. Hvis en av de presenterte MHC-I- eller MHC-II-molekylene på overflaten av den syke cellen nøyaktig samsvarer med den individuelle reseptoren til en passerende T-celle som en nøkkel i den tilhørende låsen, og hvis den samtidig er en kostimulant ( f.eks. protein B7-1 ) presenteres, går T-cellen i aktivert tilstand ved å aktivere visse gener i cellekjernen . Antigenreseptor og ko-reseptor danner sammen aktiveringssignalet. Cellen vokser og skiller seg ut i effektor- og minneceller . Avhengig av celletype har effektorcellene forskjellige funksjoner. Killer T-celler (identifisert av CD8-reseptoren ) ødelegger den syke cellen direkte; T-hjelperceller (med CD4-reseptor ) utløser alarm med løselige messenger-stoffer ( cytokiner ) og tiltrekker seg flere immunceller. Regulatoriske T-celler forhindrer overdreven angrep på intakte kroppsceller, slik at de hjelper med selvtoleranse . T-celler er derfor ansvarlige for celleformidlet cytotoksisitet , for å kontrollere den humorale immunresponsen og sist men ikke minst for mange allergiske reaksjoner . Styrken til de forskjellige reaksjonene avhenger av det stimulerende antigenet, typen presentasjonscelle og andre, i noen tilfeller fremdeles ukjente faktorer.
I thymus, et lymfatisk organ , blir de nye T-cellene forberedt for deres forskjellige funksjoner. En klassifisering kan gjøres på grunnlag av overflateantigenene CD4 og CD8: CD4 + T-lymfocytter betraktes som hjelperceller; deres reseptor gjenkjenner MHC klasse II-molekyler. CD8 + T-lymfocytter regnes som cytotoksiske T-celler; deres reseptor gjenkjenner antigener som presenteres av nesten alle kroppsceller via MHC klasse I-molekyler. Faktisk representerer den bare den vanligste kombinasjonen av T- cellefenotype og funksjon; det er også CD4 + cytotoksiske T-celler og CD8 + T-hjelperceller. CD4 + T-celler finnes hovedsakelig i perifert blod og i lymfevev med høy blodstrøm, slik som parafollikulære regioner i lymfeknuter , milt og mandler . I motsetning til det er CD8 + T-celler mer sannsynlig å bli funnet i beinmargen og i lymfevevet i mage- tarmslimhinnen , luftveiene og urinveiene .
Naive (ikke aktivert) T-celler beveger seg konstant mellom blodet og disse lymfoide vevene. For dette formålet har de liten amoeboid mobilitet og er utstyrt med celleadhesjonsmolekyler og reseptorer for kjemokiner . De forlater blodstrømmen ved hjelp av diapedesis gjennom veggene i postcapillary venules. Derfra vandrer de gjennom vevet og kommer tilbake til blodet med lymfen via thoraxkanalen , som åpner seg i venstre venehjørne. En annen mulighet er at lymfocyttene vandrer gjennom veggene i et høyt endotelvenol (HEV) inn i et sekundært lymfatisk organ.
Spesielle funksjoner til T-lymfocyttene
Immunceller spiller en viktig rolle i å kontrollere beinmetabolismen. De kan frigjøre stoffer som fremmer nedbrytningen av beinmatrisen av osteoklaster . Under østrogenmangel hos mus var T-lymfocytter stimulert for produksjon av TNF-α og RANKL ; dette kunne ha bidratt til utviklingen av tap av beinmineraler hos testdyrene. Thymus-mindre mus som eggstokkene var fjernet fra, led ikke tap av bein til tross for hormonmangel. I atymiske nakne mus og rotter, er den hastigheten for benomsetning som generelt er lavere. Osteoprotegerin fra aktiverte T-lymfocytter stimulerer osteoklastisk nedbrytning av beinstoffet og kan være involvert i utviklingen av bein- og leddsykdommer .
Struktur og differensiering av relaterte celletyper
T- og B-lymfocytter er sfæriske celler av samme størrelse som røde blodlegemer ; deres diameter hos mennesker er omtrent 7,5 um. De kan ikke skilles fra hverandre mikroskopisk eller elektron mikroskopisk. Bare ved hjelp av immunhistokjemi kan markørproteiner som CD3 , som er karakteristisk for T-lymfocytter, og CD19 , som er spesifikt for B-lymfocytter , være representert. Den kromatin i den runde eller svakt innskåret, ikke-fliket cellekjernen er tett, klumpet og levende farget. Den plasma kant rundt kjernen er smal og kan neppe ses med et lysmikroskop . De mange lysosomene kan sees på som azurofile granuler. Cellestoffet inneholder rikelig med frie ribosomer . Den Golgi-apparatet er mindre enn den for de retikulære celler.
T-celle-antigenreseptoren (TCR)
Hver TCR på perifere T-celler er bundet til et CD3-reseptormolekyl . CD3-reseptoren leder aktiveringssignalet inn i celleinteriøret. Den binder seg til både TCRαβ og TCRγδ. Omfanget av reaksjonen av reseptoren med antigen-MHC-kompleksene avhenger av konsentrasjonen av begge partnere, dvs. H. dens tetthet på involverte cellemembraner, og den spesifikke affiniteten til TCR. Med krystallografien ble den tredimensjonale strukturen til TCR belyst. Den antigenbindende, hypervariable V-regionen ligner det tilsvarende V-domenet av antistoffer. Disse molekylsegmentene i form av eksponerte sløyfer bestemmer reseptorens antigenspesifisitet og kalles også komplementaritetsbestemmende regioner CDR.
Som antigenreseptoren til B-lymfocyttene, tilhører TCR immunoglobulingenet superfamilien. To av fire mulige proteinkjeder (betegnet med α, β, γ, δ) er forbundet via disulfidbroer . Vanligvis er TCR en αβ-heterodimer, sjeldnere en γδ-heterodimer. Så to subpopulasjoner av T-celler kan skilles ut. Α-kjedene veier 43–49 kilodalton , β-kjedene 38–44 kilodalton , γ-kjedene 55–60 og δ-kjedene ca. 40 kilodalton. Ved 15 nm er komplekset av reseptor og MHC lite sammenlignet med andre membranproteiner. Genene for α- og δ-kjedene er nestet på samme gensted på kromosom 14q11-12, γ-kjedegenet er på kromosom 7p15 og β-kjedegenet på kromosom 7q32-35. Arrangementet av genene gjør det ikke mulig for en celle å utvikle reseptorer samtidig som γδ og αβ heterodimerer.
I blodet og i lymfeorganene tilhører 95–98% av T-cellene αβ-subpopulasjonen. CD4 + og CD8 + T-celler er en del av det. γδ-T-celler er overveiende (opptil 50%) å finne i epitelvev slik som huden, tarmslimhinnen eller kjønnsorganene , dvs. på overflaten av kroppen.
Lavere former
Mens T-cellene på 1980-tallet ble delt inn i de to formene T-hjelper ( CD4 +) og T-suppressorceller ( CD8 +), vet vi nå den høye "plastisiteten" av T-celler, som er delt inn i andre Endre undertyper eller utvikle egenskaper ved flere undertyper, avhengig av oppløselige mediatorer, og som kan produsere cytokiner og interleukiner som er spesifikke for undertypen. Undertyper er f.eks. B. T1, T2, T9 eller T17.
T-hjelperceller
T-celler med en hjelperfunksjon skiller ut forskjellige cytokiner og kan klassifiseres i henhold til om disse messenger-stoffene er involvert i den celleformidlede immunresponsen, eller om B-lymfocyttenes humorale immunrespons stimuleres. Tilstedeværelsen av IL-12 og interferon -y (IFN-y) induserer differensiering til TH1-cellen, mens IL-4 og IL-6 fremmer differensiering til TH2-cellen. For eksempel tilhører CD4 + lymfocytter den første gruppen (type 1) som utskiller interferon-γ (IFN-γ), IL-2 og TNF-α . CD4 + lymfocytter, som produserer cytokinene IL-4 , IL-5 , IL-6 , IL-10 og IL-13 , er klassifisert som type 2. Det samme skillet kan også gjøres for utskillelse av CD8 + T-celler og for de med en γδ T-celle-antigenreseptor. Det er også T-hjelperceller med et blandet cytokinmønster kalt Type0 T-celler.
Forskjellene mellom type 1 T-celler og type 2 T-celler ble først beskrevet av Tim Mosmann i 1986 .
Cytotoksiske T-celler
De cytotoksiske T-celler (CTL, foreldet dreperceller ), er vanligvis kjennetegnet ved CD8 + -αβ heterodimerer på overflaten. De gjenkjenner antigener presentert på MHC-I-molekyler, spesielt viralt infiserte celler og tumorceller. CTL utløser programmert celledød i de defekte cellene via deres fysiologiske signalveier (Fas / FasL ; Perforin / Granzyme ).
Regulatoriske T-celler (T Reg )
Intensiteten av immunresponsen må overvåkes konstant, på den ene siden for å ødelegge kreftcellene og patogenene , men på den andre siden for å undertrykke autoimmunitet mot normalt vev. I tillegg må etterproduksjonen og modningen av leukocyttene holdes konstant. En del av kontrollmekanismene utøves av regulatoriske T-celler (foreldede suppressor T-celler ): via cytokiner som IL-10 og TGF-β , gjennom fangst av antigener, vekst og differensieringsfaktorer, gjennom CTLA4-mediert begrensning av klonal ekspansjon ved B-celler, og ved å drepe overflødige T-celler via Fas / FasL-medierte signaler. De regulatoriske T-celler er ytterligere oppdelt på grunnlag av deres cytokinprofiler, for eksempel i (CD4 + -CD25 + T-reg-celler, T R 1-celler, T H 3 lymfocytter og NKT-celler, CD8 + regulatoriske celler).
T-minneceller
Minne-T-celler danner et slags "immunologisk minne" ved å forbli i blodet etter at de har blitt aktivert. Hvis det samme patogenet smittes igjen, blir den opprinnelige aktiveringen gjenopprettet. Tilstedeværelsen av minneceller øker multiplikasjonen av antigenspesifikke T-celler med 10 til 100 ganger. Hukommelsesrollen kan utøves av både CD4 + og CD8 + T-minneceller.
NK T-celler
De naturlige drapsmannens T-celler er et lite antall cytotoksiske αβ T-celler som ikke har antigenspesifikke reseptorer, men som fremdeles kan gjenkjenne presentasjonen av MHC-I-antigenkomplekser. De er T-celler, så du bør ikke forveksle dem med de naturlige drapscellene i det uspesifikke immunsystemet på dette tidspunktet . NK-T-celler er preget av molekylet NKR-P1A , et lektinlignende protein, på overflaten. Ytterligere markører uttrykt av NK-celler er CD56 , Neural celladhesion molecule-1 (NCAM-1) og CD57 . Disse cellene produserer også de cytotoksiske effektormolekylene perforin og granzym. Oppgaven til NK-T-cellene er å være i kontrollen av autoimmune sykdommer.
γδ antigenreseptor positive T-lymfocytter
γδ T-celler utgjør bare en liten prosentandel av T-cellene i blod og lymfoide organer, men er veldig fremtredende i huden og i mange epitelvev. Dens essensielle trekk er en T-celle reseptor, som består av γ og δ underenhetene. Γδ TCR er betydelig mindre variert enn αβ TCR; bare noen få av de mange teoretisk mulige kombinasjonene av de forskjellige gensegmentene blir brukt. Bindingspartnerne til γδ TCR er fortsatt stort sett ukjente, men det er sannsynligvis hovedsakelig kroppens egne molekyler (αβ TCR gjenkjenner vanligvis antigenene til patogener).
Når det gjelder utvikling og funksjon, skiller γδ T-celler seg betydelig fra αβ T-celler. De forlater thymus i en forhåndsaktivert tilstand, som muliggjør en rask reaksjon og rask frigjøring av aktive stoffer. Aktivering kan trolig også finne sted uavhengig av γδ TCR av cytokiner. γδ T-celler gjenkjenner vevsskader og endringer (for eksempel kreft) og aktiverer deretter både medfødte og ervervede komponenter i immunsystemet.
T-lymfocyttbundne sykdommer
Medfødte immundefekter
Arvet immunsvikt som påvirker både T-celler og B-celler, dvs. H. som skader den cellulære og humorale immunresponsen kalles alvorlig kombinert immunsvikt (SCID). De berørte barna må ivaretas i et miljø med så få bakterier som mulig og har bare en sjanse til å overleve på lang sikt etter en vellykket benmargstransplantasjon .
Den DiGeorge syndrom hindrer utvikling av epitelvev i thymus av fosteret. Som et resultat kan ikke T-cellene modnes, og den cellulære immunresponsen reduseres kraftig.
Pasienter med naken lymfocyttsyndrom utvikler leukocytter og thymusceller uten MHC-II-molekyler og dermed mangel på CD4 + T-lymfocytter.
Ervervet immunmangel
Ervervet immunsvikt kan være forårsaket av ulike sykdommer, underernæring, miljøskadelige effekter eller terapeutiske tiltak.
Infeksjoner
Det humane immunsviktvirus (HIV) infiserer CD4 + T-lymfocytter, dendrittiske celler og makrofager, som fører til immunsvikt sykdommen AIDS . Virusene HTLV I og HTLV II kan angripe T-lymfocytter hos mennesker og primater og forårsake forskjellige sykdommer, inkludert T-celle leukemi hos voksne og tropisk spastisk paraparese .
Allergisk reaksjon
En overfølsomhetsreaksjon , eller spesifikk allergi , er når en upassende immunreaksjon utløses mot kroppens eget vev eller mot et faktisk ufarlig antigen (støv, pollen , mat eller medisin). Blant de fire typene i henhold til Coombs og Gell er T-celler hovedsakelig involvert i type I (umiddelbar type) og type IV (forsinket type). I umiddelbar typen, en overdreven T 2 blir reaksjonene indikert, i tilfelle av forsinket allergi en vedvarende overdreven aktivitet av T 1 cellene og således vedvarende inflammasjon.
Autoimmune sykdommer
Autoimmune sykdommer er kroniske sykdommer forårsaket av immunreaksjoner mot kroppens egne antigener. For eksempel ved diabetes mellitus type I er det observert at insulinspesifikke CD8 + T-celler angriper β-celler i bukspyttkjertelen . Selv med revmatoid artritt er det påvist autoreaktive T-celler. I følge den utbredte teorien om multippel sklerose , initieres denne sykdommen også av aktiverte T- celler som ødelegger myelinhylsene til nerveceller .
Legemiddeleffekter
Visse medikamenter kan forårsake ønskelige og uønskede immunmangel. Etter organtransplantasjon er det en risiko for transplantatavstøting, som innebærer både cellulære og humorale immunreaksjoner. Fokuset er på T-cellereaksjonen mot allogene og xenogene MHC-molekyler i fremmed vev. Studier viser tre mekanismer: akutt avvisning av CD8 + T-celler, kronisk avvisning av CD4 + T-celler, og skade på blodkarene som leverer transplantasjonen. Alle tre mekanismene kan undertrykkes permanent av immunsuppressive medisiner. Veksthemmende, celledrepende medisiner som cytostatika og stråling med ioniserende stråling kan også skade hvite blodlegemer og spesielt T-lymfocytter.
Onkologiske sykdomsmønstre
Degenererte T-celler er utgangspunktet for en gruppe tumorsykdommer ( ondartede lymfomer ) og akutt lymfoblastisk leukemi , som ofte rammer pasienter i barndommen.
Forekomsten av T-lymfocytter i andre levende ting
Hos virvelløse dyr (som protozoer , svamper , annelider og leddyr ) er det verken lymfocytter eller lymfeknuter. Hos virveldyr vises lymfeknuter bare hos fugler og pattedyr , mens lymfocytter er mer til stede i slektstreet i brusk og beinfisk, så vel som amfibier og reptiler .
Forskningshistorie
På begynnelsen av det 20. århundre var temaet for vitenskapelig debatt om noen menneskers immunitet mot infeksjon er basert på cellulære eller humorale prosesser. Zoologen Elias Metschnikow (1845–1916) observerte at mobile celler akkumulerte rundt en torn som ble stukket i en sjøstjerne . Metschnikow antok at disse cellene spiser inntrengende bakterier ( fagocytoseteori ). I kontrast, lærde som Emil Adolf von Behring (1854–1917) anså at immunitet genereres av stoffer oppløst i blodserum . I 1888 fant Bering at multiplikasjonen av miltbrannbakterier ble forhindret av serum fra resistente rotter, men ikke av serum fra marsvin som var utsatt for miltbrann. Bare serumet til de marsvinene som tidligere hadde blitt smittet med denne kimen, var effektivt mot Vibrio metschnikovii , og serumet deres var i sin tur ikke effektivt mot andre bakterier. Med dette klarte Behring også å tilbakevise Hans Buchner , som hadde trodd at blodserumet hadde en uspesifikk bakteriedrepende aktivitet. Sammen med Kitasato utviklet Behring sin teori om humoristisk immunitet og den såkalte "blodserumterapi".
Belgiske forskere (Denys, Lecleff og Marchand ), men spesielt Almroth Wright og SR Douglas, var i stand til å løse den tilsynelatende motsetningen mellom de to teoriene rundt 1903. Wright og Douglas fant fagocytosefremmende stoffer i serumet, som de kalte opsoniner - dagens antistoffer - som koblet cellulære og humorale prosesser. I henhold til instruksjonsteorien publisert av Linus Pauling i 1940 , dannet antigener en instruksjon der blodceller omdanner et universelt immunprotein til et passende spesifikt antistoff.
Avvik fra dette, Niels Jerne ( kloneutvalgsteori ) og Paul Ehrlich ( sidekjedeteori ) anså at alle immunglobuliner allerede var forhåndsdannet, og at den riktige ble valgt av det introduserte antigenet. Frank MacFarlane Burnet anerkjente da at det ikke var de sirkulerende antistoffene som ble valgt, men individuelle immunkompetente celler, som deretter multipliserte for å danne en spesifikt produserende klon ( Nobelprisen 1960). I løpet av fosterlivet gir somatiske mutasjoner utallige varianter av mulige antigenreseptorer; samtidig blir de cellene som bærer reseptorer for kroppens egne antigener eliminert igjen.
I 1926 ble lymfocyttenes rolle i avvisning av eksogent vev anerkjent. Gowans beskrev i 1964 at slike lymfocytter er tilgjengelige overalt, ettersom de bytter fra brystkanalen til blodet og deretter tilbake i vevet via sekundære lymfeorganer. Den spesielle betydningen av thymus ble oppdaget hos leukemiske mus i 1968. På midten av 1960-tallet ble det skilt mellom B- og T-lymfocytter. Jerne beskrev deres interaksjon i antistoffproduksjon i 1974 (Nobelprisen 1984). I 1975 differensierte Kisielow og kolleger cytotoksiske fra ikke-cytotoksiske T-celler. I 1976 viste Rolf Zinkernagel og Peter Doherty at T-cellen bare aktiveres når det utløsende antigenet presenteres ved MHC. I 1982 var det mulig å syntetisere et mAb som gjenkjente T-celle lymfomceller hos mus. Overflatestrukturene og TCRene til T-celler er blitt beskrevet mer detaljert ved bruk av T-celle- hybridomer og leukemiske T-cellelinjer. I 1979 fant Kung CD3-proteinene på siden av T-celle-antigenreseptoren; deres biokjemiske karakterisering fulgt i 1984 av en forskergruppe fra Cox Terhorst.
T-celle-reseptoren ble beskrevet i 1983 i mus som en 45-50 kDa heterodimer med en a- og en P-kjede. Året etter var mRNA- isolasjonen av den humane TCR også vellykket, for første gang ved hjelp av kloning av β-kjeder av humane TCRer og mus. Noen år senere ble det funnet en andre TCR som ligner αβ TCR - γδ T-celle-antigenreseptoren. MHC-begrensningen av T-celle-antigenreseptoren ble også beskrevet for første gang i 1986. TCR-gener kan være involvert i kromosomale mutasjoner som aktiverer kreftfremmende onkogener . Ved hjelp av molekylære prøver fra TCR, kunne gener identifiseres som spiller en rolle i utviklingen av leukemi og lymfom. 1988–1989 ble det vist at CD8 er den mottakelige partneren for de antigenene som presenteres på MHC-I. Hukommelsen til CD4- og CD8-celler er beskrevet.
litteratur
- GA Holländer: Immunologi, grunnleggende for klinikker og praksis . 1. utgave. Elsevier, München 2006, ISBN 3-437-21301-6 .
- MJ Owen, JR Lamb: Immun Recognition . Thieme, Stuttgart 1991, ISBN 3-13-754101-8 .
- I. Jahn: biologihistorie, teorier, metoder, institusjoner, korte bibliografier . 3. Utgave. Gustav Fischer, Jena 1998, ISBN 3-437-35010-2 .
- A. Wollmar, T. Dingermann: Immunologi, grunnleggende og aktive ingredienser . Med samarbeid fra I. Zündorf. Vitenskapelig forlag, Stuttgart 2005, ISBN 3-8047-2189-3 .
- O. Bucher, H. Wartenberg: Cytologi, histologi og mikroskopisk menneskelig anatomi . 11. utgave. Hans Huber, Bern / Stuttgart / Toronto 1992, ISBN 3-456-81803-3 .
- K. Munk: Grunnleggende studier i biologi og zoologi . Gustav Fischer, Heidelberg / Berlin 2002, ISBN 3-8274-0908-X .
weblenker
- uni-tuebingen. de / Liste / Liste01. aspx? subject = Immunobiology Lecture Immunobiology of T lymphocytes Videoopptak av et foredrag. Fra TIMMS, Tübingen Internet Multimedia Server ved Universitetet i Tübingen .
Individuelle bevis
- ↑ YY Kong, H. Yoshida, I. Sarosi, HL Tan, E. Timms, C. Capparelli, S. Morony, AJ Oliveira-DOS-Santos, G. Van A. Itie, W. Khoo, A. Wakeham, CR Dunstan, DL Lacey, TW Mak, WJ Boyle, JM Penninger: OPGL er en nøkkelregulator for osteoklastogenese, lymfocyttutvikling og organogenese av lymfeknuter . I: Natur . teip 397 , nr. 6717 , 28. januar 1999, s. 315-323 , PMID 9950424 .
- ^ S. Cenci, MN Weitzmann, C. Roggia, N. Namba, D. Novack, J. Woodring, R. Pacifici: Østrogenmangel induserer bentap ved å forbedre T-celleproduksjon av TNF-alfa . I: Journal of Clinical Investigation . teip 106 , nr. 10. november 2000, s. 1229-1237 , PMID 11086024 .
- ↑ M. Girardi: Immunosurveillance og immunregulering av yS T-celler . I: J. of Investigative Dermatology . Nei. 126 , 2006, s. 25-31 , PMID 16417214 .
- ↑ Stefanie Sarantopoulos: Allogen stamcelletransplantasjon - en T-celle balanserende ACT. I: New England Journal of Medicine . Volum 378, utgave 5, 1. februar 2018, s. 480-482; doi: 10.1056 / NEJMcibr1713238
- ↑ Tim Mosmann, H. Cherwinski, MW Bond, MA Giedlin, RL Coffman: To typer murine hjelper T-celle klone. I. Definisjon i henhold til profiler av lymfokinaktiviteter og utskilte proteiner . I: Journal of Immunology . teip 136 , nr. 7 , 1986, s. 2348-2357 ( jimmunol. Org / cgi / content / abstract / 136/7/2348 abstract ).
- ^ M. Bonneville, RL O'Brien, WK Født: Gammadelta T-celleeffektorfunksjoner: en blanding av medfødt programmering og ervervet plastisitet. . I: Nat. Pastor Immunol. . teip 10 , 2010, s. 467-478 , PMID 20539306 .
- ↑ AC Hayday: Gammadelta T-celler og responsen til lymfoid stressovervåking. . I: Immunitet . teip 31. 2009, s. 184-196 , PMID 19699170 .
- Y György Nagy, Joanna M. Clark, Edit Buzas, Claire Gorman, Maria Pasztoi, Agnes Koncz, András Falus og Andrew P. Cope: Nitrogenoksidproduksjon av T-lymfocytter økes i revmatoid artritt . I: Immunologi Letters . teip 118 , nr. 1 , 2008, s. 55-58 , doi : 10.1016 / j.imlet.2008.02.009 .
- ↑ JB Murphy: Studier i vevsspesifisitet: II. Den ultimate skjebnen til pattedyrsvev implantert i kyllingembryo . I: Journal of Experimental Medicine . Nei. 19 , 1914, s. 181-186 .
- ↑ JB Murphy: Faktorer for motstand mot heteroplastisk vevtransplantasjon: studier i vevsspesifisitet III . I: Journal of Experimental Medicine . Nei. 19 , 1914, s. 513-522 .
- ↑ JL Gowans, EJ Knight: Ruten for sirkulasjon av lymfocytter i rotten . I: Proc. R. Soc. Lond. B. Biol. Sci. . Nei. 159 , 1964, s. 257-282 , PMID 14114163 .
- ^ JF Miller: Immunologisk funksjon av thymus . I: Lancet . Nei. 2 , 1968, s. 748-749 .
- ↑ P. Kisielow, JA Hisrst, H. Shiku, PC Beverley, MK Hoffman, EA Boyse, HF Ottgen: Ly antigener som markører for funksjonelt forskjellige subpopulasjoner av thymus-avledede lymfocytter fra mus . I: Natur . Nei. 253 , 1975, s. 219-220 , PMID 234178 .
- ↑ H. Shiku, P. Kisielow, MA Bean, T. Takahashi, EA Boyse, HF Ottgen, LJ Old: Ekspresjon av T-celledifferensieringsantigener på effektorceller i celleformidlet cytotoksisitet in vitro . I: Journal of Experimental Medicine . Nei. 141 , 1975, s. 227-241 , PMID 1078839 .
- Z RM Zinkernagel, PC Doherty: Begrensning av in vitro T-celleformidlet cytotoksisitet ved lymfocytisk koriomeningitt i et syngenisk eller semiallogent system . I: Natur . Nei. 248 , 1974, s. 701-702 , PMID 4133807 .
- ^ JP Allison, BW McIntyre, D. Bloch: Tumorspesifikt antigen av murint T-lymfom definert med monoklonalt antistoff . I: J. Immunol. . Nei. 129 , 1982, s. 2293-2300 , PMID 15661866 .
- ↑ LE Samelson, RN Germain, RH Schwatz: Monoklonale antistoffer mot antigenreseptoren på en klonet T-cellehybrid . I: Proc. Nat. Acad. Sci. USA . Nei. 80 , 1983, s. 6972-6976 , PMID 6316339 .
- ↑ RD Bigler, DE Fischer, CY Wang, EA Kan, EA Rinnooy Kan, HG Kunkel: idiotype-lignende molekyler på celler av human T-celle leukemi . I: J. Med .. . Nei. 158 , 1983, s. 1000-1005 , PMID 6604124 .
- ↑ P. Kung, G. Goldstein, E. Reinherz, SF Schlossman: Monoklonale antistoffer som definerer karakteristiske humane T-celleoverflate-antigener . I: Vitenskap . teip 206 , 1979, s. 347-349 .
- ↑ HC Oettgen, J. Kappler, WJM Tax, C. Terhorst: Karakterisering av de to tunge kjedene til T3-komplekset på overflaten av humane T-lymfocytter . I: Journal of Biological Chemistry . teip 259 , nr. 19 , 10. oktober 1984, s. 12039-12048 , PMID 6090452 .
- ↑ O. Acuto, R. E: Hussey, KA Fitzgerald, JP Protentis, SC Meuer, SF Schlossman, EL Reinherz: Den humane T-cellereseptoren: utseende i ontogeni og biokjemisk forhold av alfa- og beta-underenheter på IL-2-avhengige kloner og T-celle svulster . I: Cell . Nei. 34 , 1983, s. 717-726 , PMID 6605197 .
- Kapp J. Kappler, R. Kubo, K. Haskins, J. White, P. Marrack: Mus T-celle reseptor: sammenligning av MHC-begrensede reseptorer på to celle hybridomer . I: Cell . Nei. 34 , 1983, s. 727-737 , PMID 6605198 .
- ↑ Y. Yanagi, Y. Yoshikai, SP Clark, I. Aleksander, TW Mak: En human T-celle-spesifikke cDNA-klonen ancodes et protein som har utstrakt homologi til immunoglobulinkjeder . I: Natur . Nei. 308 , 1984, s. 145-149 , PMID 6202421 .
- ↑ SM Hedrick, DI Cohen, EA Nielsen, MM Davis : Isolering av cDNA-kloner som koder for T-celle-spesifikke membranbundne proteiner . I: Natur . Nei. 308 , 1984, s. 149-153 , PMID 16116160 .
- ↑ MB Brenner, J. McLean, DP Dialynas, JL Strominger , JA Smith, FL Owen, JG Seidman et al.: Identifisering av en antatt andre T-celle-reseptor . I: Natur . Nei. 322 , 1986, s. 145-149 , PMID 3755221 .
- ↑ Z. Dembic, W. Haas, S. Weiss, J. McCubrey, H. Kiefer, H. von Boehmer, M. Steinmetz: Overføring av spesifisitet av murine alfa- og beta T-celle-reseptorgener . I: Natur . Nei. 320 , 1986, s. 232-238 , PMID 2421164 .
- ^ WH Lewis, E. E: Michalopoulos, DL Williams, MD Minden, TW Mak: Breakpoints in the human T cell antigen receptor alfa chainlocus in two T-cell leukemia pasienter med kromosomal translokasjon . I: Natur . Nei. 317 , 1985, s. 544-546 , PMID 3876514 .
- Norm AM Norment, RD Salter, P. Parham, VH Engelhard, DR Littman: Cellecelleadhesjon mediert av CD8 og MHC-I klasse I molekyler . I: Natur . Nei. 336 , 1988, s. 79-81 , PMID 3263576 .
- ↑ D. Maspoust, V. Vezys, EJ Wherry, R. Ahmed: En kort historie av CD8 T-celler . I: Eur. J. Immunol. . Nei. 37 , 2007, s. 103-110 , PMID 17972353 .