Spektral linje
Som spektrale linjer eller resonanselinjer , skarpt adskilte linjer i et spektrum av utsendte ( emisjonslinjer ) eller absorberte ( absorpsjonslinjer ) av elektromagnetiske bølger , i smalere forstand innenfor bølgelengdeområdet for synlig lys ( lysspektrum ). Spektrallinjer er preget av bølgelengde , linjeintensitet og linjebredde . Årsaken til de spektrale linjene er de lyse elektriske overgangene iAtomer eller molekyler .
Navnet spektral linje går historisk tilbake til det faktum at det er en inngangspalte i konvensjonelle spektrometre , hvis form reflekteres på skjermen eller i betrakterens øye. Navnet ble senere også overført til toppene (dvs. maksima) i et spektrum registrert som en intensitetskurve.
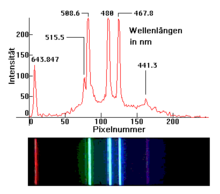
Spektrale linjer forekommer i instrumental atomspektroskopi (for eksempel kjernemagnetisk resonansspektroskopi ) eller i flammefarging . De brukes blant annet i astronomi for å analysere den molekylære strukturen til stjerner , planeter og interstellar materie , noe som ellers ville være umulig. De befant seg i lysbrekk fra solen gjennom et prisme oppdaget på 1800-tallet, hvorfra spektroskoper utviklet seg som tillot et bredt felt av applikasjoner for spektralanalysen .
Grunnleggende
En spektral linje er lyset fra en nøyaktig definert frekvens som sendes (sendes ut) eller absorberes (absorberes) av et atom eller molekyl på grunn av en overgang fra ett energinivå til et annet. Frekvensen bestemmes av energien til det emitterte eller absorberte fotonet ; dette er lik forskjellen mellom energiene til de to kvantemekaniske tilstandene . Frekvensen er karakteristisk for denne spesielle overgangen i den gitte atomtypen. Derfor kan man skille typer atomer ved å observere spektrale linjer.
Utslippslinje
En utslippslinje dukker opp som en lyslinje i spekteret. Det oppstår ved overgangen fra et høyere til et lavere energinivå , for eksempel når et elektron passerer fra en eksitert tilstand til grunntilstanden. Her sendes det ut et foton. Dette kan enten skje spontant ( spontan utslipp ) eller, for eksempel. B. med laser , blir begeistret av lys med en passende frekvens ( stimulert utslipp ).
Absorpsjonslinje
Når lys bestråles med et kontinuerlig spekter (dvs. en frekvensblanding), resulterer resonansabsorpsjon av fotoner med en passende frekvens i en absorpsjonslinje der en overgang fra et lavere til et høyere energinivå induseres - for eksempel når et elektron passerer gjennom fotonet fra valensbåndet inn i ledningsbåndet "løftes" (se fotoelektrisk effekt ).
Når du faller tilbake til det lavere energinivået, blir fotoner isotrope , dvs. H. i hvilken som helst retning, sendes ut.
Begge disse fører til at lyset blir spredt diffust av materialet som bestråles ved denne frekvensen . Så lenge det er nok absorberende atomer, kommer det til
- en mørk linje i det kontinuerlige lysspekteret som skinner gjennom ( Fraunhofer-linjen ); dette er vanligvis det som menes med begrepet absorpsjonslinje
- en lys linje mot en mørk bakgrunn når man analyserer det spredte lyset som kommer ut av siden av gassen; denne typen lyslinje kalles ikke en utslippslinje på grunn av historisk terminologi ; Linjer blir bare referert til som sådan hvis eksitasjonen ikke ble laget med lys av samme frekvens .
Utslippsprofiler
Lyset fra en spektral linje inneholder ikke en enkelt, skarpt definert frekvens, men har et (smalt) frekvensområde. Den halv Bredden av dette området kalles linjebredde . Linjebredden til en utslippslinje består av flere bidrag:
- Lorentz profil
- Den naturlige linjebredden skyldes levetiden til den opprinnelige tilstanden gjennom Heisenberg usikkerhetsprinsippet . Dette har form av en Lorentz-kurve . Det er ikke mulig å redusere dette.
- Gaussisk profil
- Atomenes termiske bevegelse skaper en dopplereffekt som skifter lyset fra et enkelt atom eller molekyl til rødt eller blått, avhengig av bevegelsesretningen. Den statistiske bevegelsen resulterer i en bredere frekvensfordeling samlet. Denne effekten kalles utvidelse av doppler . Den har form av en Gaussisk kurve og er avhengig av temperaturen . Vanligvis dominerer dopplerbredden tydelig over den naturlige linjebredden. Mekanismen er også kjent under betegnelsen inhomogen linjeutvidelse .
- Voigt-profil
- Under en måling ser det ut til at en Lorentz-kurve med endelig bredde har endret seg fra den kjente formen hvis apparatfunksjonen til målearrangementet har en halv bredde i størrelsesorden av Lorentz-kurven under vurdering. Linjeformen kan deretter beskrives ved konvolusjon av Lorentz-kurven og apparatets funksjon. Hvis apparatets funksjon er en Gaussisk kurve, kalles resultatet av konvolusjonen en Voigt-profil .
historie
Absorbsjonslinjer ble først oppdaget i 1802 av William Hyde Wollaston og i 1814, uavhengig av ham, av Joseph von Fraunhofer i spekteret av Søn . Disse mørke linjene i solspekteret kalles også Fraunhofer-linjer .
Spektrallinjene, blant andre effekter, bidro til utviklingen av kvantemekanikk . I følge klassisk elektrodynamikk kunne et elektron bundet i et atom avgi elektromagnetiske bølger av hvilken som helst frekvens; eksistensen av diskrete linjer kunne ikke forklares klassisk. Oppdagelsen om at frekvensene til hydrogenatomens spektrale linjer er proporsjonale med et uttrykk for formen med heltall og førte til begrepet kvantetall og til slutt førte Niels Bohr til sin Bohr-modell av atomet , den første - nå foreldet - kvantemekanisk atommodell. Moderne kvantemekanikk kan forutsi atomerens spektrale linjer med veldig høy grad av nøyaktighet.
litteratur
- Heinz Haferkorn : Optikk. Fysisk-tekniske grunnleggende og anvendelser. 4. utgave, Wiley-VCH 2003, ISBN 3-527-40372-8
- Ingolf Volker Hertel , Claus-Peter Schulz: Atomer, molekyler og optisk fysikk 1 . Springer 2008, ISBN 978-3-540-30617-7
- Peter M. Skrabal: Spectroscopy , vdf Verlag, 2009, ISBN 978-3-8252-8355-1




