Isoleucin
| Strukturell formel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
|
L -Isoleucine For strukturer av andre isomerer, se stereoisomerisme | ||||||||||||||||||||||
| Generell | ||||||||||||||||||||||
| Etternavn | Isoleucin | |||||||||||||||||||||
| andre navn |
|
|||||||||||||||||||||
| Molekylær formel | C 6 H 13 NO 2 | |||||||||||||||||||||
| Kort beskrivelse |
fargeløst fast stoff med svak lukt |
|||||||||||||||||||||
| Eksterne identifikatorer / databaser | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Legemiddelinformasjon | ||||||||||||||||||||||
| ATC-kode | ||||||||||||||||||||||
| eiendommer | ||||||||||||||||||||||
| Molarmasse | 131,18 g mol −1 | |||||||||||||||||||||
| Fysisk tilstand |
fast |
|||||||||||||||||||||
| Smeltepunkt |
284 ° C (spaltning, L- isoleucin) |
|||||||||||||||||||||
| pK s verdi |
|
|||||||||||||||||||||
| løselighet |
løselig i vann (40 g l -1 ved 20 ° C, L- isoleucin) |
|||||||||||||||||||||
| sikkerhetsinstruksjoner | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Så langt som mulig og vanlig, brukes SI-enheter . Med mindre annet er oppgitt, gjelder opplysningene standardbetingelser . | ||||||||||||||||||||||
Isoleucin , forkortet Ile eller I , er i sin naturlige L- form en essensiell proteinogen α - aminosyre .
Siden isoleucin kan stamme fra asparaginsyre , tilhører den aspartatgruppen . Det hører sammen med sine strukturelle isomerer leucin , norleucin og tert -leucin for substans gruppe av leucin .
historie
I 1901 foreslo Emil Fischer , som senere vant Nobelprisen , at leucinfraksjonen han isolerte inneholdt, i tillegg til leucin, en "aminosyre med samme sammensetning men med større grad av rotasjon". Faktisk var den tyske kjemikeren Felix Ehrlich i 1903 i stand til å isolere en forbindelse isomerisk til leucin fra melasse av sukkerroer , kalt isoleucin. Felix Ehrlich anerkjente grunnloven i 1907 gjennom nærmere etterforskning.
Hendelse
Isoleucin er en peptidbundet komponent i animalske og vegetabilske proteiner . De følgende eksemplene vedrører hver 100 g av maten; prosentandelen isoleucin i det totale proteinet er også gitt.
| Mat | protein | Isoleucin | andel av |
|---|---|---|---|
| storfekjøtt | 21,26 g | 967 mg | 4,5% |
| Kyllingbrystfilet | 23,09 g | 1219 mg | 5,3% |
| laks | 20,42 g | 968 mg | 4,7% |
| Kyllingegg | 12,58 g | 672 mg | 5,3% |
| Kumelk, 3,7% fett | 3,28 g | 198 mg | 6,0% |
| Valnøtter | 15,23 g | 625 mg | 4,1% |
| Hele hvetemel | 13,70 g | 508 mg | 3,7% |
| Fullkornsmel | 6,93 g | 248 mg | 3,6% |
| Ris, ikke skrelt | 7,94 g | 336 mg | 4,2% |
| Erter, tørket | 24,55 g | 1014 mg | 4,1% |
Alle disse matvarene inneholder nesten utelukkende kjemisk bundet L- isoleucin som proteinkomponent, men ingen fri L- isoleucin i rå tilstand .
Stereoisomerisme
Isoleucin har to stereosentrere, så det er fire stereoisomerer ; I vårt miljø spiller imidlertid bare L- isoleucin en rolle som proteinogen aminosyre og er fysiologisk viktig. Når det er snakk om "isoleucin" uten noe ekstra navn ( deskriptor ), blir det ofte referert til som L- isoleucin.
Enantiomeren til den naturlige L- isoleucinen er D- isoleucin. L - allo- isoleucin og dens enantiomer D - allo- isoleucin er diastereomerer av L- isoleucin.
| Isomerer av isoleucin | ||||
| Etternavn | L- isoleucin | D -isoleucin | L - allo- isoleucin | D - allo- isoleucin |
| andre navn | (2 S , 3 S ) -2-amino-3-metylpentansyre ( S ) -isoleucin |
( 2R , 3R ) -2-amino-3-metylpentansyre ( 2R , 3R ) -2-amino-3-metylvalerinsyre |
(2 S , 3R ) -2-amino-3-metylpentansyre | ( 2R , 3S ) -2-amino-3-metylpentansyre |
| Strukturell formel |

|

|

|
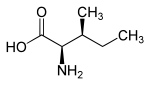
|
| CAS-nummer | 73-32-5 | 319-78-8 | 1509-34-8 | 1509-35-9 |
| 443-79-8 (uspes.) | ||||
| EF-nummer | 200-798-2 | 206-269-2 | 216-142-3 | 216-143-9 |
| 207-139-8 (uspes.) | ||||
| ECHA- infokort | 100.000.726 | 100,005,701 | 100.014.675 | 100.014.676 |
| 100.006.492 (uspes.) | ||||
| PubChem | 6306 | 76551 | 99288 | 94206 |
| 791 (uspes.) | ||||
| Wikidata | Q484940 | Q27103290 | Q27092902 | Q27109362 |
| Q27117434 (uspes.) | ||||
| Smeltepunkt | Nedbrytning: 284 ° C | |||
eiendommer
Isoleucin er til stede på det isoelektriske punkt (en viss pH-verdi ) som et zwitterion (indre salt), hvorved protonet i karboksygruppe (-COOH) blir dissosiert og aminogruppen (-NH 2 ) er protonert.
- Sidekjede : lipofil
- isoelektrisk punkt : 5,94
- Van der Waals-volum : 124
- Løselighet Lipid : logP = 4,5
Biokjemisk betydning
På den ene siden er isoleucin nødvendig som en byggestein for proteinsyntese . På den annen side kan den også brukes til å generere energi i muskelceller . Dette spiller en rolle i et proteinrikt kosthold eller under lengre anstrengelser og i faser av sult når kroppen trekker på sine egne reserver. Nedbrytningen av isoleucin gir acetyl-CoA og propionyl-CoA .
Estimatene av det daglige behovet for friske voksne varierer, avhengig av metoden, fra 7,5 til 28 mg isoleucin per kilo kroppsvekt. I den menneskelige organismen forekommer isoleucin nesten utelukkende i en bundet tilstand. Konsentrasjonen av fri isoleucin i blodet er rundt 7 mg / l; 10 til 15 mg skilles ut i urinen per dag.
Utdrag
De viktigste ekstraksjonsmetodene er gjæringsprosesser der glukoseholdige oppløsninger med tilsetning av L - treonin omdannes av L- isoleucinproduserende mikroorganismer. På den annen side oppnås en blanding av de naturlige aminosyrene L- leucin og L- isoleucin ved hydrolyse av proteiner og påfølgende separasjonsoperasjoner av hydrolysatene . Disse konstitusjonelle isomerer kan da være z. B. atskilt ved en enzymatisk prosess.
bruk
Som en komponent av aminosyreinfusjonsløsninger for parenteral ernæring er L- Isoleucin, sammen med andre aminosyrer, mye brukt i humanmedisin. En oralt administrert “kjemisk definert diett” som inneholder L- isoleucin ble utviklet for pasienter med nedsatt fordøyelse . I denne dietten er aminosyrene kilden til nitrogen; alle viktige næringsstoffer er i kjemisk nøyaktig definert form.
weblenker
Individuelle bevis
- ↑ a b c d e f Oppføring på L-isoleucin i GESTIS stoffdatabase til IFA , åpnet 5. februar 2018. (JavaScript kreves)
- ^ A b Hans Beyer, Wolfgang Walter: Lærebok for organisk kjemi . Hirzel Verlag, Stuttgart 1991, ISBN 3-7776-0485-2 , s. 823.
- ↑ S. Hansen: Oppdagelsen av proteinogene aminosyrer fra 1805 i Paris til 1935 i Illinois . ( Memento av den opprinnelige fra 15 juni 2016 i Internet Archive ) Omtale: The arkivet koblingen ble satt inn automatisk og har ennå ikke blitt sjekket. Kontroller originalen og arkivlenken i henhold til instruksjonene, og fjern deretter denne meldingen. (PDF) Berlin 2015.
- E F. Ehrlich: Om den naturlige isomeren av leucin . I: Ber Deutsche Chem Ges . Volum 37, 1904, s. 1809-1840, doi: 10.1002 / cber.19040370295 .
- E F. Ehrlich: Om den naturlige isomeren av leucin. Konstitusjon og syntese av isoleucin . I: Ber Deutsche Chem Ges . Volum 40, nr. 2, 1907, s. 2538-2562, doi: 10.1002 / cber.190704002181 .
- ↑ næringsdatabase fra US Department of Agriculture , 21. utgave.
- ↑ Bernd Hoppe, Jürgen Martens: Aminosyrer - produksjon og ekstraksjon . I: Kjemi i vår tid , 1984, 18, s. 73-86.
- ↑ JM Berg, JL Tymoczko, L. Stryer: Biochemistry. 6. utgave. Spectrum Academic Publishing House, Elsevier, München 2007; Pp. 735, 746; ISBN 978-3-8274-1800-5 .
- ↑ AV Kurpad, MM Regan, T. Raj, JV Gnanou: forgrenet aminosyre kravene hos friske voksne mennesker . I: J. Nutr. , 2006, 136 (1 Suppl), s. 256S-263S, PMID 16365094 .
- ^ Roche Lexicon Medicine. 5. utgave. Urban & Fischer Verlag, Elsevier, München 2003, ISBN 978-3-437-15150-7 .
- ↑ a b Yoshiharu Izumi, Ichiro Chibata og Tamio Itoh: Produksjon og bruk av aminosyrer . I: Angewandte Chemie , 1987, 90, s. 187-194. Angewandte Chemie International Edition på engelsk , 1978, 17, s. 176-183, doi: 10.1002 / anie.197801761 .
- ↑ Hitoshi Enei, Kenzo Yokozeki, Kunihiko Akashi: Nylig fremgang i mikrobiell produksjon av aminosyrer . Gordon & Breach Science Publishers, 1989, ISBN 978-2-88124-324-0 , s.61.
- ↑ Jürgen Martens , Horst Weigel: Enzymatisk separasjon av L -Leucine og L -Isoleucine . I: Liebigs Annalen der Chemie , 1983, s. 2052-2054.
