Influensavaksine
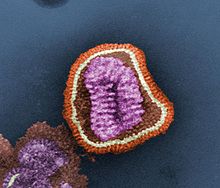
En influensavaksine (synonym influensavaksine ) er en vaksine mot influensavirus . Influensavaksiner brukes til influensavaksinasjon (influensavaksinasjon).
eiendommer
Influensavaksiner er rensede antigener , splittede vaksiner , inaktiverte virus eller dempede virus . På grunn av den relativt høye genetiske variabiliteten på grunn av antigenskift og antigendrift (som mekanismer for immununddragelse ) av influensavirusene, er epitopene som er effektive i en vaksine ofte ikke til stede i influensavirusene den påfølgende sesongen. Som et resultat er effektiviteten til godkjente influensavaksiner begrenset til virus som ligner på vaksinestammen, og det er liten immunitet mot andre influensastammer. Videre publiserer Paul Ehrlich Institute nåværende referansestammer for sesonginfluensavaksiner i Tyskland hvert år i samsvar med gjeldende anbefalinger fra Verdens helseorganisasjon og komiteen for humanmedisiner ved Det europeiske legemiddelkontoret, på grunnlag av hvilken vaksineproduksjonen. er tilpasset. På grunn av variabiliteten endres disse anbefalingene nesten hvert år for en eller flere stammer. Referansestammene inkluderer to influensa A-virus og ett influensa B-virus for vanlige trivalente (treverdige) vaksiner, og et andre influensa B-virus for tetravalente (firdrevne, tetravalente) vaksiner. I motsetning til dette, pandemiske influensavaksiner som de mot en svært patogen variant av influensa A-virus H5N1 , som utløseren av fugleinfluensa H5N1 , eller mot stammen A / California / 7/2009 (H1N1) pdm09 til influensa A-viruset H1N1 , som utløser Pandemic H1N1 2009/10 , bare en vaksinestamme. Siden de opprinnelige pandemiske H1N1-virusstammene har sirkulert over hele verden som sesonginfluensa siden 2010 (med vanlig variasjon), har de vært blant referansestammene for sesonginfluensavaksiner siden 2010. Influensavaksiner er på Verdens helseorganisasjons liste over essensielle medisiner .
immunologi
Influensavaksiner produserer nøytraliserende antistoffer som hindrer celler i å reinfisere med samme virusstamme. I liten grad er disse antistoffene kryssreaktive med andre influensastammer. Antistoffene dannes hovedsakelig mot det humorale immundominante hemagglutinin og neuraminidase . Disse antistoffene kan bli anvendt i løpet av virologiske diagnostikk for å bestemme titeren i den vaksinerte person eller vaksinen serotype . Rensede antigener, splittede eller inaktiverte influensavaksiner absorberes ikke i celler, og det er derfor det ikke er noen uttalt cellulær immunrespons .
Bivirkninger
Bivirkninger fra influensavaksiner inkluderer smerte og hevelse på injeksjonsstedet og en dagslang feber. Sammensetningen av svineinfluensavaksinen Pandemrix administrert fra 2009 til 2010 kan antagelig, i sjeldne tilfeller, føre til narkolepsi , mens de konkurrerende vaksinene som Focetria ikke ble påvirket.
Produksjon av vaksinen
Kulturmedier
Virusene for influensavaksinasjon dyrkes og multipliseres i forskjellige medier:
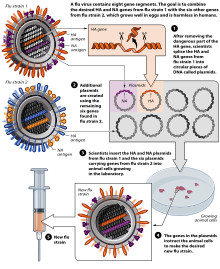
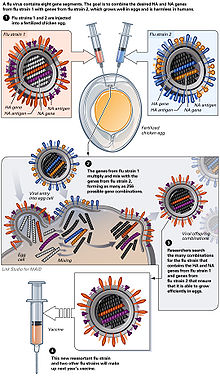
Kyllingegg
Viruset reproduseres for tiden hovedsakelig i spesielle inkuberte høneegg , de "spesifikke patogenfrie eggene", som er 10-11 dager gamle. I februar det respektive året bestemmer WHO sammensetningen av den sesongmessige vintervaksinen. Det såkalte "frøvirus" av de valgte virusstammene sendes til produsenten. For å oppnå optimale utbytter, står produsentens ut en HG (høy-vekst) reassortment . Dette tar omtrent seks uker. Influensavirus multipliserer i Chorio - allantoisk membran. Eggene som er inokulert med influensavirus inkuberes i tre dager ved 32 ° C. I løpet av denne perioden formerer viruset seg veldig sterkt. Eggene åpnes og 6-7 ml virusholdig allantoisk væske høstes per egg. Imidlertid har denne typen produksjon ulemper: Produksjonen av vaksinen tar omtrent 6 måneder, den ferdige vaksinen er tilgjengelig i juni / juli og blir utsatt for årlige kliniske studier. I tilfelle av en influensa pandemi , kan storskala eggproduksjon ikke oppnås på grunn av behovet for millioner av egg, siden planleggingen av logistiske kapasiteter som kreves for dette krever rundt to år i forveien. Eggvaksiner krever også komplisert rensing og forårsaker bivirkninger, hvor eggproteinallergier er et spesielt problem. En annen mangel er følsomheten i produksjonsprosessen for forurensning og nødvendig bruk av store mengder antibiotika . Pandemiske influensastammer er også veldig aggressive; spesielt kan stammer av aviær opprinnelse ikke reproduseres på kyllingembryoer.
Cellekulturer
Et alternativ er produksjonen av vaksinen i Vero-celler eller MDCK-celler (engelske Madin-Darby Canine Kidney celler ). Fordelene med denne teknologien er korthet i produksjonsprosessen (ved å eliminere HG- sortimentet ) og den store produksjonskapasiteten. Dette gir rask respons på raskt økende etterspørsel. Vero-celler dyrkes i industriell skala i bioreaktorer med en kapasitet på flere 1000 liter. Pandemistammer kan forplantes med høye utbytter. Den sterile teknologien (teknologi sett fra steriliserbarheten og rengjørbarheten til systemene, samt retensjonskapasiteten mot mikroorganismer eller biologisk aktive stoffer) muliggjør en sikker utforming av produksjonsanlegget. Håndtering av pandemiske influensastammer krever biologisk beskyttelsesnivå 3 (BSL-3; Bio-sikkerhetsnivå), som ikke kan oppnås for egganlegg på grunn av prosessforløpet (vanskelig å automatisere). Søknaden fra bransjens tilgjengelige influensavaksine dekker bare det gjennomsnittlige forventede årlige forventede forbruket, så WHO 19. august 2005 i tilfelle en fornyet pandemi brakte alvorlige bekymringer for en uttrykt truende mangel.
Eksperimentell prosedyre
Det forskes for eksempel på fremstilling av influensavaksine ved hjelp av ciliater . Metoden skal være raskere og mindre risikabel enn den forrige standarden.
Døde og levende vaksiner
Avhengig av type videre vaksinepreparat skilles det mellom døde vaksiner og levende vaksiner for influensavaksiner, slik tilfellet er med vaksiner mot andre patogener .
Døde vaksiner
Inaktiverte vaksiner er forskjellige i sammensetningen av virale proteiner, i antigeninnholdet og typen adjuvanser . De er delt inn i:
- Inaktiverte helpartikkelvaksiner (også: full virusvaksine ): Inaktivering (avliving) av virus ved hjelp av kjemiske stoffer / kombinasjoner av stoffer, f.eks. B. formaldehyd , beta-propiolakton og psoralen . Viruskonvolutten beholdes.
- (Inaktiverte) partikkelvaksiner (også: underenhetsvaksine ): ødeleggelse (spaltning) av viralhylsen med vaskemidler eller sterke organiske løsningsmidler. Virusene kan også inaktiveres (drepes) med kjemiske stoffer.
- Underenhetsvaksiner : overflaten er fullstendig oppløst og spesifikke komponenter ( hemagglutinin- og neuraminidaseproteiner ) blir renset. En annen mulighet er å produsere underenhetene rekombinant . Underenhetsvaksiner er bare litt immunogene , men har få bivirkninger.
Såkalte “høydose-vaksiner” er splittede vaksiner og inneholder fire ganger mengden hemagglutinin-antigen (60 µg). Virusene ble dyrket i kyllingegg.
Levende vaksiner
Ved produksjon av levende vaksiner mot influensavirus, brukes virus som er dempet, men som fremdeles er i stand til reproduksjon ("vital"): ( English Live Attenuated Influenza Vaccine , LAIV , "live attenuated influenza vaccines "). Det skilles her mellom
- Kaldetilpassede stammer : disse stammene er bare i stand til å formere seg ved temperaturer rundt 25 ° C, noe som begrenser viruset til øvre luftveier. På grunn av mangel på replikasjon i de nedre luftveiene, utvikles bare milde symptomer, ikke fullstendig influensa. Et eksempel er stammen A / Leningrad / 134/47/57 (H2N2)
- temperaturfølsomme stammer : replikasjonen av disse stammene er begrenset til et temperaturområde på 38–39 ° C, og her er det heller ikke angrep i nedre luftveier.
Disse vaksinene gis intranasalt . Fordelen deres over de døde vaksinene som har blitt brukt hittil er at de vitale virusene stimulerer immunforsvaret lenger og ikke bare forårsaker en humoristisk immunrespons , men også en cellulær immunrespons . Ulempen med influensavaksiner fra patogener som fremdeles er i stand til å reprodusere, er at bivirkningene er hyppigere eller mer alvorlige. For eksempel måtte den sveitsiske godkjenningsprosessen for et dempet influensavirus ( Nasaflu ) avvikles i 2001 på grunn av parese av ansiktsmusklene. Levende vaksiner tilgjengelig i Tyskland er kun godkjent for barn (fra 2021).
Fremtidige influensavaksiner
Vaksinene som hittil er godkjent, retter seg mot bulgene ("hodene") av hemagglutininmolekylene på virusets overflate. Imidlertid endres dette molekylområdet i mindre enn en influensasesong på grunn av antigenskift og antigendrift. Dette fører til svingende og i gjennomsnitt bare lav effektivitet av vaksinene og behovet for å teste dem på nytt hvert år, å produsere dem i store mengder og vaksinere dem til alle målpersoner. Helsemyndighetene i USA og EU støtter derfor utviklingen av en "universell vaksine" mot influensa, som i likhet med vaksinene mot nesten alle andre patogener sjelden trenger å bli tilpasset og re-vaksinert, men vil være tilstrekkelig effektiv over flere sesonger. En tilnærming til dette er vaksiner som induserer bredt nøytraliserende anti-IAV antistoffer mot det ekstracellulære domene av matriks protein 2 (M2E) eller mot et bestemt område av hemagglutinin ( engelsk stilk region , "stamme region" mellom hode og transmembrandomenet ). Både det ekstracellulære domenet til M2 og stammeområdet til hemagglutinin er ikke veldig varierende (svært konservert ) mellom undertypene av influensavirus . Det antas derfor at det er et høyt utvalgstrykk for å bevare disse aminosyresekvensene og deres funksjon, noe som begrenser mulighetene for immununddragelse av influensavirusene. Vaksiner som fester seg til stamområdet til hemagglutinin har blitt undersøkt på testpersoner i fase III siden 2018 . Ytterligere tilnærminger for å øke den bredere effektiviteten inkluderer induksjon av cytotoksiske T-celler og T-hjelperceller mot konserverte epitoper av flere stammer av influensavirus eller deres konsensus-sekvens ved hjelp av vektorer , siden cytotoksiske T-celler bare induseres i liten grad av splittede vaksiner. En annen tilnærming er influensavaksiner laget av messenger RNA , for eksempel i EU støttet av CORDIS og UniVax-prosjektet av institusjoner fra syv EU-land. På den ene siden er RNA-vaksiner ment for å sikre at influensaviruset ikke lenger gir reproduktive avkom i kroppen til den vaksinerte personen. På den annen side bør immunforsvaret være bedre forberedt på fremtidige varianter av influensavirus.
WHO: Anbefaling om sesongens sammensetning av vaksiner siden 1998/1999
Influensavaksiner må tilpasses de sirkulerende influensavirusene hver sesong. Referanselaboratorier over hele verden - i Tyskland Nasjonalt referansesenter for influensa ved Robert Koch Institute - undersøker kontinuerlig de sirkulerende influensavirusene og overfører resultatene til WHO. WHO anbefaler da vanligvis visse antigenkombinasjoner for den nordlige halvkule i februar / mars og for den sørlige halvkule i september hvert år på grunnlag av disse rapportene.
| Nordlige halvkule av jorden | Sørlige halvkule av jorden | ||
|---|---|---|---|
| årstid | sammensetning | årstid | sammensetning |
| 2021/2022 |
Kyllingbaserte eller levende dempet influensavaksiner:
cellebaserte influensavaksiner:
|
2022 |
Kyllingbaserte eller levende dempet influensavaksiner:
|
| 2020/2021 |
Kyllingbaserte eller levende dempet influensavaksiner:
i den firdobbelte vaksinen som et andre B-antigen:
cellebaserte influensavaksiner:
i den firdobbelte vaksinen som et andre B-antigen:
|
2021 |
Kyllingbaserte eller levende dempet influensavaksiner:
i den firdobbelte vaksinen som et andre B-antigen:
cellebaserte influensavaksiner:
i den firdobbelte vaksinen som et andre B-antigen:
|
| 2019/2020 | A / Brisbane / 02/2018 (H1N1), pdm09-lignende stamme A / Kansas / 14/2017 (H3N2) -lignende stamme B / Colorado / 06/2017-lignende stamme (B / Victoria / 2/87 linje) i den firdobbelte vaksinen også variant av B / Phuket / 3073/2013-lignende stamme (B / Yamagata / 16/88 linje) |
2020 | A / Brisbane / 02/2018 (H1N1) pdm09-lignende stamme A / South Australia / 34/2019 (H3N2) -lignende stamme B / Washington / 02/2019-lignende stamme (B / Victoria line) i den firdobbelte vaksinen også B / Phuket / 3073/2013-lignende stamme (B / Yamagata-linjen) |
| 2018/2019 | A / Michigan / 45/2015 (H1N1) pdm09-lignende A / Singapore / INFIMH-16-0019 / 2016 (H3N2) -lignende B / Colorado / 06/2017-lignende (B / Victoria / 2/87-linje) i firdoblet vaksine også B / Phuket / 3073/2013-lignende (B / Yamagata / 16/88 linje) |
2018 | A / Michigan / 45/2015 (H1N1) pdm09 A / Singapore / INFIMH-16-0019 / 2016 (H3N2) B / Phuket / 3073/2013 i den firdobbelte vaksinen også B / Brisbane / 60/2008 |
| 2017/2018 | A / Michigan / 45/2015 (H1N1) pdm09 A / Hong Kong / 4801/2014 (H3N2) B / Brisbane / 60/2008 i den firdobbelte vaksinen også B / Phuket / 3073/2013 |
2017 | A / Michigan / 45/2015 (H1N1) pdm09 A / Hong Kong / 4801/2014 (H3N2) B / Brisbane / 60/2008 i den firdobbelte vaksinen også B / Phuket / 3073/2013 |
| 2016/2017 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Hong Kong / 4801/2014 (H3N2) B / Brisbane / 60/2008 i den firdobbelte vaksinen også B / Phuket / 3073/2013 |
2016 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Hong Kong / 4801/2014 (H3N2) B / Brisbane / 60/2008 i den firdobbelte vaksinen også B / Phuket / 3073/2013 |
| 2015/2016 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Sveits / 9715293/2013 (H3N2) B / Phuket / 3073/2013 i den firdobbelte vaksinen også B / Brisbane / 60/2008 |
2015 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Sveits / 9715293/2013 (H3N2) (tre lignende heter) B / Phuket / 3073/2013 i den firdobbelte vaksinen også B / Brisbane / 60/2008 |
| 2014/2015 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Texas / 50/2012 (H3N2) B / Massachusetts / 2/2012 |
2014 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Texas / 50/2012 (H3N2) B / Massachusetts / 2/2012 |
| 2013/2014 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Victoria / 361/2011 (H3N2) B / Massachusetts / 2/2012 |
2013 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Victoria / 361/2011 (H3N2) B / Wisconsin / 1/2010 |
| 2012/2013 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Victoria / 361/2011 (H3N2) B / Wisconsin / 1/2010 |
2012 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Perth / 16/2009 (H3N2) B / Brisbane / 60/2008 |
| 2011/2012 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Perth / 16/2009 (H3N2) (stammer som A / Wisconsin / 15/2009) B / Brisbane / 60/2008 |
2011 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Perth / 16/2009 (H3N2) B / Brisbane / 60/2008 |
| 2010/2011 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Perth / 16/2009 (H3N2) (stammer som A / Wisconsin / 15/2009) B / Brisbane / 60/2008 |
2010 | A / California / 7/2009 (H1N1) pdm09 (såkalt "svineinfluensa") A / Perth / 16/2009 (H3N2) B / Brisbane / 60/2008 |
| 2009/2010 | A / Brisbane / 59/2007 (H1N1) A / Brisbane / 10/2007 (H3N2) B / Brisbane / 60/2008 |
2009 | A / Brisbane / 59/2007 (H1N1) (stammer som A / South Dakota / 6/2007) A / Brisbane / 10/2007 (H3N2) (som A / Brisbane / 10/2007 eller A / Uruguay / 716/2007) B / Florida / 4/2006 (stammer som B / Brisbane / 3/2007) |
| 2008/2009 | A / Brisbane / 59/2007 (H1N1) A / Brisbane / 10/2007 (H3N2) B / Florida / 4/2006 (B / Brisbane / 3/2007) |
2008 | A / Salomonøyene / 3/2006 (H1N1) A / Brisbane / 10/2007 (H3N2) B / Florida / 4/2006 |
| 2007/2008 | A / Salomonøyene / 3/2006 (H1N1) A / Wisconsin / 67/2005 (H3N2) (som A / Hiroshima / 52/2005) B / Malaysia / 2506/2004 |
2007 | A / Ny-Caledonia / 20/99 (H1N1) A / Wisconsin / 67/2005 (H3N2) B / Malaysia / 2506/2004 |
| 2006/2007 | A / Ny-Caledonia / 20/99 (H1N1) A / Wisconsin / 67/2005 (H3N2) (A / Wisconsin / 67/2005 eller A / Hiroshima / 52/2005) B / Malaysia / 2506/2004 (som B / Ohio / 1/2005 eller B / Victoria / 2/87) |
2006 | A / Ny-Caledonia / 20/99 (H1N1) A / California / 7/2004 (H3N2) (også A / New York / 55/2004) B / Malaysia / 2506/2004 |
| 2005/2006 | A / Ny-Caledonia / 20/1999 (H1N1) A / California / 7/2004 (H3N2) (som A / New York / 55/2004) B / Jiangsu / 10/2003 |
2005 | A / Ny-Kaledonia / 20/99 (H1N1) A / Wellington / 1/2004 (H3N2) B / Shanghai / 361/2002 (B / Shanghai / 361/2002, B / Jilin / 20/2003 eller B / Jiangsu / 10 / 2003) |
| 2004/2005 | A / Ny-Caledonia / 20/99 (H1N1) A / Fujian / 411/2002 (H3N2) (som A / Wyoming / 3/2003 eller A / Kumamoto / 102/2002) B / Shanghai / 361/2002 (som stammene B / Shanghai / 361/2002 eller B / Jilin / 20/2003). På grunn av den utbredte bruken ble B / Jiangsu / 10/2003-stammer også brukt. |
2004 | A / Ny-Caledonia / 20/99 (H1N1) A / Fujian / 411/2002 (H3N2) (A / Kumamoto / 102/2002 og A / Wyoming / 3/2003 var lignende virusisolater dyrket i kyllingegg) B / Hong Kong / 330/2001 (B / Shandong / 7/97, B / Hong Kong / 330/2001 og B / Hong Kong / 1434/2002; B / Brisbane / 32/2002 var også tilgjengelig) |
| 2003/2004 | A / Ny-Caledonia / 20/99 (H1N1) A / Moskva / 10/99 (H3N2) (stammer som A / Panama / 2007/99) B / Hong Kong / 330/2001 (stammer som B / Shandong / 7/97 , B / Hong Kong / 330/2001, B / Hong Kong / 1434/2002) |
2003 | A / Ny-Caledonia / 20/99 (H1N1) A / Moskva / 10/99 (H3N2) (stammer som A / Panama / 2007/99) B / Hong Kong / 330/2001 (stammer som B / Shandong / 7/97 , B / Hong Kong / 330/2001, B / Hong Kong / 1434/2002) |
| 2002/2003 | A / Ny-Caledonia / 20/99 (H1N1) A / Moskva / 10/99 (H3N2) (stammer som A / Panama / 2007/99) B / Hong Kong / 330/2001 |
2002 | A / Ny-Caledonia / 20/99 (H1N1) A / Moskva / 10/99 (H3N2) (stammer som A / Panama / 2007/99) B / Sichuan / 379/99 (stammer som B / Guangdong / 120/2000, B / Johannesburg / 5/99 eller B / Victoria / 504/2000) |
| 2001/2002 | A / Ny-Caledonia / 20/99 (H1N1) A / Moskva / 10/99 (H3N2) (stammer som A / Panama / 2007/99) B / Sichuan / 379/99 (stammer som B / Johannesburg / 5/99 og B / Victoria / 504/2000) |
2001 | A / Moskva / 10/99 (H3N2) (stammer som A / Panama / 2007/99) A / Ny-Caledonia / 20/99 (H1N1) B / Sichuan / 379/99 (stammer som B / Guangdong / 120/2000, B / Johannesburg / 5/99 eller B / Victoria / 504/2000) |
| 2000/2001 | A / Moskva / 10/99 (H3N2) (stammer som A / Panama / 2007/99) A / Ny-Caledonia / 20/99 (H1N1) B / Beijing / 184/93 |
2000 | A / Moskva / 10/99 (H3N2) A / Ny-Caledonia / 20/99 (H1N1) B / Beijing / 184/93 (stammer som B / Shangdong / 7/97) |
| 1999/2000 | A / Sydney / 5/97 (H3N2) A / Beijing / 262/95 (H1N1) B / Beijing / 184/93 (stammer som B / Shangdong / 7/97) |
1999 | A / Sydney / 5/97 (H3N2) A / Beijing / 262/95 (H1N1) B / Beijing / 184/93 (vaksiner som B / Harbin / 7/94) |
| 1998/1999 | A / Sydney / 5/97 (H3N2) A / Beijing / 262/95 (H1N1) B / Beijing / 184/93 (vaksiner som B / Harbin / 7/94) |
1998 | |
Vaksiner godkjent i Tyskland
Sesong vaksiner 2020/2021 med stammejustering for 2020/2021
| beskrivelse | Indikasjonsgruppe for sykdom / stoff | Innehaver av markedsføringstillatelse | Vaksintype | Godkjenningsnummer | Dato for godkjenning | tilleggsinformasjon |
|---|---|---|---|---|---|---|
| Afluria Tetra 2020/2021 | Influensasplitt vaksine (virusvaksine, inaktivert) intramuskulært
Bruk fra du er 18 år |
Seqirus Nederland BV
Paasheuvelweg 28 1105 BJ Amsterdam Nederland |
Mono | PEI.H.1 2019.01.1 | 05/27/2020 | PharmNet.Bund
Vaksineprodusent: Seqirus Pty Ltd. Poplar Road 63 Parkville 3052, Victoria AU - Australia
|
| Gründipal 2020/2021 | Overflate-antigen influensa-underenhetsvaksine
(Virusvaksine, inaktivert) intramuskulær Bruk fra 6 måneders alder |
Seqirus, Srl, Via Fiorentina 1, 53100 Siena ( SI ), Italia | Mono | PEI.H.00968.01.1 | 06.04.1999 | PharmNet.Bund
Vaksineprodusent: Seqirus Vaccines Ltd. Gaskill Road Speke Liverpool L24 9GR UK |
| Fluad 2020/2021 | Overflate-antigen influensa-underenhetsvaksine
(Virusvaksine, inaktivert, adjuvansert) intramuskulær Bruk fra fylte 65 år |
Seqirus, Srl,
Via Fiorentina 1, 53100 Siena ( SI ), Italia |
Mono | PEI.H.01444.01.1 | 07/05/2000 | PharmNet.Bund
Vaksineprodusent: Seqirus Vaccines Ltd. Gaskill Road Speke Liverpool L24 9GR UK |
| Flucelvax Tetra 2020/2021 | Overflate-antigen influensa-underenhetsvaksine
(Virusvaksine fra cellekulturer, inaktivert, fri for eggehvite), intramuskulær Brukes fra en alder av 2 år |
Seqirus Nederland BV
Hullenbergweg 89 1101 CL Amsterdam Nederland |
Mono | EU / 1/18/1326/001 | 12/12/2018 | EPAR: Flucelvax Tetra
Vaksineprodusent: Seqirus Inc. 475 Green Oaks Parkway Holly Springs NC 27540 USA
|
| Fluenz Tetra 2020/2021 | Influensavaksine
(Virusvaksine, levende dempet), nasal Bruk fra 2 år til og med 17 år |
AstraZeneca AB, SE-151 85 Södertälje, Sverige | Mono | EU / 1/13/887 | 04/12/2013 |
EPAR : Fluenz Tetra
Vaksineprodusent: MedImmune UK Limited, Plot 6 Renaissance Way, Boulevard Industry Park, Speke, Liverpool L249JW UK Markedsføres i Tyskland i sesongen 2020/2021 |
| Influsplit Tetra 2020/2021 | Influensasplitt vaksine
(Virusvaksine, inaktivert), intramuskulær Brukes fra en alder av 6 måneder |
GlaxoSmithKline GmbH & Co. KG , München | Mono | PEI.H.11629.01.1 | 03/04/2013 | PharmNet.Bund
Vaksineprodusent: GlaxoSmithKline Biologicals NL fra SmithKline Beecham Pharma GmbH & Co. KG Circus Street 40 01069 Dresden, Tyskland
|
| Influvac 2020/2021 | Overflate-antigen influensa-underenhetsvaksine
(Virusvaksine, inaktivert) intramuskulær Brukes fra en alder av 6 måneder |
Mylan Healthcare GmbH ,
Freundallee 9A, 30173 Hannover, Tyskland |
Mono | PEI.H.00191.01.1 | 17.08.1998 | PharmNet.Bund
Vaksineprodusent: Abbott Biologicals BV CJ van Houtenlaan 36 1381 CP Weesp Nederland |
| Influvac Tetra 2020/2021 | Overflate-antigen influensa-underenhetsvaksine
(Virusvaksine, inaktivert) intramuskulær eller dyp subkutan Brukes fra en alder av 3 år |
Mylan Healthcare GmbH ,
Freundallee 9A, 30173 Hannover, Tyskland |
Mono | PEI.H.11881.01.1 | 31.07.2017 | PharmNet.Bund
Vaksineprodusent: Abbott Biologicals BV CJ van Houtenlaan 36 1381 CP Weesp Nederland Markedsføres i Tyskland i sesongen 2020/2021 |
| Vaxigrip Tetra 2020/2021 | Influensasplitt vaksine (virusvaksine, inaktivert)
intramuskulært eller subkutant Injeksjonsvæske, suspensjon i en ferdigfylt sprøyte Bruk fra 6 måneders alder |
Sanofi Pasteur
14 Espace Henry Vallée 69007 Lyon Frankrike |
Mono | PEI.H.11808.01.1 | 07/14/2016 | PharmNet.Bund
Vaksineprodusent: Sanofi Pasteur 14 Espace Henry Vallée 69007 Lyon Frankrike Influensavaksine "Vaxigrip Tetra 2020/2021" introdusert fra Frankrike
|
| Xanaflu Tetra 2020/2021 | Overflate-antigen influensa-underenhetsvaksine
(Virusvaksine, inaktivert) intramuskulær eller dyp subkutan Brukes fra en alder av 3 år |
Mylan Healthcare GmbH ,
Freundallee 9A, 30173 Hannover, Tyskland |
Mono | PEI.H.11882.01.1 | 31.07.2017 | PharmNet.Bund
Vaksineprodusent: Abbott Biologicals BV CJ van Houtenlaan 36 1381 CP Weesp Nederland Markedsføres i Tyskland i sesongen 2020/2021 |
2020/2021 sesongvaksiner uten belastningsjustering for 2020/2021
| beskrivelse | Indikasjonsgruppe for sykdom / stoff | Innehaver av markedsføringstillatelse | Vaksintype | Godkjenningsnummer | Dato for godkjenning | tilleggsinformasjon |
|---|---|---|---|---|---|---|
| Afluria | Influensasplitt vaksine
(Virusvaksine, inaktivert) intramuskulær Brukes fra en alder av 5 år |
Seqirus GmbH , Emil-von-Behring-Str. 76, 35041 Marburg, Tyskland | Mono | PEI.H.03523.01.1 | 06.08.2007 | PharmNet.Bund
Vaksineprodusent: Seqirus Pty Ltd. 45 Poplar Road, Parkville, Victoria 3052 AU - Australia |
| Efluelda | Influensasplitt vaksine
(Virusvaksine, inaktivert, 60 mikrogram HA / stamme) intramuskulært eller subkutant Bruk fra fylte 65 år |
Sanofi Pasteur
14 Espace Henry Vallée 69007 Lyon Frankrike |
Mono | PEI.H.12011.01.1 | 05.05.2020 | PharmNet.Bund
Vaksineprodusent: Sanofi Pasteur Parc Industriel d'Incarville 27100 Val de Reuil Frankrike |
| Fluad Tetra | Overflate-antigen influensa-underenhetsvaksine
(Virusvaksine, inaktivert, adjuvansert) intramuskulær Bruk fra fylte 65 år |
Seqirus Nederland BV
Paasheuvelweg 28 1105 BJ Amsterdam Nederland |
Mono | EU / 1/20/1433 | 20.05.2020 |
EPAR : Fluad Tetra
Vaksineprodusent: Seqirus Vaccines Limited Gaskill Road, Speke L24 9GR Liverpool Storbritannia |
| Fluarix | Influensasplitt vaksine (virusvaksine, inaktivert)
intramuskulær Bruk fra 6 måneders alder |
GlaxoSmithKline Biologicals SA, Belgia - Rixensart | Mono | PEI.H.11676.01.1 | 24/01/2013 | PharmNet.Bund
Vaksineprodusent: GlaxoSmithKline Biologicals Filial av SmithKline Beecham Pharma GmbH & Co. KG Circus Street 40 01069 Dresden |
| Fluarix Tetra | Influensasplitt vaksine (virusvaksine, inaktivert)
intramuskulær Bruk fra 6 måneders alder |
GlaxoSmithKline GmbH & Co. KG , München | Mono | PEI.H.11991.01.1 | 03.09.2020 | Vaksineprodusent:
GlaxoSmithKline Biologicals NL fra SmithKline Beecham Pharma GmbH & Co. KG Circus Street 40 01069 Dresden, Tyskland |
| Vaxigrip Tetra | Influensasplitt vaksine (virusvaksine, inaktivert)
intramuskulært eller subkutant Injeksjonsvæske, suspensjon i hetteglass for flere uttak Bruk fra 6 måneders alder |
Sanofi Pasteur
14 Espace Henry Vallée 69007 Lyon Frankrike |
Mono | PEI.H.11808.02.1 | 01/29/2020 | Vaksineprodusent:
Sanofi Pasteur 14 Espace Henry Vallée 69007 Lyon Frankrike |
Sesong 2017/2018
| vaksine | kommentar | Stoffgruppe | virulens | Minimumsalder for vaksinerte |
Maksimal alder for vaksinerte |
administrasjon |
|---|---|---|---|---|---|---|
| Afluria 2017/2018 | Delt vaksine | inaktivert | 5 | - | intramuskulær | |
| Begipal 2017/2018 | Overflate-antigen-underenhetsvaksine | inaktivert | 0,5 | - | intramuskulær | |
| Fluad 2017/2018 | Overflate-antigen-underenhetsvaksine | inaktivert | 65 | - | intramuskulær | |
| Fluarix | Delt vaksine | inaktivert | 0,5 | - | intramuskulær | |
| Fluenz Tetra 2017/2018 | Influensavirustyper A, H1N1 / A, H3N2 / B (Victoria-slekt) / B (Yamagata-slekt) | alle | live dempet | 2 | 17. | nese |
| Influensavaksine CSL | Delt vaksine | inaktivert | 5 | - | intramuskulær | |
| Influensavaksine STADA N 2017/2018 | Overflate-antigen-underenhetsvaksine | inaktivert | 0,5 | - | intramuskulær | |
| IDflu | Styrke: 15 µg | Delt vaksine | inaktivert | 60 | - | intradermal |
| Influs split SSW | Delt vaksine | inaktivert | 0,5 | - | intramuskulær | |
| Influsplit Tetra 2017/2018 | Delt vaksine | inaktivert | 3 | - | intramuskulær | |
| Influvac 2017/2018 | Overflate-antigen-underenhetsvaksine | inaktivert | 0,5 | - | intramuskulær | |
| Influvac Tetra | Overflate-antigen-underenhetsvaksine | inaktivert | 18. | - | intramuskulær eller dyp subkutan | |
| INTANZA | Styrke: 15 µg | Delt vaksine | inaktivert | 60 | - | intradermal |
| Optaflu | produsert i cellekultur | Overflate-antigen-underenhetsvaksine | inaktivert | 18. | - | intramuskulær |
| Vaxigrip 2017/2018 | Delt vaksine | inaktivert | 0,5 | - | intramuskulært, om nødvendig dypt subkutant | |
| Vaxigrip Tetra 2017/2018 | Delt vaksine | inaktivert | 3 | - | intramuskulært, om nødvendig dypt subkutant | |
| Xanaflu 2017/2018 | Overflate-antigen-underenhetsvaksine | inaktivert | 0,5 | - | intramuskulær | |
| Xanaflu Tetra | Overflate-antigen-underenhetsvaksine | inaktivert | 18. | - | intramuskulær eller dyp subkutan |
For de 10 vaksinene med indikasjonen 2017/2018 ble endringene for 2017/2018 sesongen allerede godkjent 24. august 2017.
litteratur
- DM Knipe, Peter M. Howley , DE Griffin, (red.): Fields Virology. 5. utgave. Lippincott Williams & Wilkins, Philadelphia 2007, ISBN 978-0-7817-6060-7 .
Individuelle bevis
- ^ WHO-modelliste over viktige medisiner. (PDF) I: Verdens helseorganisasjon. Oktober 2013, åpnet 22. april 2014 .
- ↑ J. Wrammert, K. Smith, J. Miller, WA Langley, K. Kokko, C. Larsen, NY Zheng, I. Mays, L. Garman, C. Helms, J. James, GM Air, JD Capra, R Ahmed, PC Wilson: Rask kloning av humane monoklonale antistoffer med høy affinitet mot influensavirus. I: Natur . Volum 453, nummer 7195, mai 2008, s. 667-671, doi: 10.1038 / nature06890 . PMID 18449194 , PMC 2515609 (gratis fulltekst).
- ↑ X. Cheng, M. Eisenbraun, Q. Xu, H. Zhou, D. Kulkarni, K. Subbarao, G. Kemble, H. Jin: H5N1-vaksinespesifikke B-celleresponser i ildere som er grunnet med levende svekkede sesongmessige influensavaksiner. I: PLOS ONE . Volum 4, nummer 2, 2009, art. E4436, doi: 10.1371 / journal.pone.0004436 . PMID 19209231 , PMC 2635969 (gratis fulltekst).
- ^ I. Leroux-Roels, G. Leroux-Roels: Nåværende status og fremgang for utvikling av prepandemisk og pandemisk influensavaksine. I: Ekspertgjennomgang av vaksiner. Volum 8, nummer 4, april 2009, s. 401-423, doi: 10.1586 / erv.09.15 . PMID 19348557 .
- ↑ Z. Wang, S. Tobler, J. Roayaei, A. Eick: Levende svekkede eller inaktiverte influensavaksiner og medisinske møter for luftveissykdommer blant amerikansk militærpersonell. I: JAMA . Volum 301, nummer 9, mars 2009, s. 945-953, doi: 10.1001 / jama.2009.265 . PMID 19255113 .
- ↑ Influensavaksinasjon : Hvordan Pandemrix forårsaker narkolepsi Ärzteblatt, per 2. juli 2015; åpnet 10. oktober 2020
- ↑ N. Feltelius, I. Persson, J. Ahlqvist-Rastad, M. Andersson, L. Arnheim-Dahl, P. Bergman, F. Granath, C. Adori, T. Hökfelt, S. Kuhlmann-Berenzon, P. Liljeström , M. Maeurer, T. Olsson, .. Örtqvist, M. Partinen, T. Salmonson, B. Zethe: Et koordinert tverrfaglig forskningsinitiativ for å adressere en økt forekomst av narkolepsi etter Pandemrix-vaksinasjonsprogrammet 2009–2010 i Sverige. I: Journal of Internal Medicine . Volum 278, nummer 4, oktober 2015, s. 335–353, doi: 10.1111 / joim.12391 . PMID 26123389 .
- St MC Sturkenboom: Den narkolepsipandemiske influensahistorien: kan sannheten noen gang avdekkes? I: Vaksine. Volum 33 Suppl 2, juni 2015, s. B6-B13, doi: 10.1016 / j.vaksine.2015.03.026 . PMID 26022571 .
- ↑ Spesialistinformasjon Flucelvax (PDF), Seqirus. Hentet 26. mai 2021.
- ↑ Ukentlig epidemiologisk rekord / Relevé épidémiologique hebdomadaire ; 19. august 2005, 80 år / 19 août 2005, 80e année. (PDF; 220 kB) HVEM; Nei. 33, 2005, 80, 277-288
- ^ Ny influensavaksine fra Münster . Antenne Münster, 11. april 2019; åpnet 7. juli 2019
- ↑ am: Influensavaksine fra ciliates. I: Farmasøytisk avis. 22. august 2013. Hentet 21. oktober 2013 .
- ↑ et b c beslutning og vitenskapelig begrunnelse for STIKO for oppdateringen av influensavaksine anbefaling for personer i alderen ≥60 år. I: RKI. 7. januar 2021, åpnet 11. januar 2021 .
- ↑ Robert B. Belshe, Kathryn M. Edwards, Timo Vesikari, Steven V. Black, Robert E. Walker, Micki Hultquist, George Kemble, Edward M. Connor: Live Attenuated versus Inactivated Influenza Vaccine in Spedbarn og Små barn. I: New England Journal of Medicine. 356, 2007, s. 685, doi: 10.1056 / NEJMoa065368 .
- ↑ Christopher S. Ambrose, Catherine Luke, Kathleen Coelingh: Nåværende status for levende svekket influensavaksine i USA for sesong- og pandemisk influensa. I: Influensa og andre respiratoriske virus. 2, 2008, s. 193, doi: 10.1111 / j.1750-2659.2008.00056.x . PMC 2710797 (fri fulltekst).
- ↑ T. Jefferson, A. Rivetti, C. Di Pietrantonj, V. Demicheli, E. Ferroni: vaksiner for å hindre influensa hos friske barn. I: The Cochrane Library 8: CD004879. 2012. doi: 10.1002 / 14651858.CD004879.pub4 . PMID 22895945 .
- ^ P. Sendi, R. Locher, B. Bucheli, M. Battegay: Intranasal influensavaksine i en arbeidende befolkning. I: Kliniske smittsomme sykdommer . Volum 38, nummer 7, april 2004, s. 974-980, doi: 10.1086 / 386330 . PMID 15034829 .
- ↑ Ashley P. Taylor: Første universelle influensavaksine for å gå inn i fase 3-prøveversjon , online 12. november 2018, åpnet 11. juni 2019
- H NIH begynner den første menneskelige prøven av en universell kandidat for influensavaksine . NIH 3. april 2019; åpnet 11. juni 2019
- ↑ L. Moise, F. Terry, M. ardito, R. Tassone, H. Latimer, C. Boyle, WD Martin, AS De Groot: Universal H1N1 influensavaksine utvikling: identifisering av konsensus klasse II-hemagglutinin og neuraminidase-epitoper avledet fra stammer sirkulerer mellom 1980 og 2011. I: Humane vaksiner og immunterapeutika. Volum 9, nummer 7, juli 2013, s. 1598-1607, doi: 10.4161 / hv.25598 . PMID 23846304 .
- X K. Xiang, G. Ying, Z. Yan, Y. Shanshan, Z. Lei, L. Hongjun, S. Maosheng: Fremgang med adenovirus-vektorerte universelle influensavaksiner. I: Menneskelige vaksiner og immunterapeutika. Volum 11, nummer 5, 2015, s. 1209-1222, doi: 10.1080 / 21645515.2015.1016674 . PMID 25876176 , PMC 4514376 (fri fulltekst).
- ↑ EU-kommisjonen: En "universell" influensavaksine gjennom syntetiske, dendritiske cellemålrettede, selvrepliserende RNA-vaksiner , åpnet 10. juni 2019
- ↑ UniVax-prosjekt: selvbeskrivelse
- ↑ Francesco Berlanda Scorza1, Norbert Pardi: Nye barn på blokken: RNA-baserte influensavirusvaksiner . 1. april 2018, PMC 6027361 (gratis fulltekst)
- ^ Anbefalinger om sammensetningen av vaksiner mot influensavirus . WHO; åpnet 2. juli 2019
- ↑ HVEM | Anbefalt sammensetning av influensavirusvaksiner for bruk i den nordlige halvkule influensasesongen 2021 - 2022. Hentet 26. mai 2021 .
- ↑ Gul liste online: STIKO-anbefaling for influensasesongen 2021/22 | Gul liste. Hentet 26. mai 2021 .
- ↑ HVEM | Anbefalt sammensetning av influensavirusvaksiner for bruk i influensasesongen 2020 - 2021. Hentet 22. mai 2020 .
- ^ Paul Ehrlich Institute - Influensavaksiner. Hentet 22. mai 2020 .
- ↑ HVEM | Anbefalt sammensetning av influensavirusvaksiner for bruk i influensasesongen på den sørlige halvkule 2021. Hentet 30. oktober 2020 .
- ^ Judith Koch, Sabine Vygen-Bonnet, Ole Wichmann: Stående vaksinasjonskommisjon (STIKO). De viktigste endringene på et øyeblikk. I: Deutsche Ärzteblatt. Volum 116, utgave 39, (27. september) 2019, s. B 1418 - B 1421, her: s. B 1421 ( vaksinesammensetning 2019/2020 ).
- ↑ Anbefalt sammensetning av influensavirusvaksiner for bruk i den nordlige halvkule influensasesongen 2019-2020. Oppdatering fra 21. mars 2019
- ↑ Anbefalt sammensetning av influensavirusvaksiner til bruk i influensasesongen på den sørlige halvkule 2020 , 27. september 2019
- ↑ Anbefalt sammensetning av influensavirusvaksiner for bruk i den nordlige halvkule influensasesongen 2018-2019. WHO, 22. februar 2018, åpnet 24. mars 2018 .
- ↑ Anbefalt sammensetning av influensavirusvaksiner til bruk i influensasesongen på den sørlige halvkule 2018 .
- ↑ hvem.int
- ↑ Anbefalt sammensetning av influensavirusvaksiner for bruk i den sørlige halvkule influensasesongen 2017 .
- ↑ Anbefalt sammensetning av influensavirusvaksiner for bruk i den nordlige halvkule influensasesongen 2016-2017 .
- ↑ Anbefalt sammensetning av influensavirusvaksiner for bruk i influensasesongen på den sørlige halvkule 2016 .
- ↑ Anbefalt sammensetning av influensavirusvaksiner for bruk i den nordlige halvkule influensasesongen 2015-2016 .
- ^ WHO - Anbefalt sammensetning av influensavirusvaksiner for bruk i 2015 sørlige halvkule influensasesong .
- ^ WHO - Anbefalt sammensetning av influensavirusvaksiner for bruk i den nordlige halvkule influensasesongen 2014-2015 .
- ^ WHO - Anbefalt sammensetning av influensavirusvaksiner for bruk i 2014-sesongen på den sørlige halvkule .
- ^ WHO - Anbefalt sammensetning av influensavirusvaksiner for bruk i den nordlige halvkule influensasesongen 2013-14 .
- ^ WHO - Anbefalt sammensetning av influensavirusvaksiner for bruk i 2013 sørlige halvkule influensasesong .
- ↑ WHO - Anbefalt sammensetning av influensavirusvaksiner for bruk i den nordlige halvkule influensasesongen 2012-2013 .
- ^ WHO - Anbefalt sammensetning av influensavirusvaksiner for bruk i den sørlige halvkule influensasesongen 2012 .
- ↑ Anbefalt sammensetning av influensavirusvaksiner for bruk i den nordlige halvkule influensasesongen 2011–2012 . Verdens Helseorganisasjon
- ↑ WHO / Europas anbefalinger om influensavaksinasjon i vintersesongen 2011/2012 . (PDF; 96 kB) Verdens helseorganisasjon (WHO), oktober 2011 (engelsk); WHO: Ofte stilte spørsmål: Anbefalt sammensetning av influensavirusvaksiner for bruk på den nordlige halvkule i influensasesongen 2011–2012 . (PDF; 24 kB) 17. februar 2011 (engelsk)
- ↑ who.int (PDF; 103 kB)
- ↑ who.int , phac-aspc.gc.ca (PDF; 204 kB)
- ↑ who.int (PDF; 318 kB)
- ↑ hvem.int ,
- ↑ Sentrene for sykdomskontroll og forebygging - influensa (influensa) - Ukentlig rapport: Oppsummering av influensa 20, sesong 2004-2005 .
- ^ WHO - Anbefalinger for influensavaksinekomposisjon .
- ↑ who.int (PDF; 217 kB)
- ↑ hvem.int ,
- ↑ Oppdatering: Influenza Activity - United States and Worldwide, 2003-04 Season, and Composition of the 2004-05 Influenza Vaccine .
- ^ WHO - Anbefalinger for influensavaksinekomposisjon .
- ↑ http://www.who.int/csr/disease/influenza/recommendations2004/en/index.html ( Memento fra 30. mai 2004 i Internet Archive )
- ^ WHO - Anbefalinger for influensavaksinekomposisjon .
- ^ WHO - Anbefalinger for influensavaksinekomposisjon .
- ^ WHO - Anbefalinger for influensavaksinekomposisjon .
- ^ WHO - Anbefalinger for influensavaksinekomposisjon .
- ^ WHO - Anbefalinger for influensavaksinekomposisjon .
- ^ WHO - Anbefalinger for influensavaksinekomposisjon .
- ^ WHO - Anbefalinger for influensavaksinekomposisjon .
- ^ WHO - Anbefalinger for influensavaksinekomposisjon .
- ^ WHO - Anbefalinger for influensavaksinekomposisjon .
- ^ WHO - Anbefalinger for influensavaksinekomposisjon .
- ^ WHO - Anbefalinger for influensavaksinekomposisjon .
- ^ A b Paul Ehrlich Institute - Influensavaksiner. Hentet 21. desember 2020 .
- ↑ Godkjente vaksiner. ( Memento fra 26. juni 2019 i Internet Archive ) PEI