Glysin
| Strukturell formel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
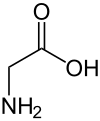
| ||||||||||||||||||||||
| Generell | ||||||||||||||||||||||
| Etternavn | Glysin | |||||||||||||||||||||
| andre navn |
|
|||||||||||||||||||||
| Molekylær formel | C 2 H 5 NO 2 | |||||||||||||||||||||
| Kort beskrivelse |
fargeløst og luktfritt, krystallinsk fast stoff |
|||||||||||||||||||||
| Eksterne identifikatorer / databaser | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Legemiddelinformasjon | ||||||||||||||||||||||
| ATC-kode | ||||||||||||||||||||||
| eiendommer | ||||||||||||||||||||||
| Molarmasse | 75,07 g mol −1 | |||||||||||||||||||||
| Fysisk tilstand |
fast |
|||||||||||||||||||||
| tetthet |
1,161 g cm −3 |
|||||||||||||||||||||
| Smeltepunkt |
Nedbrytning: 232-236 ° C |
|||||||||||||||||||||
| pK s verdi |
|
|||||||||||||||||||||
| løselighet |
lett løselig i vann
|
|||||||||||||||||||||
| sikkerhetsinstruksjoner | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toksikologiske data | ||||||||||||||||||||||
| Termodynamiske egenskaper | ||||||||||||||||||||||
| ΔH f 0 |
−528,5 kJ / mol |
|||||||||||||||||||||
| Så langt som mulig og vanlig, brukes SI-enheter . Med mindre annet er oppgitt, gjelder opplysningene standardbetingelser . | ||||||||||||||||||||||
Glycin , forkortet til Gly eller G , (også glysin eller glykocolla , fra gammelgresk κόλλα kólla: lim, i henhold til systematisk kjemisk nomenklatur aminoeddiksyre eller aminoetansyre), er den minste og enkleste α - aminosyren og ble først oppnådd i 1820 fra gelatin, dvs. fra kollagenhydrolysat . Den tilhører gruppen av hydrofile aminosyrer og er den eneste proteinogene (eller proteindannende) aminosyren achiral og er derfor ikke optisk aktiv .
Glysin er ikke viktig, så det kan syntetiseres av den menneskelige organismen selv og er en viktig komponent i nesten alle proteiner og en viktig node i stoffskiftet.
Navnet er avledet av den søte smaken av ren glycin ( gresk γλυκύς glykýs , tysk 'søt' ).
historie
Glysin er den første aminosyren som ble oppnådd gjennom den sure fordøyelsen av proteiner. Dette ble oppnådd av Henri Braconnot i Nancy i 1819, som hydrolyserte lim med svovelsyre med sikte på å utvinne sukker fra animalsk materiale.
Han kalte derfor de søtsmakende krystallene som ble oppnådd etter rensing, sucre de gélatine, på engelsk for "lim sukker". Gelatin er hovedingrediensen i glutenlim .
Rett etter ble stoffet omdøpt til Glykokoll ("søtt lim") før Jöns Jakob Berzelius bestemte seg for i 1848 at han fra nå av skulle bruke det kortere navnet glycin . Den kjemiske strukturen ble ikke beskrevet riktig før i 1858 av den franske kjemikeren Auguste André Thomas Cahours .
syntese
Aminonitrilen (nærmere bestemt: α- aminoacetonitril ) dannet under reaksjonen av formaldehyd , hydrogencyanid og ammoniakk ( Strecker-syntese ) gir glysin under hydrolyse :
Som en delvis reaksjon spilte denne reaksjonen en spesiell rolle i hypotesen om at organiske molekyler som "byggesteiner" for de første primitive organismer ble skapt for rundt 4 milliarder år siden av de enkle uorganiske forbindelsene i jordens uratmosfære . En sammensetning av vann (H 2 O), metan (CH 4 ), ammoniakk (NH 3 ), hydrogen (H 2 ) og karbonmonoksid (CO) samt helium (He) og andre edelgasser ble antatt for denne opprinnelige atmosfæren (se → Miller -Urey eksperiment ).
Kjemisk kan glysin også produseres fra monokloreddiksyre og ammoniakk:
Det meste av glysinet i kroppen absorberes gjennom mat, men det kan også lages av serin .
eiendommer
Glysin er hovedsakelig til stede som et "indre salt" eller zwitterion , hvis dannelse kan forklares med det faktum at protonen til den sure karboksygruppen migrerer til det eneste elektronparet på nitrogenatomet i den basiske aminogruppen :
Zwitterion vandrer ikke i det elektriske feltet fordi det er fulladet. Strengt tatt er dette tilfelle ved det isoelektriske punktet (ved en viss pH-verdi, her 5,97), hvor glycinet også har sin laveste løselighet i vann.
- Van der Waals-volum : 48
- Grad av hydrofobisitet : -0,4
Fritt glysin har en søt smak, hvor påvisningsterskelverdien på 25 til 35 mmol / L er lokalisert.
Hendelse
Følgende eksempler gir en oversikt over glysininnholdet og relaterer hver til 100 g av maten; prosentandelen av glysin i forhold til det totale proteinet er også gitt:
| Mat | Totalt protein |
Glysin | andel av |
|---|---|---|---|
| Svin , rå | 21 g | 0,95 g | 4,5% |
| Kyllingbrystfilet , rå | 21 g | 0,95 g | 4,4% |
| Laks , rå | 20,5 g | 0,95 g | 4,7% |
| Gelatinepulver , usøtet | 86 g | 19 g | 22,3% |
| Kyllingegg | 12,5 g | 0,43 g | 3,4% |
| Kumelk , 3,7% fett | 3,3 g | 0,07 g | 2,1% |
| Valnøtter | 15 g | 0,82 g | 5,4% |
| Gresskarfrø | 30 g | 1,85 g | 6,1% |
| Hele hvetemel | 14 g | 0,55 g | 4,0% |
| Fullkornsmel | 7,0 g | 0,28 g | 4,1% |
| Ris , ikke skrelt | 8,0 g | 0,39 g | 4,9% |
| Soyabønner , tørket | 36,5 g | 1,9 g | 5,2% |
| Erter , tørket | 24,5 g | 1,1 g | 4,4% |
Alle disse matvarene inneholder nesten utelukkende kjemisk bundet glysin som proteinkomponent, men ingen gratis glysin.
Glycin ble først påvist i partikkelprøver fra komaen til en komet i 2009 , samlet med Stardust- romfartøyet i 2004 nær 81P / Wild 2 . I 2016 ble det også oppdaget i halen til kometen 67P / Churyumov-Gerasimenko .
Funksjoner
metabolisme
Omdannelsen av serin glycin tjener ikke bare til å generere glysin, men også å omdanne tetrahydrofolsyre til N- 5 N 10 -methylen tetrahydrofolsyre (TH4), som er nødvendig blant annet for syntesen av tymin nukleotider ( DNA komponent) .
Omvendt kan glysin bli anvendt for å syntetisere serin ved å absorbere CH 3 fra TH4, som deretter er tilgjengelig for proteinsyntese, som grunnleggende substans av kolin eller som pyruvat.
Glysin er også ofte nødvendig for syntese av andre komponenter i genetisk materiale ( puriner ).
Det brukes også til biosyntese av hem ( oksygenbinding i blodet ), kreatin (energilagring i muskler) eller glutation :
- Glycin + succinyl-CoA → 5-aminolevulinsyre → porfyrinsyntese for å bygge opp hem.
- Glycin + guanodin gruppe (fra arginin ) → guanidinoacetat , som deretter kan brukes i kreatininsyntese.
- Glycin + Glu-Cys peptidbinding → glutation-syre
Som et biprodukt kan skadelig oksalsyre også dannes fra glycin .
Som en såkalt glukogen eller glukoplastisk aminosyre kan glysin omdannes til glukose via pyruvat i løpet av metabolismen .
Proteinkomponent
På grunn av sin lille størrelse, er glycin fortrinnsvis innarbeidet i polypeptider i romlig begrensede stillinger (proteinsekundærstruktur ).
Det er spesielt vanlig i kollagen , det vanligste proteinet i dyreorganismer. Her utgjør den en tredjedel av alle aminosyrene, da den lar kollagenet vinde opp for å danne sin tredobbelte helixstruktur på grunn av den lille størrelsen .
Nervesystemet
Glycin virker i sentralnervesystemet via glysinreseptoren som en inhiberende nevrotransmitter , dvs. som et inhiberende signalstoff. Effekten skjer via åpningen av ligandstyrte kloridkanaler og fører dermed til et hemmende postsynaptisk potensial (IPSP), som reduserer aktiviteten til nedstrøms nervecelle.
På NMDA-reseptoren har den derimot, i tillegg til hovedagonistglutamatet , en stimulerende effekt på et spesielt glycinbindingssted.
Glycin-frigivende nerveceller (glysinerg nevroner) finnes hovedsakelig i hjernestammen og ryggmargen , i det sistnevnte at de hemmer aktiviteten av de motoriske nevroner i den fremre horn , som fører til en reduksjon i aktiviteten av musklene innervert av disse celler.
Effekten av glysin reduseres av stryknin , som fungerer som en antagonist og blokkerer bindingsstedet til glysinreseptoren, og stivkrampetoksin , som hemmer frigjøringen av glysin. Å blokkere glysinreseptorene eller redusere glykinnivået reduserer inhiberingen av motorisk neuronaktivitet, noe som kan føre til livstruende kramper.
Glycinencefalopati kan skyldes unormal akkumulering av glysin .
bruk
Glysin tilsettes mat som smaksforsterker .
Glysin og dets natriumsalt er generelt godkjent i EU som et tilsetningsstoff med nummer E 640 uten maksimale mengderestriksjoner for mat, negative helseeffekter er ikke kjent.
Glysin er også en komponent i infusjonsløsninger for parenteral ernæring.
Ved monopolær transuretral reseksjon kan glysin brukes som tilsetningsstoff til vanningsvæsken i tillegg til en blanding av mannitol og sorbitol .
I molekylær biologisk og biokjemisk forskning, er glycin anvendes i form av en TRIS -glycin -buffer-system for protein separasjon ved hjelp av SDS-PAGE ; glycinionene fungerer som sekundære ioner i stablegelen.
litteratur
- G. Löffler, PE Petrides: Biokjemi og patobiokjemi. 7. utgave. Springer Verlag, 2003, ISBN 3-540-42295-1 .
weblenker
Individuelle bevis
- ↑ Oppføring på GLYCINE i CosIng-databasen til EU-kommisjonen, åpnet 8. juli 2020.
- ↑ Oppføring på E 640: Glysin og dets natriumsalt i den europeiske databasen for tilsetningsstoffer, tilgjengelig 11. august 2020.
- ↑ a b c d e f Oppføring av glysin i GESTIS stoffdatabase til IFA , åpnet 17. desember 2019. (JavaScript kreves)
- ^ A b F. A. Carey: Organisk kjemi. 5. utgave The McGraw Companies, 2001, s. 1059, Link
- ↑ Hans-Dieter Jakubke, Hans Jeschkeit: aminosyrer, peptider, proteiner , Verlag Chemie, Weinheim, s. 38–43, 1982, ISBN 3-527-25892-2 .
- ↑ a b c d e Robert C. Weast (red.): CRC Handbook of Chemistry and Physics . 1. Studentutgave. CRC Press, Boca Raton, Florida 1988, ISBN 0-8493-0740-6 , s. C-706.
- ↑ David R. Lide (red.): CRC Handbook of Chemistry and Physics . 90. utgave. (Internett-versjon: 2010), CRC Press / Taylor og Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, s. 5-22.
- ↑ H. Braconnot, sur la konvertering des MATIERES animales eget Nouvelles stoffer par le moyen de l`acide sulfurique., Ann. Chim. Phys., Bind 10, s. 29ff (1819).
- ↑ S. Hansen: Oppdagelsen av proteinogene aminosyrer fra 1805 i Paris til 1935 i Illinois. ( Memento fra 15. juni 2016 i Internet Archive ) Berlin 2015.
- ↑ PM Hardy: Protein aminosyrer. I: GC Barrett (red.): Kjemi og biokjemi av aminosyrene. Chapman and Hall, 1985, ISBN 0-412-23410-6 , s.9 .
- T W. Ternes, A. Täufel, L. Tunger, M. Zobel (red.): Lebensmittel-Lexikon. 4. utgave. Behr's Verlag, Hamburg 2005, ISBN 3-89947-165-2 , s. 62f.
- ↑ næringsdatabase fra US Department of Agriculture , 22. utgave.
- ↑ Hans-Dieter Jakubke, Hans Jeschkeit: aminosyrer, peptider, proteiner , Verlag Chemie, Weinheim, s. 19, 1982, ISBN 3-527-25892-2 .
- ↑ NASA-forskere gjør første oppdagelse av Livets byggestein i Comet nasa.gov, august 2009; Byggesteiner i livet fra hele Spektrum.de, august 2009 (åpnet 4. oktober 2010).
- ↑ Jamie E. Elsila, et al.: Cometary glycin påvist i prøver returnert av Stardust. Meteoritics & Planetary Science 44, No. 9, 1323-1330 (2009), pdf online @ gsfc.nasa.gov, åpnet 23. november 2011.
- Gang Wolfgang Stieler: Aminosyre funnet i kometer. Heise.de, Technology Review, 27. mai 2016.
- ^ Georg Löffler, Petro E. Petrides, Peter C. Heinrich: Biochemistry & Pathobiochemistry. Springer Medizin Verlag, Heidelberg 2006, ISBN 3-540-32680-4 , s. 1040.
- ↑ S. Ebel, HJ Roth (red.): Leksikon av farmasi. Georg Thieme Verlag , 1987, ISBN 3-13-672201-9 , s. 28.
- ^ Dawkins GPC og Miller R. En sorbitol-mannitol-løsning for urologisk elektrokirurgisk reseksjon - en tryggere væske enn glycin 1,5% europeisk urologi 1999; 36: 99-102.
- ↑ UK Laemmli: spaltning av strukturelle proteiner under montering av hodet til bakteriofag T4. I: Natur . Vol. 227, 1970, s. 680-685, doi: 10.1038 / 227680a0 , PMID 5432063 .








