Cystein
| Strukturell formel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
| Struktur av L- cystein, den naturlig forekommende enantiomeren | ||||||||||||||||||||||
| Generell | ||||||||||||||||||||||
| Etternavn | Cystein | |||||||||||||||||||||
| andre navn |
|
|||||||||||||||||||||
| Molekylær formel | C 3 H 7 NO 2 S | |||||||||||||||||||||
| Kort beskrivelse |
fargeløst fast stoff med en karakteristisk lukt |
|||||||||||||||||||||
| Eksterne identifikatorer / databaser | ||||||||||||||||||||||
| ||||||||||||||||||||||
| eiendommer | ||||||||||||||||||||||
| Molarmasse | 121,16 g mol −1 | |||||||||||||||||||||
| Fysisk tilstand |
fast |
|||||||||||||||||||||
| Smeltepunkt |
220-228 ° C |
|||||||||||||||||||||
| pK s verdi |
|
|||||||||||||||||||||
| løselighet |
|
|||||||||||||||||||||
| sikkerhetsinstruksjoner | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toksikologiske data | ||||||||||||||||||||||
| Så langt som mulig og vanlig, brukes SI-enheter . Med mindre annet er oppgitt, gjelder opplysningene standardbetingelser . | ||||||||||||||||||||||
Cystein (uttales: cyste-in), forkortet til Cys eller C , er en α - aminosyre med den sidekjede-CH 2 -SH som inneholder svovel . Bare den naturlig forekommende enantiomeriske formen L - cystein [synonym: ( R ) -cystein] er en proteinogen aminosyre; hos voksne kan det dannes i leveren fra den svovelholdige aminosyren L - metionin .
Oksidasjon av sulfhydrylgruppene gjør at to cysteinrester kan danne en disulfidbro med hverandre , noe som skaper cystin . Slike disulfidbroer stabiliserer den tertiære og kvaternære strukturen til mange proteiner og er viktige for dannelsen og opprettholdelsen av funksjonelle konformasjoner .
Isomerisme
Cystein kan eksistere i de enantiomere formene D og L , med bare L- formen som forekommer i proteiner . Siden svovel er prioritert høyere enn oksygen i henhold til CIP-nomenklaturen , er L- cystein - som disulfid L - cystin og L - selenocystein - en proteinogen aminosyre med en ( R ) konfigurasjon .
I denne artikkelen gjelder informasjonen om fysiologi L- cystein alene . Hvis det snakkes om cystein uten tilsetning , menes generelt L- cystein. Det racemiske DL- cysteinet [synonym: ( RS ) -cystein] og enantiomerisk rent D- cystein [synonym: ( S ) -cysteinet] er syntetisk tilgjengelig og har liten praktisk betydning.
Den racemisering av L- aminosyrer som kan benyttes for aminosyre dateres - et aldersbestemmelse for fossilt benmateriale.
| Enantiomerer av cystein | ||
| Etternavn | L- cystein | D- cystein |
| andre navn | ( R ) -stein | ( S ) -cystein |
| Strukturell formel |  |
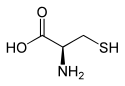
|
| CAS-nummer | 52-90-4 | 921-01-7 |
| 3374-22-9 (racemat) | ||
| EF-nummer | 200-158-2 | 213-062-0 |
| 222-160-2 (racemat) | ||
| ECHA- infokort | 100.000 145 | 100.011.875 |
| 100.020.147 (racemat) | ||
| PubChem | 5862 | 92851 |
| 594 (racemate) | ||
| DrugBank | DB00151 | DB03201 |
| - (racemate) | ||
| FL-nummer | 17.033 | - |
| Wikidata | Q186474 | Q16633812 |
| Q27089394 (racemat) | ||
historie
L- cystein ble først isolert som cystin i 1810 av den engelske naturvitenskapsmannen William Hyde Wollaston fra nyrestein, som navnet ( gammelgresk κύστις küstis , tysk 'blære' , ' urinblære ') er avledet fra. Wollaston kalte først det nye stoffet for "cystisk oksid" før Jöns Jakob Berzelius senere kalte det cystin. Den svenske kjemikeren Count Mörner lyktes i å isolere den fra proteiner for første gang i 1899. Før det hadde Freiburg-professoren Eugen Baumann lyktes for første gang i å oppnå den faktiske aminosyren cystein ved å redusere cystin. Emil Fischer var endelig i stand til å forklare strukturformelen til cystein uten tvil.
Hendelse
L- cystein finnes i proteiner, men ikke alle proteiner inneholder cystein. Beregningsanalyse av 207 ikke-relaterte proteiner viste en gjennomsnittlig massefraksjon på 2,6% cystein; i samme analyse ble 1,7% cystein bestemt for myseprotein .
Høyt L- cysteininnhold (og dermed høy stabilitet) kan finnes f.eks. B. i keratin : fjærkeratin inneholder ca. 7%, ullkeratin 11 til 17% cystein. Men selv veldig små sterisk stabiliserte proteiner som slangetoksiner ( myotoksin , nevrotoksin osv., Ca. 40 til 70 aminosyrer) inneholder 10 til 14% cystein i form av cystin (disulfidbroer).
Mat
Følgende eksempler gir en oversikt over cysteininnholdet og relaterer hver til 100 g av maten; prosentandelen cystein i det totale proteinet er også gitt.
| Mat | Totalt protein | Cystein | andel av |
|---|---|---|---|
| Svin, rå | 20,95 g | 242 mg | 1,2% |
| Kyllingbrystfilet, rå | 21,23 g | 222 mg | 1,0% |
| Laks, rå | 20,42 g | 219 mg | 1,1% |
| Kyllingegg | 12,57 g | 272 mg | 2,2% |
| Kumelk, 3,7% fett | 3,28 g | 30 mg | 0,9% |
| Solsikkefrø | 20,78 g | 451 mg | 2,2% |
| Valnøtter | 15,23 g | 208 mg | 1,4% |
| Hele hvetemel | 13,70 g | 317 mg | 2,3% |
| Fullkornsmel | 6,93 g | 125 mg | 1,8% |
| Ris, avskallet | 7,94 g | 96 mg | 1,2% |
| Soyabønner, tørket | 36,49 g | 655 mg | 1,8% |
| Erter, tørket | 24,55 g | 373 mg | 1,5% |
Cystein er en av de ikke-essensielle aminosyrene. I det minste for voksne regnes det som sikkert at kroppen også kan syntetisere alle cysteinbehov fra den essensielle aminosyren metionin , så lenge dietten inneholder nok av det. Om cystein i sin tur er i stand til å erstatte en del av metioninet er fortsatt gjenstand for forskning. Noen ganger er cystein og metionin gruppert under betegnelsen svovelholdige aminosyrer, og et vanlig krav er oppgitt. Det skal bemerkes at dette ikke er et reelt kombinert krav, men bare metioninkravet i et cysteinfritt kosthold.
Begrepene cystein og cystin brukes ofte synonymt i litteraturen og næringsdatabaser når man spesifiserer cysteininnholdet. Strengt tatt er dette ikke riktig, ettersom cystein betegner monomeren og cystin betegner dimeren dannet av en svovelbro. Imidlertid kvantifiserer mange vanlige analysemetoder ikke de to forbindelsene hver for seg.
Biokjemisk betydning
Ulike funksjoner av cystein i organismen er avledet fra den relative reaktiviteten til dens frie tiolgruppe . Under proteinfolding kan det for eksempel dannes en disulfidbro (–S - S–) mellom cysteinrester av samme polypeptidkjede , som kommer i romlig nærhet til hverandre under foldeprosessen. Broen av en ytterligere kovalent binding mellom aminosyrer i ikke-tilstøtende posisjoner i kjeden øker stabiliteten til deres romlige arrangement, den tertiære strukturen . I det foldende proteinmolekylet, under påvirkning av proteindisulfidisomeraser, kan en disulfidbro, også kjent som en cystinbro , muligens flyttes til andre cysteinrester. Tverrbroene dannet av S- atom av cysteinrester spiller en viktig rolle i foldingen av det opprinnelige proteinet og stabiliserer dets tertiære struktur gjennom kovalente bindinger. Stabiliserende disulfidbroer forekommer i mange, hovedsakelig sekretoriske og ekstracellulære proteiner, for eksempel i insulin . De kan også stabilisere den kvaternære strukturen til et proteinkompleks som består av flere polypeptidkjeder eller lenkkjeder med hverandre, for eksempel i tilfelle av antistoffer , og knytte lenker for å danne bunter, som i tilfelle keratiner . Når det gjelder korte peptider med cystein i kjedeenden, slik som nonapeptid oksytocin , et proteohormon , skaper dannelsen av en disulfidbro en ringformet struktur som gjør uspesifikk nedbrytning av peptidaser vanskeligere.
En større gruppe enzymer har jern-svovelklynger koordinert av cysteinrester . Den relativt reaktive tiolgruppen av cystein kan også være direkte involvert i den katalytiske mekanismen, som i glyceraldehyd-3-fosfatdehydrogenase , hvor cystein binder substratet til det aktive stedet.
Cystein er også et utgangsmateriale i biosyntese av forbindelser som glutation , koenzym A og taurin .
eiendommer
Cystein er hovedsakelig til stede som et "indre salt" eller zwitterion , hvis dannelse kan forklares med det faktum at protonen til karboksygruppen vandrer til det ene paret elektroner på nitrogenatomet i aminogruppen :
Zwitterion vandrer ikke i det elektriske feltet fordi det er fulladet. Strengt tatt er dette tilfelle ved det isoelektriske punktet (ved en viss pH-verdi), hvor cystein også har sin laveste løselighet i vann. Det isoelektriske punktet til cystein er ved pH 5,02.
Cystein kan telles blant ikke- essensielle aminosyrer da det kan produseres av kroppen. Imidlertid er den essensielle aminosyren metionin nødvendig for dette. Derfor anses cystein vanligvis å være semi-essensiell. Som en komponent i mange proteiner og enzymer er det ofte involvert i den katalytiske mekanismen.
- Sidekjede : hydrofil
- Van der Waals-volum : 86
- Grad av hydrofobisitet : 2.5
I en nøytral til alkalisk vandig løsning, når det utsettes for luft, finner det seg oksidasjon til cystin . Ved eksponering for sterkere oksidasjonsmidler dannes cysteinsyre .
Teknisk utvinning
Som nesten alle andre aminosyrer, kan L- cystin oppnås gjennom hydrolyse gjennom virkningen av saltsyre på proteiner som keratin (hovedsakelig fra keratinrikt vev som menneske- eller dyrehår eller fjær) . L- cystinet oppnådd på denne måten kan deretter omdannes til L- cystein ved elektrokjemisk reduksjon .
Siden i dag er det en klar trend fra animalske produkter til plantebaserte alternativer blant forbrukere. Cystein, som ble hentet fra plantekilder, blir nå også brukt. Dette lages ved gjæring fra råvarer på vegansk basis og uorganiske sporstoffer. The L -cystein brukes i baking bransjen som Teigweichmacher.
For en stund nå er representasjonen også ved gjæring med bakterier , z. B. Escherichia coli , også mulig ved bruk av genetisk modifiserte organismer (se illustrasjon av tryptofan ).
Racemisk cystein ( DL- cystein) kan oppnås fullstendig syntetisk fra 2-kloracetaldehyd , natriumhydrogensulfid , ammoniakk og aceton via mellomproduktet 2,2-dimetyl-3-tiazolin oppnådd etter Asinger-reaksjonen . Deretter ble hydrogencyanid glødet og syrehydrolyse.
Biosyntese og metabolisme
Cystein dannes biosyntetisk i leveren fra serin , som gir den grunnleggende strukturen, og metionin via homocystein , som bidrar med SH-gruppen . Enzymer cystathionine synthetase og cystathionase er nødvendige for dette. Som et resultat hemmer mangel på serin eller metionin cysteinsyntese.
Aminosyren kan brytes ned av α, β - eliminering . Dette gir aminoakrylat og hydrogensulfid (H 2 S). H 2 S oksyderes til sulfat (SO 4 2− ). Aminoakrylat isomeriserer til iminopropionate , som hydrolytisk spalter av dets aminogruppe, og dermed blir pyruvat .
Det kan også bli β-merkaptopyruvat gjennom transaminering . Sulfittoverføringen overfører sulfitt til tiolgruppen og omdanner den til et tiosulfat . Etter hydrolyse av karbon-svovelbindingen frigjøres deretter pyruvat; tiosulfatet (S 2 O 3 2− ) oksyderes til sulfatet. Cystein kan også oksyderes i SH-gruppen og deretter dekarboksyleres til taurin .
Ved genetiske mangler i mage i Cystintransportør og en gjenopptakelse, etter opptak i nyrene i cystinuri oppstår. Den mutasjon i genet rBAT også påvirker metabolismen av aminosyrer som lysin , arginin og ornitin , dvs. polyamino-aminosyrer.
Terapeutiske funksjoner
Aktive farmasøytiske ingredienser produseres fra L- cystein i industriell skala, f.eks. B. ( R ) - S - karboksymetylcystein og ( R ) - N - acetylcystein (henholdsvis ACC og NAC). Disse to aktive farmasøytiske ingrediensene brukes som orale mucolytika for å smøre det ofte tyktflytende bronkialslimet ved kronisk bronkitt og kronisk obstruktiv lungesykdom. Når cystein gis, blir det økte bronkialslimet som dannes i løpet av disse sykdommene tynnere og kan derfor hostes lettere. Cystein øker også en rekke lymfocyttfunksjoner, for eksempel cytotoksisk T-celleaktivitet. Cystein og glutation forhindrer ekspresjon av NF-AT , den nukleære transkripsjonsfaktoren, i stimulerte T-cellelinjer . In vitro-studier viser at den stimulerende effekten av TNF ( tumornekrosefaktor ), indusert av frie radikaler, på HIV- replikasjon i monocytter kan inhiberes av svovelholdige antioksidanter. Disse grunnleggende studiene antyder at behandling av inflammatoriske sykdommer og AIDS med cystein kan være nyttig med det.
Cystein kan komplekse tungmetallioner . Det brukes derfor blant annet som et terapeutisk middel for sølvforgiftning . Siden det binder frie radikaler til tiolgruppen , brukes cystein også for å forhindre strålingsskader . Hos fostre, premature babyer og nyfødte, så vel som i levercirrhose , er aktiviteten til enzymet cystathionase enten fraværende eller sterkt begrenset. I disse tilfellene er det nødvendig med en eksogen tilførsel av cystein. Det er en radikal rensemaskin som gjør de celleskadelige stoffene ufarlige, og som en viss forebyggende funksjon mot nevrodegenerative sykdommer postuleres i nylig studier .
Ved det sjeldne nevrodegenerering med hjerne jernakkumulering bevirker en mutasjon i enzymet pantotenat kinase koding PANK2 gen at det vil bli en opphopning av cystein jern - komplekser i hjernen - særlig i globus pallidus og substantia nigra pars reticulata er -. Dette fører igjen til en økning i frie radikaler og til slutt til oksidativ skade på nervecellene i hjernen.
Cystein er en komponent av aminosyreinfusjonsløsninger for parenteral ernæring.
Tilsetningsstoff
L- cystein brukes i form av hydrokloridet som et melbehandlingsmiddel og bakemiddel ved fremstilling av bakevarer . Det myker opp limet ved å depolymerisere molekylene i gluteninfraksjonen gjennom tiol-disulfid-utveksling med de intermolekylære disulfidbindinger ( dvs. bryte bindingene som holder langkjedede molekyler sammen). Som et resultat blir deigen mer elastisk og utvikler seg raskere. Med høy-gluten mel , kan et høyere volum av bakevarer oppnås fordi den drivgass (for eksempel karbondioksyd som dannes ved den gjær ) kan løsne deigen lettere. Cysteinhydroklorid kan også tilsettes til produksjonen av pasta for å øke produksjonen av deigen (et tilskudd på 0,01% forkorter blandings- eller eltetiden med 15–20%). Det hemmer dannelsen av melanoidiner ved ikke-enzymatisk garvning og motvirker dermed misfarging. I tillegg til disse bruksområdene fungerer cystein, i likhet med andre aminosyrer, som en smak , smakforsterker og næringsstoff .
L- cysteinhydroklorid eller hydrokloridmonohydrat er godkjent i henhold til europeisk matlov som tilsetningsstoff uten maksimal mengdebegrensning ( quantum satis ) under nummer E 920 . I prinsippet skal det bli erklært, men ikke hvis det ikke lenger er teknologisk effektive i den merkede produktet i samsvar med artikkel 20 i Food Information vedtekter og § 9, punkt 8, nr 1 av Additiv Authorization forordningen . Ifølge Backmittelinstitut (et anlegg fra Association of Baking Ingredients ), strekker den teknologiske effektiviteten til cystein, som brukes som et melbehandlingsmiddel (dvs. det ble tilsatt melet før deigen), ikke til den ferdigbakte varer, men til deigen , hvis den brukes som et halvfabrikat . Som et resultat trenger den ikke å merkes for ferdige bakevarer. Den Federation of tyske Forbruker Organisasjoner deler ikke dette juridisk uttalelse.
Ytterligere bruksområder
I japanske frisørsalonger erstatter cystein, som er i stand til å bryte disulfidbindinger i keratin, den sterkt luktende tioglykolsyren som er vanlig i Europa når det gjelder å forberede håret på permanente bølger . Cystein brukes også i andre kosmetiske produkter.
weblenker
Individuelle bevis
- ↑ Oppføring på E 920: L-cystein i den europeiske databasen for tilsetningsstoffer, tilgjengelig 11. august 2020.
- ↑ Oppføring på CYSTEINE i CosIng-databasen til EU-kommisjonen, åpnet 11. august 2020.
- ↑ a b c d e f datablad (R) - (+) - cystein (PDF) fra Merck , åpnet 23. mars 2011.
- ↑ a b c David R. Lide (red.): CRC Handbook of Chemistry and Physics . 90. utgave. (Internett-versjon: 2010), CRC Press / Taylor og Francis, Boca Raton, FL, Egenskaper av aminosyrer, s. 7-1.
- ↑ a b c Oppføring på L-cystein. I: Römpp Online . Georg Thieme Verlag, åpnet 21. juli 2011 ..
- ↑ Hans-Dieter Jakubke, Hans Jeschkeit: aminosyrer, peptider, proteiner , Verlag Chemie, Weinheim, 62, 1982, ISBN 3-527-25892-2 .
- ^ William Hyde Wollaston: On Cystic Oxide, a New Species of Urinary Calculus . I: Phil. Trans. Royal. Soc. teip 100 , 1810, s. 223 ff . (Engelsk).
- ↑ Sabine Hansen: Oppdagelsen av proteinogene aminosyrer fra 1805 i Paris til 1935 i Illinois. Berlin 2015.
- ↑ Eugen Baumann: Om cystin og cystein . I: Journal of Physiological Chemistry . teip 8 , nei. 4 , 1884, s. 299 ff .
- ^ Emil Fischer, K. Raske: Konvertering av l-serin til aktiv naturlig cystin . I: Rapporter fra German Chemical Society . teip 41 , nei 1 , 1908, s. 893 ff .
- ↑ Abby Thompson, Mike Boland, Harjinder Singh: Melkeproteiner: Fra uttrykk til mat . Academic Press, 2009, ISBN 978-0-08-092068-9 , pp. 492 (engelsk, begrenset forhåndsvisning i Google Book-søk).
- ↑ David Plackett: Biopolymerer: Nye materialer for bærekraftige filmer og belegg . Wiley, 2011, ISBN 978-1-119-99432-9 , pp. 115 (engelsk, begrenset forhåndsvisning i Google Book-søk).
- ↑ næringsdatabase fra US Department of Agriculture , 22. utgave.
- ↑ Ronald O. Ball, Glenda Courtney-Martin, Paul B. Pencharz: In vivo sparing av metionin av cystein i svovelaminosyre krav i dyremodeller og voksne mennesker . I: The Journal of Nutrition . teip 136 , 6 Suppl, juni 2006, ISSN 0022-3166 , s. 1682S-1693S , PMID 16702340 (engelsk).
- ↑ M. Aristoy, F. Toldra: Amino Acids . I: LML Nollet (red.): Håndbok for matanalyse . 2. utgave. Marcel Dekker AG, New York / Basel 2004, ISBN 0-8247-5036-5 , s. 95, 110 (engelsk).
- ↑ Peter Heinrich, Matthias Müller, Lutz Graeve (red.): Löffler / Petrides biokjemi og Pathobiochemistry. 9. utgave, Springer-Verlag, Heidelberg 2014, ISBN 978-3-642-17971-6 , s. 485.
- ↑ JM Berg, JL Tymoczko, L. Stryer: Biochemistry. 6. utgave. Spektrum Akademischer Verlag, Elsevier GmbH, München 2007, ISBN 978-3-8274-1800-5 , s. 38f, 48, 494f, 570.
- ^ D. Doenecke, J. Koolman, G. Fuchs, W. Gerok: Karlsons Biochemie und Pathobiochemie . Red.: Peter Karlson, Detlef Doenecke. 15. helt revidert. og redesignet utgave. Thieme, Stuttgart 2005, ISBN 3-13-357815-4 , s. 41, 208, 219 .
- ↑ PM Hardy: Protein aminosyrer . I: GC Barrett (red.): Kjemi og biokjemi av aminosyrene . Chapman and Hall, London / New York 1985, ISBN 0-412-23410-6 , pp. 9 (engelsk).
- ↑ a b Plantebasert L-cystein for mykning av deig. wacker.com, åpnet 8. august 2020 .
- ↑ Jürgen Martens , Heribert Offermanns , Paul Scherberich: En enkel syntese av racemisk cystein. I: Angewandte Chemie . Volum 93, 1981, s. 680, doi: 10.1002 / ange.19810930808 ; Angewandte Chemie International Edition. Engelsk, bind 20, 1981, s. 668, doi: 10.1002 / anie.198106681 .
- ↑ P. Fürst, H.-K. Biesalki blant andre: ernæringsmedisin . Red.: Hans-Konrad Biesalski, Olaf Adam. 3., eksp. Utgave. Thieme, Stuttgart 2004, ISBN 3-13-100293-X , s. 94 .
- ↑ B. Zhou, SK Westaway, B. Levinson, MA Johnson, J. Gitschier, SJ Hayflick: A novel pantotenat kinase-genet (PANK2) er defekt i Hallervorden-Spatz-syndrom . I: Naturgenetikk . teip 28 , nr. 4. august 2001, ISSN 1061-4036 , s. 345-349 , doi : 10.1038 / ng572 , PMID 11479594 (engelsk).
- ^ Siegfried Ebel, Hermann J. Roth (red.): Leksikon av farmasi . Thieme, Stuttgart 1987, ISBN 3-13-672201-9 , pp. 66 .
- ↑ a b Hans-Dieter Belitz , Werner Grosch , Peter Schieberle : Lærebok om matkjemi . 6. helt reviderte utgave. Springer, Berlin / Heidelberg 2008, ISBN 978-3-540-73201-3 , doi : 10.1007 / 978-3-540-73202-0 .
- Ku Peter Kuhnert: Leksikon av tilsetningsstoffer . 4., fullstendig revidert utgave. Behr, Hamburg 2014, ISBN 978-3-95468-118-1 .
- ↑ Forordning (EF) nr. 1333/2008 i den konsoliderte versjonen av 9. februar 2016
- ↑ Forordning (EU) nr. 231/2012 i den konsoliderte versjonen av 20. oktober 2015
- ↑ Martina Bröcker, Amin Werner: Den teknologiske effektiviteten til tilsetningsstoffer i brød, kjeks, fine bakevarer og deigstykker . I: bmi aktuell . Desember 2007 ( wissensforum-backwaren.de [PDF; 134 kB ]). Den teknologiske effektiviteten av tilsetningsstoffer i brød, småvarer, fine bakevarer og deigemnene ( Memento av den opprinnelige fra 06.04.2016 i Internet Archive ) Omtale: The arkiv koblingen er satt inn automatisk og har ennå ikke blitt sjekket. Kontroller originalen og arkivlenken i henhold til instruksjonene, og fjern deretter denne meldingen.
- Melbehandlingsmidler . Consumer Association Federal Association e. V., åpnet 7. april 2016 .



