5'-hette struktur
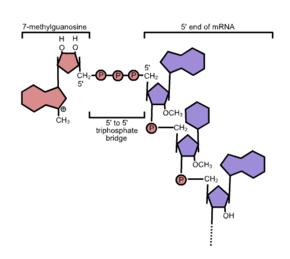
Den 5 'cap struktur (fra engelsk cap , cap') er en hetteliknende innretning i den 5 'ende av mRNA- molekyler, som i cellekjernen av eukaryote celler tilsettes. 5'-hetten beskytter ikke bare et RNA fra nedbrytning, men er også viktig for eksport av et mRNA fra kjernen til cytoplasmaet og for oversettelse av mRNA av ribosomer .
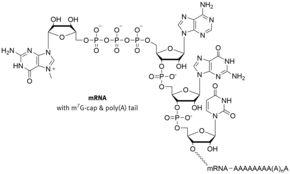
Ofte er disse i 5'-hetten strukturen er en modifisert guanin - nukleotid som har en sjelden 5'-5 ' fosfodiesterbinding er knyttet til hodeenden av RNA. Denne kjemiske reaksjonen, kjent som capping , finner sted under transkripsjonen av et gen så snart en RNA-polymerase har koblet de første nukleotidene til et mRNA . I motsetning til (kotranskriptionellen) avkorting av 5'-enden som er polyadenylering av 3'-enden av - en mRNA- haling (fra engelsk hale , hale ') sa tilsetningen av en poly (A) hale - en post-transkripsjonell modifikasjon , bare etter at separasjon av mRNA og RNA-polymerase er utført.
I tillegg til mRNA, finnes capping også i mange ikke-kodende RNAer . Som et alternativ til cap-strukturen bruker noen RNA-virus IRES eller cap-uavhengige oversettelseselementer for å initiere oversettelse .
Cap strukturer
Polymerase II
Den klassiske m 7 G- hetten finnes i mRNAer som er transkribert av RNA-polymerase II . Her (etter hydrolyse av terminal γ-fosfat av trifosfatase) overføres en GMP- rest (fra GTP ) i form av en 5'-5'-trifosfatbinding til 5'-enden av RNA ved den såkalte capping enzym og deretter i posisjon 7 av guaninet ved hjelp av mRNA-cap-metyltransferase med forbruk av S- adenosylmetionin (SAM), en universal metylgruppedonat, metylert , resultatet: 5'-5 'm 7 GpppN. I tillegg forekommer ytterligere metyleringer av de første basene av mRNA i posisjon 2 ', man snakker da om Cap1 (bare den første metylerte basen) eller Cap2 (de to første basene metylerte).
Du kan også finne z. B. i trypanosomer mye mer kompliserte hettekonstruksjoner der ikke bare det første nukleotidet er modifisert, men også de følgende (f.eks. Trypanosoma brucei Cap-4).
Polymerase III
RNA-polymerase III-transkripsjoner inneholder ikke slike 5'-cap-strukturer, men noen få RNA har monometylering på en γ-fosfatrest (f.eks. U6 snRNA).
Virus
Noen virus viser en særegenhet i den biosyntetiske banen til hettestrukturen: GTP blir først metylert og først deretter overført til RNA.
funksjon
Som poly (A) halen ved 3'-enden av mRNA, spiller hetten på strukturen en viktig rolle i stabiliseringen av mRNAene. Uten denne strukturen nedbrytes mRNAene i cytoplasmaet raskt fra 5 'til 3' av eksonukleaser .
Hettestrukturen spiller også en viktig rolle i utslipp av RNA fra cellekjernen gjennom kjerneporene i cytoplasmaet (RNA-eksport). Det er bundet av hettebindende kompleks under transkripsjon , som sammen med andre faktorer sikrer effektiv transport.
Kappestrukturen er også av avgjørende betydning for igangsetting av oversettelse . Både bundet av CBC (i løpet av første runde med oversettelse) og av eIF4E (under alle påfølgende runder) sørger det for at ribosomet rekrutteres og begynner med initialiseringen. Dette fører til en ringlukking av RNA (lukket sløyfemodell for translasjon), der 5'-enden interagerer med poly A-halen (via eIF4E, eIF4G og det cytoplasmatiske poly A-bindende proteinet PABPC).
Fordi noen virus replikerer seg utelukkende i cytoplasmaet, mottar de ikke en hette-struktur fra mobilmaskineriet. For å kompensere for ulempene dette medfører, stjeler de en hette fra cellulære mRNAer, kjent som cap-snapping . Et mRNA fra vertsorganismen spaltes nær 5'-enden (som selvfølgelig har hetten) og brukes som en såkalt avkortet leder for å initiere viral oversettelse.
Det faktum at virale polymeraser ikke produserer m 7 G-Cap muliggjør en spesifikk differensiering mellom "fremmed" og "endogent" RNA - et RNA som bare bærer en ung cap th trifosfat i 5'-enden kan brukes som en indikasjon på Infeksjon gjelder. Faktisk, i det medfødte immunforsvaret (hvis grunnleggende oppgave er å skille mellom "fremmed" og "selv"), er RIG-I en intracellulær reseptor som gjenkjenner denne strukturen som PAMP og deretter utløser en antiviral immunrespons.
litteratur
- Rolf Knippers: Molecular Genetics. 8. reviderte utgave. Georg Thieme Verlag, Stuttgart et al. 2001, ISBN 3-13-477008-3
- reactome: mRNA capping - doi : 10.3180 / REACT_1470.1
Individuelle bevis
- ↑ Hornung et al.: 5′-trifosfat RNA er liganden for RIG-I , I: Science, 10. november 2006: Vol. 314 nr.5801 s. 994-997 doi : 10.1126 / science.1132505 . Opprinnelig publikasjon i Science om anerkjennelse av unge cap ter RNA